题目内容
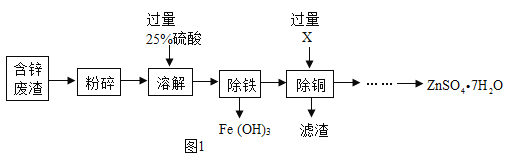
【题目】某天然矿泉水的主要成份如下,请认真阅读后填空.
主要成分(mg/L):
碳酸氢根(HCO3-):173-205 氯离子(Cl-):1.0-8.0 硫酸根(SO42-):16.08
-19.52 钠离子(Na+):8-50 PH值:7.8±0.5
(1)“SO42-”中数字“2”的含义是____________________。
(2)我们向该矿泉水滴加__________,发现有大量浮渣产生说明该矿泉水属于硬水。
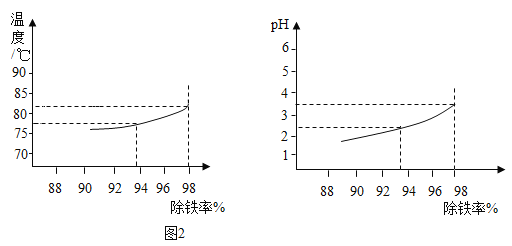
(3)天然水是混合物,用图1所示的简易装置净化水后,所得的水为_______(填纯净物或混合物)。
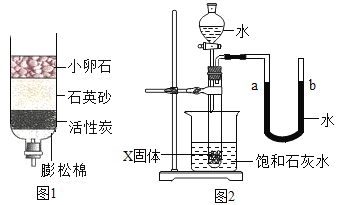
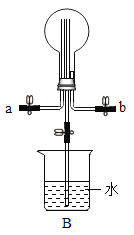
(4)如图2所示实验,将水加入到试管中,观察到a液面下降,b液面上升,饱和石灰水变浑浊,则X固体可能为__________(填物质的化学式)。
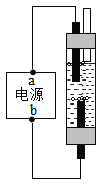
(5)如图是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氢气和氯气,该反应的化学方程式为:________________。能量变化角度看,该反应中将______转化为化学能。
【答案】每个硫酸根带两个单位负电荷 肥皂水 混合物 NaOH或CaO 2NaCl+2H2O![]() 2NaOH+Cl2↑+2H2↑ 电能
2NaOH+Cl2↑+2H2↑ 电能
【解析】
本题主要考察离子符号、物质遇水吸、放热情况以及电解氯化钠溶液的相关知识
(1)SO42-是硫酸根离子,“2”的含义是表示每个硫酸根带两个单位负电荷;
(2)肥皂水可以简单、有效的区分硬水和软水;
(3)U型管中,观察到a液面下降,b液面上升,集气瓶内压强变大,因为瓶内温度升高,物质遇水反应放热,氢氧化钠固体遇水放热,氧化钙遇水放热;
(4)2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑;
2NaOH+Cl2↑+H2↑;
(5)电能转化为化学能。

【题目】结合下列过程,回答有关问题。
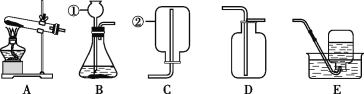
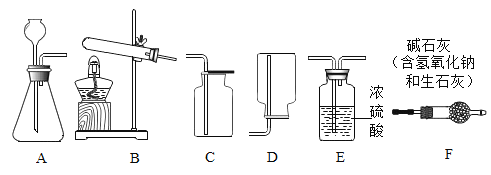
(1)写出标号仪器的名称:①____,②____。
(2)实验室制取并收集二氧化碳的装置组合为____,化学方程式为____。
(3)写出实验室用高锰酸钾制取O2的化学方程式:______。试管口放一团棉花的目的是____,用E装置收集满时,接下来的操作顺序是____(填序号)。
①用玻璃片盖住集气瓶 ②将集气瓶正放在桌面 ③熄灭酒精灯 ④移出导管
(4)向5mL 5%的H2O2溶液中加入2滴一定浓度的FeCl3溶液,立即产生大量气泡。已知FeCl3溶液中主要含有三种微粒:H2O、Fe3+、Cl-。
[问题] 哪种微粒对H2O2溶液的分解起催化作用?
[假设] 假设一:可能是H2O;假设二:可能是Fe3+;假设三:可能是Cl-。
[分析] 假设一不可能成立,理由是______。
[实验]
操作 | 现象 | 结论 |
其他条件不变,向H2O2溶液中加入NaCl溶液 | 无明显变化 | 假设____成立 |
其他条件不变,向H2O2溶液中加入Na2SO4溶液 | 无明显变化 | |
其他条件不变,向H2O2溶液中加入Fe2(SO4)3溶液 | 立即产生大量气泡 |
(5)从循环利用的角度分析,二氧化锰与氯化铁溶液相比,____(填化学式)更适合作该反应的催化剂。
【题目】学习完碱的相关知识后,某兴趣小组对“二氧化碳与碱的反应”进行了探究。
(1)甲、乙两位同学分别进行了如下实验:
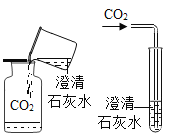
甲同学向盛有二氧化碳的集气瓶中倒入澄清石灰水,观察到石灰水先变浑浊,后变澄清;乙同学将二氧化碳通入到澄清石灰水中,观察到石灰水变浑浊。你认为____________同学的实验能验证氢氧化钙的性质,反应的化学方程式为________________。
(2)实验小组同学又将CO2通入某浓度的氢氧化钠溶液中,一段时间后,发现有固体析出。
(提出问题)析出固体的成分是什么?
(猜想与假设)同学们提出以下猜想:
猜想A:Na2CO3;
猜想B:NaHCO3;
猜想C:________________________
(进行实验)甲同学取少量固体溶于水,滴加无色酚酞溶液,溶液变红,则认为猜想A正确;乙同学认为甲同学的实验不合理,理由是________________________。
乙同学设计了以下方案进行验证:
实验步骤 | 实验现象 | 实验结论 |
①取少量固体于试管中,加水充分溶解后,加入过量的_________溶液 | 无明显现象 | 猜想B正确 |
②在①溶液中加入稀盐酸 | _____________________ |
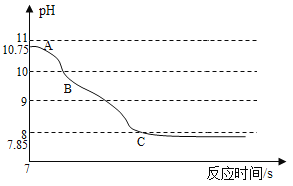
(反思交流)该小组同学将二氧化碳通入氢氧化钠溶液中,利用数字化技术测定溶液pH值变化,待完全反应后,观察到溶液中逸出大量气泡,pH出现两段S型变化曲线。
(实验分析)(3)AB段变化的原因可能是_____________________________________。BC段变化的原因可能是_______________。利用实验验证变化后的产物,实验操作为______________________.实验现象是________________.
【题目】小鹏同学家厨房的排水管道由于油渍和厨余残渣过多而造成了堵塞,通过查询资料,得知这时需要用到厨房管道疏通剂。小鹏同学购买了市场上固态、液态两种管道疏通剂,请你和同学们一起对小鹏购买的这两种管道疏通剂进行探究。
(查阅资料)
①厨房管道疏通剂的作用:快速分解菜渣、油脂、皂垢、毛发等堵塞污物,疏通管道。
②固体管道疏通剂的主要成分是氢氧化钠、硝酸钠和铝粉,氢氧化钠能使垃圾分散成小颗粒,使头发变成碎屑。
③铝粉能与![]() 反应,化学方程式为
反应,化学方程式为![]() ,并放出热量。
,并放出热量。
④液态管道疏通剂的成分主要是![]() 和一种钠盐。
和一种钠盐。
探究一:
(提出问题)固态管道疏通剂能够疏通管道的原理是什么?
(实验验证)
操作 | 现象 | 结论 |
将菜叶、头发、米饭等垃圾放入烧杯中,然后加入少量固态管道疏通剂,再加入水 | (1)烧杯中产生___________烧杯壁_____________,垃圾翻动,变成碎屑 | 反应中产生的气体和热量使垃圾翻动 |
(反思评价)
(2)同学们讨论后,认为固态管道疏通剂虽然能疏通管道,但使用过程中不安全,理由是_______________________________。
探究二:
(提出问题)液态管道疏通剂中除![]() 外,另一种钠盐是什么呢?
外,另一种钠盐是什么呢?
(猜想假设)老师提示这种钠盐是![]() 中的一种。
中的一种。
(实验验证)(不考虑疏通剂中其他成分对实验的影响)
操作 | 现象 | 结论 |
取少量液态疏通剂加入试管中,滴加 | 产生白色沉淀 | (3)琳琳认为该钠盐是 |
(提出质疑)
(4)同学们一致对琳琳的结论提出质疑,理由是___________________________。
(拓展延伸)
(5)可补充一个实验证明该钠盐是![]() ,取沉淀滴加______________(填名称),沉淀不溶解证明该钠盐是
,取沉淀滴加______________(填名称),沉淀不溶解证明该钠盐是![]() 。
。