题目内容
已知浓硝酸是一种易挥发的强酸,见光易分解,其分解的反应方程式为:4HNO3
2H2O+4NO2↑+X↑.根据上述信息,回答下列问题:
(1)浓硝酸的化学性质: (写出一条即可);
(2)HNO3中氢、氧元素的质量比: ;
(3)判断X的化学式: .
| ||
(1)浓硝酸的化学性质:
(2)HNO3中氢、氧元素的质量比:
(3)判断X的化学式:
考点:质量守恒定律及其应用,元素质量比的计算,化学性质与物理性质的差别及应用
专题:化学用语和质量守恒定律
分析:(1)根据化学性质为通过化学变化表现出来的性质,和题干对硝酸的介绍,推断硝酸的化学性质;
(2)根据水的化学式,计算出水中氢、氧元素的质量比;
(3)利用反应的化学方程式,根据反应前后原子种类、个数不变,推断生成物X的化学式.
(2)根据水的化学式,计算出水中氢、氧元素的质量比;
(3)利用反应的化学方程式,根据反应前后原子种类、个数不变,推断生成物X的化学式.
解答:解:(1)硝酸见光分解,表明硝酸化学性质不稳定,见光易分解;
(2)HNO3中氢、氧元素的质量比=1:16×3=1:48;
(3)由反应4HNO3
2H2O+4NO2↑+X↑,反应前4HNO3中含H、N、O原子个数分别为4、4、12,而反应后2H2O、4NO2中共含有H、N、O原子个数分别为4、4、10,根据反应前后原子种类、个数不变,可判断X分子由2个O原子构成,则物质X的化学式为O2.
故答案为:(1)不稳定,见光易分解;(2)1:48;(3)O2.
(2)HNO3中氢、氧元素的质量比=1:16×3=1:48;
(3)由反应4HNO3
| ||
故答案为:(1)不稳定,见光易分解;(2)1:48;(3)O2.
点评:根据化学变化前后原子的种类、数目不变,由反应的化学方程式,可以推断反应中某物质的分子构成及物质化学式的确定.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
下列实验操作中,正确的是( )
A、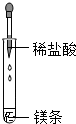 |
B、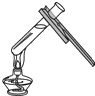 |
C、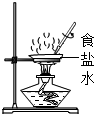 |
D、 |
下列叙述正确的是( )
| A、人体缺乏铁元素会引起贫血,所以我们应该适量补铁 |
| B、将生锈的菜刀浸泡在食盐水中,可除去其表面的铁锈 |
| C、用甲醛溶液浸泡鲜虾仁 |
| D、用清洗过的霉变大豆榨豆浆 |