题目内容
(11分)氧气和二氧化碳是初中化学常见的两种重要物质。请你参与下列氧气和二氧化碳有关制备、转化的实验探究活动。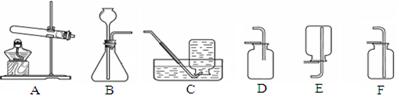
Ⅰ:实验室制取氧气和二氧化碳。
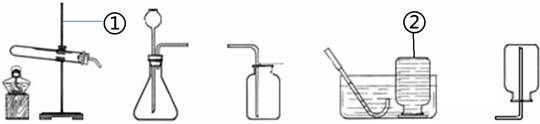
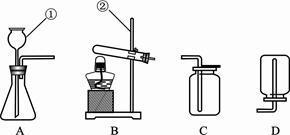
(1)用高锰酸钾制取氧气,发生反应的化学方程式是 。如果要制得较纯净的氧气,应该选择装置 (填上述装置图示中序号)收集。
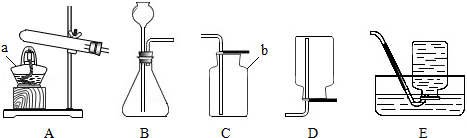
(2)制取二氧化碳,可选择图示中B与F组合为装置,需要的化学药品是 ;向B中加入药品前的一步实验操作是 。该组合装置既可用于制取二氧化碳又可用来制取氧气,其中选用相同发生装置制取二氧化碳和氧气的原因是 。
Ⅱ:用过氧化钠反应来制取氧气,是潜水员使用的供氧装置的原理。
【查阅资料】常温常压下过氧化钠是淡黄色固体,在不需要加热的情况下能与二氧化碳反应生成氧气和另一化合物(生活中常见的盐);过氧化钠能与水反应生成氧气和氢氧化钠。
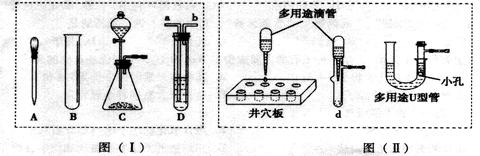
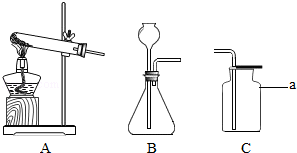
【设计装置】为验证过氧化钠(Na2O2)和CO2反应原理,设计如下实验装置。
【实验操作】向装置X中通入足量CO2气体,观察到X瓶中的淡黄色固体逐渐变为白色粉末,同时见到Y、Z装置中有气泡出现。
【实验分析】
(3)过氧化钠与二氧化碳反应除生成氧气外,另一化合物的化学式为 ;Y中的溶液是 ;Z中浓硫酸的作用是 。
(4)验证过氧化钠和二氧化碳反应生成氧气的操作是 。
(5)反应结束后,可设计一个简单实验,验证X瓶中过氧化钠是否有剩余(除用二氧化碳验证外),其实验原理是 (用化学方程式表示)。
(1)2KMnO4△K2MnO4 + MnO2 + O2 ↑(1分) ;C;2)稀盐酸和大理石(或写化学式); 气密性检查; 药品状态相同且都不需要加热;(3)Na2CO3;NaOH(或KOH、Ba(OH)2 ); 除去水蒸气;(4)在尖嘴管口收集一试管气体,将带火星的木条伸入试管内,观察木条是否复燃;(5)2Na2O2 + 2H2O ="4NaOH" + O2↑ (2分)
解析试题分析:(1)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气;氧气不易溶于水(排水法),密度比空气大(向上排空气法);
(2)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,大理石和石灰石的主要成分是碳酸钙,通常情况下,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气,与制取二氧化碳的药品状态相同且都不需要加热;(3)过氧化钠与二氧化碳反应生成碳酸钠和氧气;氢氧化钠溶液能够吸收二氧化碳气体;浓硫酸具有吸水性,可以用作某些物质的干燥剂;(4)氧气能够支持燃烧,能使带火星的木条复燃;(5)水与过氧化钠反应生成氧气和氢氧化钠,检验是否有氧气生成,来检验是否有剩余.
考点:常用气体的发生装置和收集装置与选取方法;实验室制取氧气的反应原理;氧气的检验和验满;二氧化碳的实验室制法;书写化学方程式

下表中,除去物质所含少量杂质的方法和反应类型归类均正确的是
| 选项 | 物质 | 所含杂质 | 除去方法 | 反应类型 |
| A | CuO粉 | Cu粉 | 在空气中加热 | 化合反应 |
| B | CO2 | CO | 通过灼热的CuO | 置换反应 |
| C | H2 | HCl | 通过盛氢氧化钠溶液的洗气瓶 | 分解反应 |
| D | KCl | K2SO4 | 溶解,加足量的硝酸钡溶液,并过滤 | 复分解反应 |



 NaCl+N2↑+2H2O
NaCl+N2↑+2H2O