题目内容
【题目】用化学用语填空:
(1)4个氢氧根离子________;(2)2个铜原子________;
(3)四氧化三铁________;(4)五氧化二磷中磷元素的化合价________;
(5)保持水化学性质的最小粒子________;(6)铝离子结构示意图________.
【答案】4OH-; 2Cu; Fe3O4; ![]() H2O;
H2O; 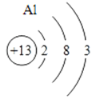
【解析】
化合物的化学式书写:显正价的元素其符号写在左边,显负价的写在右边,化合价的绝对值交叉约减,得化学式右下角的数字,数字为1时不写,化学式前边的数字表示分子的个数;单质的化学式的书写:在元素符号右下角标上一个分子中原子的个数。化学式中元素符号右下角的数字为一个分子中原子的个数。离子符号书写:元素(或根)符号右上角的数字表示一个离子带电荷的数值,数字在左,正负号在右,电荷数为1时,1不写;离子符号前加数字,表示离子的个数。元素化合价的书写:在元素符号的正上方标化合价的数值,正负号在左,数字在右。
(1)4个氢氧根离子:4OH-;
(2)2个铜原子:2Cu;
(3)四氧化三铁:Fe3O4;
(4)五氧化二磷中磷元素的化合价![]() ;
;
(5)保持水化学性质的最小粒子就是构成水的微粒水分子:H2O;
(6)铝离子结构示意图

练习册系列答案
相关题目