题目内容
【题目】某城区自来水(含有较多的可溶性钙镁化合物)在实验室通过蒸馏的方法净化水。甲是制备蒸馏水的装置,乙是电解水的装置:![]() ;
;
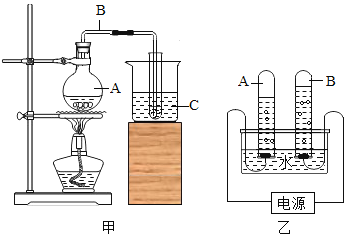
(1)用________ 鉴别该自来水和蒸馏水;生活中通过______把硬水转化为软水。
(2)从分子角度分析甲乙两个变化根本的区别是______________。
(3)举例说明分子之间有间隔 ______________;
【答案】加热蒸干,观察是否留下固体 煮沸 分子本身是否发生改变 50mL水和50mL酒精混合,液体总体积小于100mL
【解析】
(1)自来水是混合物,加热蒸干会留下固体,蒸馏水是纯净物,蒸干后,不会留下任何物质。用加热蒸干,观察是否留下固体鉴别该自来水和蒸馏水;天然水加热煮沸,水中的钙、镁化合物转化为沉淀,水的硬度降低,生活中通过煮沸把硬水转化为软水;
(2)从分子角度,甲、乙两个变化根本的区别是分子本身是否发生改变;
(3)50mL水和50mL酒精混合,液体总体积小于100mL,说明分子之间有间隔。

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目