题目内容
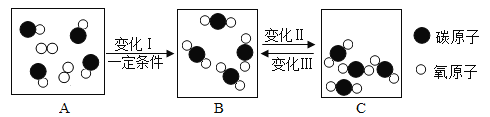
【题目】如图是某化学反应的微观示意图。

(1)该化学变化中发生改变的粒子是______(填“原子”或“分子”),反应后生成的b与c的粒子个数比为______;
(2)某物质X的燃烧反应方程式是为:X+3O2![]() 2CO2+3H2O,由此可以推断出X一定含有的元素是______,理由是______。
2CO2+3H2O,由此可以推断出X一定含有的元素是______,理由是______。
【答案】分子 2:1 碳、氢、氧 该反应的化学方程式X+3O2![]() 2CO2+3H2O,根据质量守恒定律,反应前后原子种类、数目不变,反应物中氧原子个数分别为6,反应后的生成物中碳、氧、氢原子个数分别为2、7、6,则每个X分子由2个碳、6个氢原子、1个氧原子构成,X一定含有的元素是碳、氢、氧元素
2CO2+3H2O,根据质量守恒定律,反应前后原子种类、数目不变,反应物中氧原子个数分别为6,反应后的生成物中碳、氧、氢原子个数分别为2、7、6,则每个X分子由2个碳、6个氢原子、1个氧原子构成,X一定含有的元素是碳、氢、氧元素
【解析】
(1)由化学反应的微观示意图和微粒的变化可知,反应方程式可表示为:2a=2b+c,该反应前后原子的种类、数目不变,该化学变化中发生改变的粒子是分子,反应后生成的b与c的粒子个数比为2:1;
(2)该反应的化学方程式X+3O2![]() 2CO2+3H2O,根据质量守恒定律,反应前后原子种类、数目不变,反应物中氧原子个数分别为6,反应后的生成物中碳、氧、氢原子个数分别为2、7、6,则每个X分子由2个碳、6个氢原子、1个氧原子构成,X一定含有的元素是碳、氢、氧元素。
2CO2+3H2O,根据质量守恒定律,反应前后原子种类、数目不变,反应物中氧原子个数分别为6,反应后的生成物中碳、氧、氢原子个数分别为2、7、6,则每个X分子由2个碳、6个氢原子、1个氧原子构成,X一定含有的元素是碳、氢、氧元素。

【题目】某校兴趣小组用氯酸钾制取氧气,请按下面要求计算。
(1)取氯酸钾和二氧化锰的混合物一定量放入大试管中加热,加热至不再有气体产生为止,共收集到氧气 4.8g,求混合物中氯酸钾的质量______(计算结果精确到 0.1g)。
(2)若将一定质量的氯酸钾加热,有关物质质量与反应时间的变化如表所示:
时间/min | t1 | t2 | t3 | t4 | t5 |
O2 质量/g | 2.4 | 4.8 | 7.2 | 9.6 | 9.6 |
剩余固体质量/g | 22.1 | 19.7 | m | 14.9 | 14.9 |
其中 m=_____;t3时剩余固体中含有的物质是_____(填化学式)。
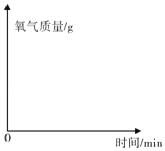
(3)若将(1)中氯酸钾平均分成两份,一份加 入 1g 二氧化锰,另一份不加,分别放入试管中,同时、同温度加热至充分反应,请在图象上画出产生O2的曲线______。