题目内容
某兴趣小组同学对实验室制备氧气的条件进行如下探究实验.
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将x g KClO3与1.0g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
Ⅰ中反应的化学方程式是
【反思】单独加热KClO3时反应缓慢,加入MnO2或CuO后反应明显加快,若要证明MnO2 和CuO是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的
(2)某同学称取-定质量的氯酸钾和二氧化锰混合物16.0g,放入大试管中加热至质量不再变化为止,称得固体质量为11.2g.
[数据处理]
(1)根据质量守恒定律,计算得到氧气的质量为
(2)计算氯酸钾的质量
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将x g KClO3与1.0g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
Ⅰ中反应的化学方程式是
2KClO3
2KCl+3O2↑
| ||
| △ |
2KClO3
2KCl+3O2↑
;Ⅱ中x的值应为
| ||
| △ |
3.0
3.0
.【反思】单独加热KClO3时反应缓慢,加入MnO2或CuO后反应明显加快,若要证明MnO2 和CuO是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的
化学性质
化学性质
和质量
质量
是否改变.(2)某同学称取-定质量的氯酸钾和二氧化锰混合物16.0g,放入大试管中加热至质量不再变化为止,称得固体质量为11.2g.
[数据处理]
(1)根据质量守恒定律,计算得到氧气的质量为
4.8g
4.8g
g.(2)计算氯酸钾的质量
12.25
12.25
g.分析:(1)根据氯酸钾在二氧化锰做催化剂的条件下分解成氯化钾和氧气分析;根据控制氯酸钾的质量相等才能比较出二氧化锰和氧化铜的催化效果分析;根据催化剂的特点进行分析.
(2)根据反应前后质量的减少量,就是生成氧气的质量,求出氧气质量,再根据化学方程式由氧气质量,计算出参加反应的氯酸钾的质量.
(2)根据反应前后质量的减少量,就是生成氧气的质量,求出氧气质量,再根据化学方程式由氧气质量,计算出参加反应的氯酸钾的质量.
解答:解:(1)Ⅰ中反应物是氯酸钾,生成物是氯化钾和氧气,用最小公倍数法配平,反应条件是二氧化锰做催化剂加热,所以方程式是:2KClO3
2KCl+3O2↑;设计对照实验时只能有一个变量,其它量必须相同,该实验的变量是催化剂的种类,所以氯酸钾的质量必须相等,所以X是3.0g;催化剂是一种物质,在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质,所以要证明MnO2 和CuO是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的质量和化学性质不变;
(2)根据质量守恒定律可知,反应前后质量的减少量,就是生成氧气的质量,所以生成氧气的质量为:16.0g-11.2g=4.8g,设要生成4.8g氧气需要参加反应的氯酸钾的质量为X,则:
2KClO3
2KCl+3O2↑
245 96
X 4.8g
根据:
=
解得X=12.25g.
故答案为:(1)2KClO3
2KCl+3O2↑;3.0;化学性质;质量;(2)4.8g;12.25.
| ||
| △ |
(2)根据质量守恒定律可知,反应前后质量的减少量,就是生成氧气的质量,所以生成氧气的质量为:16.0g-11.2g=4.8g,设要生成4.8g氧气需要参加反应的氯酸钾的质量为X,则:
2KClO3
| ||
| △ |
245 96
X 4.8g
根据:
| 245 |
| 96 |
| X |
| 4.8g |
故答案为:(1)2KClO3
| ||
| △ |
点评:本题通过实验探究了二氧化锰和氧化铜在过氧化氢制氧气中的催化作用,侧重实验能力和分析能力的考查.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
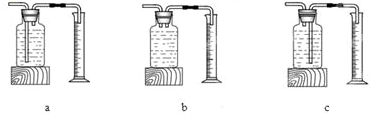
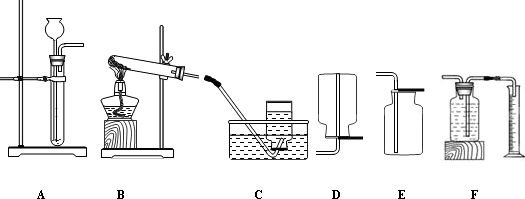

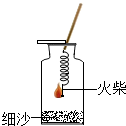 某兴趣小组同学对实验室制备氧气的条件,及氧气的性质进行如下探究.
某兴趣小组同学对实验室制备氧气的条件,及氧气的性质进行如下探究.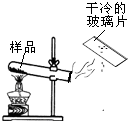
 维C泡腾片(主要成分见图1)溶于水,有许多气泡产生(如图2).某兴趣小组同学对气体的成分进行如下探究.
维C泡腾片(主要成分见图1)溶于水,有许多气泡产生(如图2).某兴趣小组同学对气体的成分进行如下探究.