题目内容
某兴趣小组同学对实验室制备氧气的条件进行如下探究实验.
①为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将3.0g KClO3与xg CuO均匀混合加热
在相同温度下,比较两组实验中相同时间内产生O2的体积.
Ⅰ中反应的化学方程式是
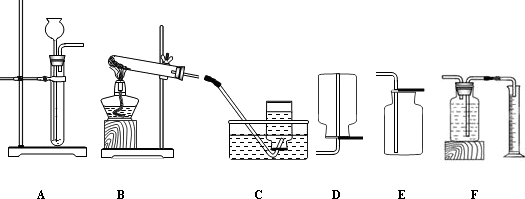
本实验中,与发生装置连接用来测量O2体积的装置可以用下图中的

②乙探究了影响双氧水分解速度的某种因素.实验数据记录如下:
为完成本实验,应选择下图气体发生和收集装置中的组合是
实验结论:在相同条件下,
①为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将3.0g KClO3与xg CuO均匀混合加热
在相同温度下,比较两组实验中相同时间内产生O2的体积.
Ⅰ中反应的化学方程式是
2KClO3
2KCl+3O2↑
| ||
| △ |
2KClO3
2KCl+3O2↑
;Ⅱ中x的值应为
| ||
| △ |
1.0
1.0
.本实验中,与发生装置连接用来测量O2体积的装置可以用下图中的
C
C
(填编号).
②乙探究了影响双氧水分解速度的某种因素.实验数据记录如下:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |
AF
AF
.(选填序号)
实验结论:在相同条件下,
双氧水的浓度越大
双氧水的浓度越大
,双氧水分解得越快.分析:氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;控制变量法只能控制一个变量,因此X是1.0;本实验中,测量O2体积的装置是C,因为氧气密度比水的密度小,必须从短管进入,才能把水排出来;由表格信息可知:在相同条件下,双氧水浓度越大,双氧水分解得快;如果用双氧水制氧气就不需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.
解答:解:①氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;控制变量法只能控制一个变量,因此X是1.0;本实验中,测量O2体积的装置是C,因为氧气密度比水的密度小,必须从短管进入,才能把水排出来;故答案为:2KClO3
2KCl+3O2↑;1.0;C
②由表格信息可知:在相同条件下,双氧水浓度越大,双氧水分解得快;如果用双氧水制氧气就不需要加热,而要完成本实验,必须用到F,才能测量出水的体积,进而测得生成氧气的体积,所以答案应为AF;故答案为:AF;双氧水的浓度越大;
| ||
| △ |
②由表格信息可知:在相同条件下,双氧水浓度越大,双氧水分解得快;如果用双氧水制氧气就不需要加热,而要完成本实验,必须用到F,才能测量出水的体积,进而测得生成氧气的体积,所以答案应为AF;故答案为:AF;双氧水的浓度越大;
点评:本考点既考查了实验步骤的设计,又考查了化学方程式的书写,还对实验进行了评价,综合性比较强.实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.

练习册系列答案
相关题目

 某兴趣小组同学对实验室制备氧气的条件,及氧气的性质进行如下探究.
某兴趣小组同学对实验室制备氧气的条件,及氧气的性质进行如下探究.

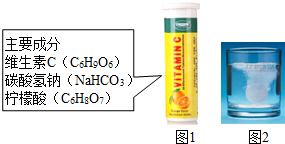 维C泡腾片(主要成分见图1)溶于水,有许多气泡产生(如图2).某兴趣小组同学对气体的成分进行如下探究.
维C泡腾片(主要成分见图1)溶于水,有许多气泡产生(如图2).某兴趣小组同学对气体的成分进行如下探究.