题目内容
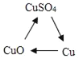
【题目】一种焰火火药中所含的硝酸铜在燃放时产生绿色火焰,发生如下反应:2Cu(NO3)2═2CuO+O2↑+4X↑。下列有关说法错误的是
A.产物中CuO属于氧化物
B.Cu(NO3)2中铜元素的化合价为+1
C.该反应的基本反应类型为分解反应
D.根据质量守恒定律可知X的化学式为NO2
【答案】B
【解析】
在硝酸铜分解的反应方程式2Cu(NO3)2═2CuO+O2↑+4X↑中,铜原子在反应前后,个数相等,氮、氧原子个数反应后比反应前分别少了4个和8个,由此可知X的化学式为NO2。
A、产物中CuO由氧元素和铜元素组成的,属于氧化物,不符合题意;
B、Cu(NO3)2中NO3的化合价为-1价,设铜元素的化合价为X,根据化合物里正负化合价为0,![]() ,则铜元素的化合价为+2,符合题意;
,则铜元素的化合价为+2,符合题意;
C、该反应由一种物质生成两种物质,基本反应类型为分解反应,不符合题意;
D、根据质量守恒定律可知X的化学式为NO2,不符合题意。故选B。

 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案【题目】水、溶液与生活息息相关。
(1)现有六个常见化学名词:乳化、溶解、煮沸、蒸馏、降温结晶、蒸发结晶。请选择适合的词填在后面的横线上。
①用洗洁精洗去衣服上的油污________________。
②海水晒盐的原理是________________。
(2)如图是A. B. C三种物质的溶解度曲线,回答下列问题:

①A. B两种物质在________________°C时溶解度相同。
②t2°C时,三种物质的溶解度由大到小的顺序是_______________。
③t2°C时,将三种物质各ag分别加入到100g水中,充分溶解后,若只有一种物质能形成饱和溶液,则a的取值范围是______________。
(3)无土栽培是利用营养液栽培作物的一种方法,以下是栽培绿叶菜营养液配方。
肥料成分 | 硝酸钙 | 硝酸钾 | 磷酸二氢钠 | 硫酸镁 | 硫酸铵 |
用量(毫克/升) | 1260 | 255 | 350 | 537 | 235 |
①该营养液中存在的铵根离子的符号_____________。
②某硫酸铵溶液pH=4.5,则硫酸铵溶液显_____________ (填“酸性”、 “碱性”或“中性”) 。
③已知钠离子的结构示意图为 ,则钠原子最外层电子数为_____________。
,则钠原子最外层电子数为_____________。
④若在实验里配制10升该营养液,需要称取的硫酸镁的质量是_____________亳克。