题目内容
(6分)如右图所示进行实验:S+02点燃S02。已知集气瓶的容积为150 mL.氧气的密度为1.4g/L,为了节约药品.理论上所取硫的质量不能超过多少克?(计算结果保留两位小数)


解:氧气的质量="(0.15" L 0.02 L) 1.4g/L=0.18g(2分)
1.4g/L=0.18g(2分)
设所取硫的质量最多为x。(与答题共l分)
S + 02 点燃 SO2
32 32
X 0.18g (1分)
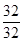 =
=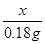 (1分) x="0.18" g (1分)
(1分) x="0.18" g (1分)
答:(略)。
 1.4g/L=0.18g(2分)
1.4g/L=0.18g(2分)设所取硫的质量最多为x。(与答题共l分)
S + 02 点燃 SO2
32 32
X 0.18g (1分)
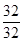 =
=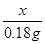 (1分) x="0.18" g (1分)
(1分) x="0.18" g (1分)答:(略)。
本题主要考查同学们利用化学方程式进行简单计算的掌握情况。正确找出已知量和待求量之间的数量关系是关键。
解:氧气的质量为(0.15L-0.02L)×1.4g/L=0.18g
设所取硫的质量为x。
S+O2 SO2
SO2
32 32
x 0.18g
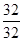 =
=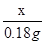 x=0.18g
x=0.18g
答:略。
解:氧气的质量为(0.15L-0.02L)×1.4g/L=0.18g
设所取硫的质量为x。
S+O2
 SO2
SO232 32
x 0.18g
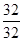 =
=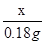 x=0.18g
x=0.18g答:略。

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
