题目内容
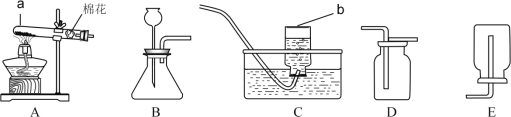
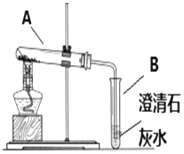
【题目】实验室选用如图所示装置制取气体,根据要求回答下列问题。
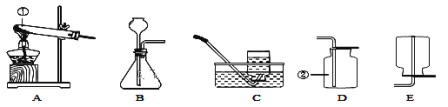
(1)指出图中标号仪器的名称①_________。
(2)实验室常用加热高锰酸钾的方法制取氧气,其反应的化学方程式为_____;实验结束时应先将导管移出水槽,再熄灭酒精灯,其目的是________。
(3)实验室制取二氧化碳的发生装置是_______(填序号),该反应的化学方程式为_________,用装置D收集二氧化碳气体,验满的方法是__________。
(4)实验室制取某气体时,既可用C也可用E装置收集,由此推测该气体所具有的物理性质是_____(填序号)。
A.该气体的密度大于空气 B.该气体难溶于水
C.该气体的密度小于空气
【答案】试管 2KMnO4 ![]() K2MnO4 + MnO2 + O2↑ 防止水倒流到试管中引起试管炸裂 B CaCO3+2HCl=CaCl2+CO2↑+H2O 将燃烧的木条放在集气瓶口,如果燃烧的木条熄灭,说明收集满了二氧化碳 BC
K2MnO4 + MnO2 + O2↑ 防止水倒流到试管中引起试管炸裂 B CaCO3+2HCl=CaCl2+CO2↑+H2O 将燃烧的木条放在集气瓶口,如果燃烧的木条熄灭,说明收集满了二氧化碳 BC
【解析】
(1)①是试管。
(2)加热高锰酸钾生成锰酸钾、二氧化锰、氧气;实验结束时应先将导管移出水槽,再熄灭酒精灯,其目的防止水倒流到试管中引起试管炸裂。
(3)固液常温反应制取气体选择发生装置B,实验室制取二氧化碳用石灰石与稀盐酸,它们发生反应生成氯化钙、水、二氧化碳。二氧化碳一般不支持燃烧,将燃烧的木条放在集气瓶口,如果燃烧的木条熄灭,说明收集满了二氧化碳。
(4)能用排水法收集气体,说明气体难溶于水,能用向下排空气法收集气体,说明气体的密度比空气的密度小,故选BC。

【题目】某中学化学兴趣小组按照课本实验方法,做木炭与氧化铜反应实验。请写出木炭与氧化铜反应化学方程式:______。实验时,同学们发现很难观察到紫红色铜的生成,却往往观察到有暗红色固体出现。请你参与探究木炭与氧化铜反应得到的暗红色固体的成分,完成下列各题:
已知信息:Ⅰ.木炭与氧化铜反应除生成铜外还可能生成氧化亚铜(Cu2O);
Ⅱ.Cu和Cu2O均为不溶于水的固体;
Ⅲ.Cu2O+H2SO4=CuSO4+Cu+H2O
提出问题:红色固体含有什么物质?
(1)猜想假设:猜想一:红色固体只含Cu;猜想二:红色固体只含Cu2O;猜想三:______(请补充完成猜想三)。
(2)实验探究:(填写表中空格)
实验操作 | 实验现象 | 实验结论 |
a.取少量红色固体加入到足量硫酸溶液中 | 无明显现象 | 假设 ______ 成立 |
b.取少量红色固体加入到足量硫酸溶液中 | ______ | 假设二和假设三均有可能成立 |
(3)试管B中看到的现象是:______,反应的化学方程式:______。
【题目】某兴趣小组在实验室中模拟高炉炼铁化学原理的实验,对固体产物成分等进行探究。
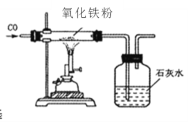
(设计实验)用一氧化碳还原氧化铁粉末,实验装置如图。
(进行实验)
(1)实验中观察到玻璃管中的现象是________________________,
洗气瓶中的现象是_________________________________________。
(2)该装置的不足之处是___________________________________
(3)该小组按上述实验设计,利用储气罐预先收集好一氧化碳,并进行实验。当看到固体颜色完全变了,停止实验,测得下列有关数据如下:
氧化铁质量 | 装置中玻璃管和固体的总质量 |
16g | 反应前67.9g |
反应后65.5g |
(分析与讨论)
小刚同学看到反应后玻璃管中全是黑色,认为反应后玻璃管中固体全部是铁,但小强同学提出了质疑,于是大家提出查阅资料。
[查阅资料]
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关。
②一氧化碳还原氧化铁的实验过程中固体产物可能是铁,也可能生成铁的氧化物,
如四氧化三铁、氧化亚铁等。
有关铁及其氧化物的性质如下:
物质性质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
颜色 | 黑色 | 黑色 | 红色 | 黑色 |
能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
[实验与猜想]
该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末部分被吸引,则该黑色固体粉末可能是_______________(填序号)。
①Fe ②FeO ③Fe3O4、Fe ④FeO、Fe ⑤FeO、Fe3O4 ⑥FeO、Fe3O4、Fe
(4)(实验结论)通过实验中获得的数据进行分析,要保证实验成功,将氧化物全部被还原成铁,储气罐的一氧化碳气体预先装入_____________克最合适。
A.4.8 B.5.6 C.8.4 D.9.6