网址:http://m.1010jiajiao.com/timu_id_92674[举报]
一、选择题(本题20分)每题只有一个正确答案,将其标号填在下表中。每题2分。
题号
1
2
3
4
5
6
7
8
9
10
答案
D
B
B
C
C
B
D
D
C
D
二、选择题(本题共10分)每题有1~2个正确答案,将其标号填在下表中。每题2分。正确答案只有一个选项的,多选不给分;正确答案包括两个选项的只选一个且正确给1分,一对一错不给分。
题号
11
12
13
14
15
答案
C
CD
BC
A
BC
三、(本大题共9小题 共21分)
16.(4分)每空1分。降低 吸水性 AgNO3溶液
17.(4分)每空1分。①CO2 ②HCl ③Ca(OH)2 ④CaCO3
18.(4分)每空1分。①CuSO4.5H2O ②C ③NaOH ④H2CO3
19.(1分)每空1分。①
20.(1分)每空1分。4:1:8
21.(4分)每空1分。 ①Fe(NO3)2 ②Ag ③Fe(NO3)2 Cu(NO3)2 AgNO3;Ag
22.(1分)每空1分。Ba2+ Cl- OH-
23.(1分)每空1分。③②①④;③②④①;答出一种即给1分。
24.(1分)每空1分。3:4
四、(本大题共4题 共14分)
25.(8分)每空1分。⑴ CaO+H2O====Ca(OH)2 CaCO3====CaO+CO2↑ Fe+CuSO4==FeSO4+Cu CuSO4+Ca(OH)2==Cu(OH)2↓+CaSO4
⑵① Ca(OH)2+Na2CO3==CaCO3↓+2NaOH ② MgCl2+2NaOH==Mg(OH)2↓+2NaCl
③ BaCO3+ H2SO4==BaSO4↓+H2O+CO2↑ ④ Zn+CuCl2 ==ZnCl2+Cu
26.(3分)每空1分。 HCl+AgNO3==AgCl↓+HNO3
H2SO4+Ba(NO3)2==BaSO4↓+2HNO3
2KOH + Cu(NO3)2==Cu(OH)2↓+2NaNO3
27.(3分)每空1分。⑴溶液由红色逐渐变为无色 ⑵挥发性 盐酸能跟碱发生中和反应
五、(本大题共2题 共12分)
28.(6分)每空1分。⑴CuSO4 ⑵BaCO3 BaSO4 ⑶Na2SO4 BaCl2 Na2CO3;Na2SO4 BaCl2 BaCO3;Na2SO4 BaCl2 Na2CO3 BaCO3;(每种可能性1分)
29.(6分)实验步骤和实验现象每空0.5分,化学方程式每个1分。
实验步骤
实验现象
化学方程式
稀盐酸
无色的气泡
Na2CO3+2HCl==2NaCl+H2O+CO2↑
BaCl2溶液
白色沉淀
Na2SO4+BaCl2==BaSO4↓+2NaCl
AgNO3溶液
白色沉淀
NaCl+AgNO3==AgCl↓+ NaNO3
六、(本大题共2题 共13分)
30.(6分)⑴题1分,其余每空1分。⑴丙戊甲已丁 ⑵ A ⑶ 甲中黑色物质变红乙中无水硫酸铜变蓝⑷ 甲中黑色物质变红丁中石灰水变浑浊⑸没有尾气的处理 在B导管处点燃
31.(7分)⑴每个物质1分,多答不给分 NaCl Na2SO4 ⑵每空一分,多答不给分Na2SO4 ;NaCl ;Ba(NO3)2, AgNO3;Na2SO4+Ba(NO3)2==BaSO4↓+2NaNO3
七、计算题(本大题共2题 共10分)
32.(4分)解:(1)设需用这种盐酸的质量为χ
χ=
(2)设可制得氢气的质量为У
Zn+2HCl==ZnCl2+H2↑
65 2
65 2
У=
答:可制得氢气
33.(6分)解:设25%的氢氧化钠溶液的质量为m
mg.25%
mg-
m=
设生成的硫酸钠溶液的质量为χ,生成的氢氧化铜沉淀的质量为У,硫酸铜溶液中溶质的质量为z
2NaOH + CuSO4== Na2SO4+ Cu(OH)2↓
80 160 142 98
80 160 142 98
χ=
У=
z=
硫酸铜溶液的质量为
硫酸铜溶液的溶质质量分数为
本资料由《七彩教育网》www.7caiedu.cn 提供!
①做细铁丝在氧气中燃烧的实验时,氧气的集气瓶底炸裂.
答:
②用试管加热水时 发现试管炸裂
答:

(1)上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法证明该装置不漏气.
答:
(2)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:
| ||
| ||
(3)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用:
A中加入的试剂是
B中加入的试剂是
C中加入的试剂是
D中加入的试剂是

(1)写出标号仪器的名称:a
(2)检查上图B装置气密性的方法是
(3)实验室用加热高锰酸钾制取氧气的化学方程式为
| ||
| ||
(4)实验室用5%的过氧化氢溶液和二氧化锰混合制取氧气,它的化学方程式为
| ||
| ||
(5)因为氧气的密度比空气
(1)北京奥运村的生活热水都是由太阳能热水利用系统提供.下列关于太阳能的说法中,正确的是
A.是化石燃料;B.取之不尽;C.可转化为热能、电能;D.是无污染能源
(2)为了确保“水立方”的水质达到国际泳联最新卫生标准,泳池的水将采用“砂滤-臭氧-活性炭”净水工艺,其中活性炭净水是利用它的

(3)北京奥运祥云火炬上端的外壁有430个通气孔(如右图所示)
这些孔不仅能把燃烧的废气排出去,还能
(4)在举重项目中,我国体育健儿取得娇人的成绩.举重运动员在抓杠铃前常擦一种白色粉末碳酸镁,碳酸镁的化学式是
(1)如果硫粉在氧气中燃烧,观察到的现象是
| ||
| ||
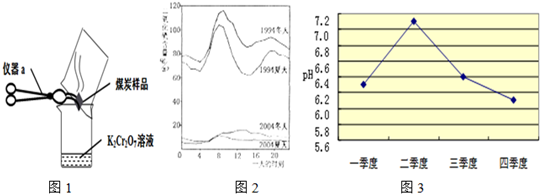
(2)几位同学为了探究木炭中是否含有少量硫元素,他们设计了如图1所示实验进行测定.请写出图中仪器a的名称:
 +H2O”.然而化学方程式中有一生成物不清楚,请根据已学知识推测其化学式:
+H2O”.然而化学方程式中有一生成物不清楚,请根据已学知识推测其化学式:(3)如图2是1994年和2004年某城市的一天各个时刻测到的空气中二氧化硫的含量.下列说法不正确的是
A.曲线显示冬天大气中的二氧化硫含量比夏天高
B.曲线显示了1994年一天中大约8点左右二氧化硫的含量较高
C.二氧化硫的含量在10年间降低的原因可能是加强了燃料的脱硫和控制了二氧化硫的排放
D.二氧化硫污染的主要来源是汽车排放的尾气,控制污染的方法是禁止使用汽车
(4)在研究酸雨危害的过程中,测定该地区雨水的pH的实验操作
某化学兴趣小组取刚降到地面的雨水,每隔一定时间用较精密的pH计测定其pH,数据如下:
| 测定时间/分钟 | 0 | 1 | 2 | 3 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 |
(5)酸雨造成的危害很多.某兴趣小组调查发现某市的石刻的表面有不同程度的腐蚀.且近20年的腐蚀速度大大超过以往,其中最主要原因之一就是酸雨.为了减缓石刻腐蚀,请你提一条建议:
酸雨还会使土壤酸化.为了中和酸性土壤,可以使用熟石灰粉末,若该酸雨的成分是硫酸,请写出该中和反应的化学方程式
(6)某校化学兴趣小组在学完碱的化学性质后,想到用NaOH溶液吸收SO2,反应化学方程式如下:2NaOH+SO2═Na2SO3+H2O 用NaOH溶液吸收1000L已除去CO2的空气样品,溶液质量增重了0.64g.已知此时空气的密度约为1.3g/L,求:
①被吸收的SO2的质量
②发生反应的NaOH的质量.(相对原子质量:Na-23 S-32 O-16)
③空气中SO2的质量分数(计算结果精确到0.01%).