网址:http://m.1010jiajiao.com/timu_id_92668[举报]
一、选择题(本题20分)每题只有一个正确答案,将其标号填在下表中。每题2分。
题号
1
2
3
4
5
6
7
8
9
10
答案
D
B
B
C
C
B
D
D
C
D
二、选择题(本题共10分)每题有1~2个正确答案,将其标号填在下表中。每题2分。正确答案只有一个选项的,多选不给分;正确答案包括两个选项的只选一个且正确给1分,一对一错不给分。
题号
11
12
13
14
15
答案
C
CD
BC
A
BC
三、(本大题共9小题 共21分)
16.(4分)每空1分。降低 吸水性 AgNO3溶液
17.(4分)每空1分。①CO2 ②HCl ③Ca(OH)2 ④CaCO3
18.(4分)每空1分。①CuSO4.5H2O ②C ③NaOH ④H2CO3
19.(1分)每空1分。①
20.(1分)每空1分。4:1:8
21.(4分)每空1分。 ①Fe(NO3)2 ②Ag ③Fe(NO3)2 Cu(NO3)2 AgNO3;Ag
22.(1分)每空1分。Ba2+ Cl- OH-
23.(1分)每空1分。③②①④;③②④①;答出一种即给1分。
24.(1分)每空1分。3:4
四、(本大题共4题 共14分)
25.(8分)每空1分。⑴ CaO+H2O====Ca(OH)2 CaCO3====CaO+CO2↑ Fe+CuSO4==FeSO4+Cu CuSO4+Ca(OH)2==Cu(OH)2↓+CaSO4
⑵① Ca(OH)2+Na2CO3==CaCO3↓+2NaOH ② MgCl2+2NaOH==Mg(OH)2↓+2NaCl
③ BaCO3+ H2SO4==BaSO4↓+H2O+CO2↑ ④ Zn+CuCl2 ==ZnCl2+Cu
26.(3分)每空1分。 HCl+AgNO3==AgCl↓+HNO3
H2SO4+Ba(NO3)2==BaSO4↓+2HNO3
2KOH + Cu(NO3)2==Cu(OH)2↓+2NaNO3
27.(3分)每空1分。⑴溶液由红色逐渐变为无色 ⑵挥发性 盐酸能跟碱发生中和反应
五、(本大题共2题 共12分)
28.(6分)每空1分。⑴CuSO4 ⑵BaCO3 BaSO4 ⑶Na2SO4 BaCl2 Na2CO3;Na2SO4 BaCl2 BaCO3;Na2SO4 BaCl2 Na2CO3 BaCO3;(每种可能性1分)
29.(6分)实验步骤和实验现象每空0.5分,化学方程式每个1分。
实验步骤
实验现象
化学方程式
稀盐酸
无色的气泡
Na2CO3+2HCl==2NaCl+H2O+CO2↑
BaCl2溶液
白色沉淀
Na2SO4+BaCl2==BaSO4↓+2NaCl
AgNO3溶液
白色沉淀
NaCl+AgNO3==AgCl↓+ NaNO3
六、(本大题共2题 共13分)
30.(6分)⑴题1分,其余每空1分。⑴丙戊甲已丁 ⑵ A ⑶ 甲中黑色物质变红乙中无水硫酸铜变蓝⑷ 甲中黑色物质变红丁中石灰水变浑浊⑸没有尾气的处理 在B导管处点燃
31.(7分)⑴每个物质1分,多答不给分 NaCl Na2SO4 ⑵每空一分,多答不给分Na2SO4 ;NaCl ;Ba(NO3)2, AgNO3;Na2SO4+Ba(NO3)2==BaSO4↓+2NaNO3
七、计算题(本大题共2题 共10分)
32.(4分)解:(1)设需用这种盐酸的质量为χ
χ=
(2)设可制得氢气的质量为У
Zn+2HCl==ZnCl2+H2↑
65 2
65 2
У=
答:可制得氢气
33.(6分)解:设25%的氢氧化钠溶液的质量为m
mg.25%
mg-
m=
设生成的硫酸钠溶液的质量为χ,生成的氢氧化铜沉淀的质量为У,硫酸铜溶液中溶质的质量为z
2NaOH + CuSO4== Na2SO4+ Cu(OH)2↓
80 160 142 98
80 160 142 98
χ=
У=
z=
硫酸铜溶液的质量为
硫酸铜溶液的溶质质量分数为
本资料由《七彩教育网》www.7caiedu.cn 提供!
| A.只有①和② | B.只有②和③ | C.只有①和③ | D.①②③ |
某同学检验一瓶NaOH溶液是否变质,设计了下列三种检验方法:①加少量饱和石灰水,有沉淀生成,则氢氧化钠溶液已变质 ②加少量稀盐酸,有气泡产生,则氢氧化钠溶液已变质 ③加少量Ba(OH)2溶液,有沉淀生成,则氢氧化钠溶液已变质.其中方法和结论都正确的是
- A.只有①和②
- B.只有②和③
- C.只有①和③
- D.①②③
[问题情景]某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时,有较多的气泡放出.这一现象激发起同学们的探究欲望,生成的是什么气体呢?
[提出猜想]从物质组成元素的角度分析,放出的气体可能是SO2、O2、H2.
[查阅资料]SO2易溶于水,它能与NaOH溶液反应,生成Na2SO3和H2O.浓硫酸是干燥剂,能吸水.
[方案设计]依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O2,则检验方法是
(2)乙同学认为是SO2,则只需将放出的气体通入盛有NaOH溶液的洗气瓶中,称量通气前后洗气瓶的质量.写出SO2与NaOH反应的化学方程式:
(3)实验小组同学合作设计了如图1组合实验方案,排除和验证猜想的气体.
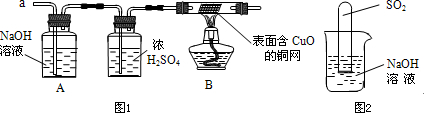
如果放出的是O2和H2的混合物,你认为方案中的安全隐患是
丙同学认为:为确保安全,实验前应先收集一试管气体,用拇指
[实验探究]经丙同学确认安全后,小组同学首先对装置A进行称量,再将收集到的气体从a通入,过一会儿点燃B处酒精灯;一段时间后,发现表面含CuO的铜网由黑色变为光亮的红色;停止通气,再次称量装置A,发现质量不变.
结论:(4)铁粉与硫酸铜溶液反应时,产生的气体是
(5)写出H2还原CuO的化学方程式:
| ||
| ||
[思维拓展]
(6)不通过称量,如何判断SO2与NaOH溶液发生了反应呢?有一同学设计了如图2所示的装置进行实验,发现试管内液面上升,就得出SO2与NaOH溶液发生反应的结论.其他同学认为这一方案不严谨,理由是