摘要:反应④ CH2=CHOOCH + H2O CH3CHO + HCOOH
网址:http://m.1010jiajiao.com/timu_id_91681[举报]
(2013?闵行区一模)已知有机物A是一种重要的有机化工基础原料,过氧乙酸( )是一种强氧化剂.以下是以有机物A为原料合成己内酯的路线示意图:
)是一种强氧化剂.以下是以有机物A为原料合成己内酯的路线示意图:
2A
CH2=CH-C≡CH
CH2=CH-CH=CH2
B
 →
→

完成下列填空:
(1)A的电子式为
 ,反应②的反应类型是
,反应②的反应类型是
(2)B的结构简式为
 .
.
(3)己内酯有多种异构体,写出能同时满足下列要求的物质结构简式
 .
.
①能发生银镜反应;②能发生水解反应;③能使溴的四氯化碳溶液褪色;④分子结构中有三个甲基.
(4)写出由CH2=CH-C≡CH合成氯丁橡胶( )的有关化学反应方程式.
)的有关化学反应方程式.
查看习题详情和答案>>
 )是一种强氧化剂.以下是以有机物A为原料合成己内酯的路线示意图:
)是一种强氧化剂.以下是以有机物A为原料合成己内酯的路线示意图:2A
| 催化剂 |
| 反应① |
| 乙烯 |
| △ |
| H2O |
| 催化剂 |
 →
→
完成下列填空:
(1)A的电子式为


氧化反应
氧化反应
.(2)B的结构简式为


(3)己内酯有多种异构体,写出能同时满足下列要求的物质结构简式


①能发生银镜反应;②能发生水解反应;③能使溴的四氯化碳溶液褪色;④分子结构中有三个甲基.
(4)写出由CH2=CH-C≡CH合成氯丁橡胶(
 )的有关化学反应方程式.
)的有关化学反应方程式.下列各表述与示意图一致的是 ( )

A.图①中a、b曲线分别表示反应CH2=CH?2(g)+H2(g)——CH3CH(g)+Q使用和未使用催化剂时,反应过程中的能量变化
B.图②表示25℃时,用0.1mol·L-1盐酸滴定20mL 0.1mol·L-1NaOH溶液,溶液的pH随加入酸体积的变化
C.图③表示锌料与过量稀盐酸反应时,V(H2)随时间的变化图
D.图④中曲线表示反应2SO2(g)+O2(g)2SO3(g)+Q正、逆反应的平衡常数K随温度的变化
2005年全世界石油价格居高不下,其主要原因是随着社会生产的发展,人口增多,对能源的需求量逐年增加,全球石油储量下降.寻求和制备代号称“黑金”的新能源已经成为紧迫任务,化学工作者正在研究以天然气和醇类合成优质汽油的方法.
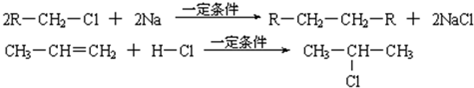
已知:
(1)凡与醛基直接相连的碳原子上的氢称为α一H原子,在稀碱溶液的催化作用下,一个醛分子上的α一H原子连接到另一个醛分子的氧原子上,其余部分连接到羰基碳原子上生成羟基醛,如:

(2)
(3)合成路线如下:
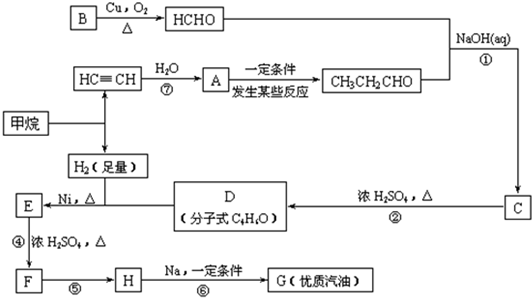
(1)写出D的结构简式
(2)在反应②~⑦中,属于加成反应的是
(3)写出下列反应方程式
E→F:
H→G:
(4)H也能与NaOH水溶液反应,其反应方程式为
 ,生成的有机物能否在Cu或Ag作催化剂的条件下被空气氧化
,生成的有机物能否在Cu或Ag作催化剂的条件下被空气氧化
查看习题详情和答案>>
已知:
(1)凡与醛基直接相连的碳原子上的氢称为α一H原子,在稀碱溶液的催化作用下,一个醛分子上的α一H原子连接到另一个醛分子的氧原子上,其余部分连接到羰基碳原子上生成羟基醛,如:

(2)

(3)合成路线如下:

(1)写出D的结构简式
CH2=CH(CH3)CHO
CH2=CH(CH3)CHO
(2)在反应②~⑦中,属于加成反应的是
③⑤⑦
③⑤⑦
,属于消去反应的是②④
②④
.(3)写出下列反应方程式
E→F:
CH3CH(CH3)CH2OH
CH3CH=(CH3)CH2+H2O
| 浓硫酸 |
| △ |
CH3CH(CH3)CH2OH
CH3CH=(CH3)CH2+H2O
;| 浓硫酸 |
| △ |
H→G:
2(CH3)3CCl+2Na
(CH3)3CC(CH3)3+2NaCl
| 一定条件 |
2(CH3)3CCl+2Na
(CH3)3CC(CH3)3+2NaCl
.| 一定条件 |
(4)H也能与NaOH水溶液反应,其反应方程式为


否
否
(选填“能”或“否”). 随着石油资源的日趋紧张,天然气资源的转化利用越来越受到人们的关注.如图所示是最近研发出的天然气利用新途径:首先,甲烷在催化剂作用下发生“氧氯化反应”生成一氯甲烷;然后,一氯甲烷在400℃的条件下通过分子筛催化转化为低碳烯烃.
随着石油资源的日趋紧张,天然气资源的转化利用越来越受到人们的关注.如图所示是最近研发出的天然气利用新途径:首先,甲烷在催化剂作用下发生“氧氯化反应”生成一氯甲烷;然后,一氯甲烷在400℃的条件下通过分子筛催化转化为低碳烯烃.请根据以上信息回答下列问题:
(1)第一轮次反应投料时甲烷和氯化氢的最佳体积比为
l:1
l:1
.(2)由一氯甲烷生成丙烯的化学方程式为
3CH3Cl
CH2=CH-CH3+3HCl
| 分子筛 |
3CH3Cl
CH2=CH-CH3+3HCl
.| 分子筛 |
(3)若该途径中的第一步“甲烷氧氯化反应”的转化率为80%,经除水、分离出混合物中的一氯甲烷后,剩余物质全部留用并投入第二轮次生产;第二步反应生成含有乙烯、丙烯、丁烯的混合气体,碳原子的利用率为90%,分离出其中的烯烃气体后剩余物质全部留用并投入第二轮次生产.则:
①标准状况下,1m3甲烷经过一轮反应可得到
0.45
0.45
kg乙烯、丙烯、丁烯的混合气体.②第二轮次反应投料时,需补充的甲烷、氧气和HCl的体积比为
10:5:1
10:5:1
.