摘要:图中操作①.②都要用到玻璃棒.其中操作①玻璃棒的作用是 ,从操作③的现象分析.溶液D中含有的物质是 ,写出溶液D与Na2CO3溶液反应的化学方程式 .反应类型为 .
网址:http://m.1010jiajiao.com/timu_id_912262[举报]
 (2011?兰州)正确的实验操作对实验结果很重要.在实验课上,老师要求同学们配制10%的氢氧化钠溶液50.0g.
(2011?兰州)正确的实验操作对实验结果很重要.在实验课上,老师要求同学们配制10%的氢氧化钠溶液50.0g.(1)甲同学正确计算出需要固体氢氧化钠的质量为
5.0
5.0
g.(2)乙同学在溶解步骤中用到的玻璃仪器除烧杯外,还用到了仪器
玻璃棒
玻璃棒
.(3)丙同学按如图所示的操作称量氢氧化钠固体,请指出图中的错误:
①
砝码和NaOH固体放反了
砝码和NaOH固体放反了
;②
NaOH固体不能直接放在托盘天平的托盘上称量
NaOH固体不能直接放在托盘天平的托盘上称量
.(4)若其他操作步骤都正确,丙同学按上图所示进行实验,最后得到的氢氧化钠溶液的溶质质量分数
小于
小于
10%(填“大于”、“小于”或“等于”). 实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样。已知它是无色液体,是初中化学常用的试剂。小强和小华同学很感兴趣,决定对其成分进行探究:
实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样。已知它是无色液体,是初中化学常用的试剂。小强和小华同学很感兴趣,决定对其成分进行探究:
提出问题:这瓶试剂可能是什么溶液呢?
交流讨论:根据受损标签的情况判断,这瓶试剂不可能是
A.酸 B.碱 C.盐
查阅资料:Ⅰ.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3 。
Ⅱ.Na2CO3和NaHCO3溶液都呈碱性。
Ⅲ.测定室温(20℃)时,四种物质的溶解度的数据如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
得出结论:小华根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,这瓶试剂不可能是 。
设计实验并继续探究:
(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,这瓶试剂不可能是 。
(2)小强为了确定该溶液是哪种溶液,他又进行了如下实验:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加 | 产生大量的气泡 | 该溶液是 |
拓展与应用:确定该溶液还可以选择与小强不同的试剂,你选择的试剂是 (要求类别不同)。
钢铁是人类生活和生产中非常重要的材料。
(3)工业炼铁的反应过程如下图所示,其中焦炭 的作用是燃烧提供能量和 。
的作用是燃烧提供能量和 。

(4)在工业冶炼中要得到224t,理论上需要含Fe2O380%,的赤铁矿石的质量是多少?
查看习题详情和答案>>(2005?济南)海水的综合利用可以制备金属镁,其流程如图所示(图中A、B、C均表示主要成分):

请填写下列空白:
(1)C的化学式为
(2)写出A→B的化学反应方程式
(3)整个过程中没有涉及到的基本反应类型是
(4)若在实验室进行粗盐提纯,溶解、过滤、蒸发(结晶)三步操作中都要用到的玻璃仪器是
查看习题详情和答案>>

请填写下列空白:
(1)C的化学式为
Mg(OH)2
Mg(OH)2
.(2)写出A→B的化学反应方程式
CaO+H2O=Ca(OH)2
CaO+H2O=Ca(OH)2
.(3)整个过程中没有涉及到的基本反应类型是
置换反应
置换反应
.(4)若在实验室进行粗盐提纯,溶解、过滤、蒸发(结晶)三步操作中都要用到的玻璃仪器是
玻璃棒
玻璃棒
.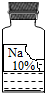 (2013?鹤壁二模)实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:
(2013?鹤壁二模)实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:提出问题:这瓶试剂可能是什么溶液呢?
交流讨论:根据受损标签的情况判断,这瓶试剂不可能是
A
A
A.酸 B.碱 C.盐
查阅资料:
Ⅰ.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3.
Ⅱ.Na2CO3和NaHCO3溶液都呈碱性.
Ⅲ.测定室温(20℃)时,四种物质的溶解度的数据如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
NaHCO3
NaHCO3
.设计实验并继续探究:
(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,这瓶试剂不可能是
NaCl
NaCl
.(2)小强为了确定该溶液是哪种溶液,他又进行了如下实验:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加 盐酸 盐酸 |
产生大量的气泡 | 该溶液是 Na2CO3 Na2CO3 |
Ca(OH)2
Ca(OH)2
(要求类别不同).钢铁是人类生活和生产中非常重要的材料.(3)工业炼铁的反应过程如下图所示,其中焦炭的作用是燃烧提供能量和
制取CO
制取CO
.
(4)在工业冶炼中要得到224t铁,理论上需要含Fe2O380%的赤铁矿石的质量是多少?
(1)若用氯酸钾和二氧化锰来制取氧气,该反应的化学方程式为 ,其中二氧化锰在化学反应前后固体混合物中的质量分数将 .(填“变大”、“变小”或“不变”)
(2)待固体完全反应后通过以下四步实验操作回收二氧化锰.正确操作的先后顺序是 (填写选项序号).
a.烘干 b.溶解 c.洗涤 d. 过滤
(3)过滤、蒸发时都需用到的仪器是 (填序号).
A.酒精灯 B.烧杯 C.玻璃棒 D.漏斗 E.量筒
(4)小丽想要用回收的氯化钾配制50g 10%的氯化钾溶液.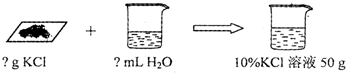
配制该溶液的操作步骤
①计算:需要氯化钾固体的质量为 g,水 mL(水的密度近似看作1g/cm3)
②称量:用托盘天平称取所需固体,再用 mL的量筒量取所需的水;
③溶解:将称得的氯化钾固体放入烧杯中,再倒入量取的水,用玻璃棒充分搅拌;
④装瓶:将配制的溶液倒入试剂瓶,并贴上标签.请在装有所配制溶液的试剂瓶(见图)标签上标明相应信息.
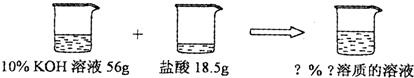
(5)如图所示,已知一定质量分数、一定质量的氢氧化钾溶液与一定质量的盐酸恰好完全反应.求算反应后溶液的溶质质量分数.
 查看习题详情和答案>>
查看习题详情和答案>>
(2)待固体完全反应后通过以下四步实验操作回收二氧化锰.正确操作的先后顺序是
a.烘干 b.溶解 c.洗涤 d. 过滤
(3)过滤、蒸发时都需用到的仪器是
A.酒精灯 B.烧杯 C.玻璃棒 D.漏斗 E.量筒
(4)小丽想要用回收的氯化钾配制50g 10%的氯化钾溶液.

配制该溶液的操作步骤
①计算:需要氯化钾固体的质量为

②称量:用托盘天平称取所需固体,再用
③溶解:将称得的氯化钾固体放入烧杯中,再倒入量取的水,用玻璃棒充分搅拌;
④装瓶:将配制的溶液倒入试剂瓶,并贴上标签.请在装有所配制溶液的试剂瓶(见图)标签上标明相应信息.
(5)如图所示,已知一定质量分数、一定质量的氢氧化钾溶液与一定质量的盐酸恰好完全反应.求算反应后溶液的溶质质量分数.
 查看习题详情和答案>>
查看习题详情和答案>>
