摘要:(1)除去二氧化碳和水蒸气:用氢氧化钠溶液吸收二氧化碳生成碳酸钠和水.用浓硫酸吸收水蒸气.请写出氢氧化钠和二氧化碳反应的文字表达式.并注明各物质的化学式. (2)除去氧气:他们分别收集一瓶气体用下图装置进行除去氧气的燃烧实验,其中甲同学选用红磷,乙同学选用木炭.你认为选用 的方法不科学.原因是 .
网址:http://m.1010jiajiao.com/timu_id_909907[举报]
除去氮气中混有的少量氢气、二氧化碳、水蒸气,可能采用的方法如下:①通过浓硫酸;②通过灼热的氧化铜粉末;③通过氢氧化钠溶液;④通过浓盐酸,采用的方法和操作顺序均正确的是
[ ]
A.①②③
B.③②①
C.②③④
D.④①③
查看习题详情和答案>>
B.③②①
C.②③④
D.④①③
过氧化钠是一种黄色固体,化学式为Na2O2,化学兴趣小组的同学将包有过氧化钠固体的棉花放入如图1所示的烧杯中,缓慢倒入二氧化碳气体后,发现位于下面的蜡烛先熄灭,上面的后熄灭,同时发现棉花燃烧起来.
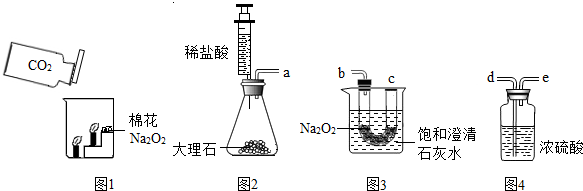
(1)实验中:位于下面的蜡烛先熄灭,上面的后熄灭,这一现象说明二氧化碳具有
(2)棉花为什么会燃烧呢?小组同学联想起物质燃烧的相关知识,推理出烧杯里的棉花要燃烧,除了满足“棉花是可燃物”这一条件,还需要满足的条件是
提出问题:在实验中是如何给棉花燃烧提供上述条件的呢?
查阅资料:在常温下Na2O2和CO2能发生化学反应.
设计实验:讨论后,小组同学利用如图2、3、4所示的实验装置进行探究.要使Na2O2和CO2反应,实验装置中导管口正确的链接顺序是a→
实验步骤:①按以上顺序装好装置,并检查其气密性,添加药品;②推动注射器,并将稀盐酸注入锥形瓶中;③一段时间后,在c处放置一根带火星的小木条,观察现象.
实验现象:带火星的小木条复燃且饱和澄清石灰水变浑浊.
实验分析:
①浓硫酸的作用是
②烧杯内变浑浊的原因是
实验结论:
①“小木条复燃”说明了Na2O2和CO2反应产生了
②“饱和的澄清石灰水变浑浊”说明Na2O2和CO2反应
查看习题详情和答案>>

(1)实验中:位于下面的蜡烛先熄灭,上面的后熄灭,这一现象说明二氧化碳具有
密度大于空气密度
密度大于空气密度
物理性质.(2)棉花为什么会燃烧呢?小组同学联想起物质燃烧的相关知识,推理出烧杯里的棉花要燃烧,除了满足“棉花是可燃物”这一条件,还需要满足的条件是
氧气和温度达到棉花的着火点
氧气和温度达到棉花的着火点
.提出问题:在实验中是如何给棉花燃烧提供上述条件的呢?
查阅资料:在常温下Na2O2和CO2能发生化学反应.
设计实验:讨论后,小组同学利用如图2、3、4所示的实验装置进行探究.要使Na2O2和CO2反应,实验装置中导管口正确的链接顺序是a→
d
d
→e
e
→b→c.实验步骤:①按以上顺序装好装置,并检查其气密性,添加药品;②推动注射器,并将稀盐酸注入锥形瓶中;③一段时间后,在c处放置一根带火星的小木条,观察现象.
实验现象:带火星的小木条复燃且饱和澄清石灰水变浑浊.
实验分析:
①浓硫酸的作用是
除去CO2中的水蒸气
除去CO2中的水蒸气
.②烧杯内变浑浊的原因是
温度升高,氢氧化钙的溶解度减小,溶质析出
温度升高,氢氧化钙的溶解度减小,溶质析出
.实验结论:
①“小木条复燃”说明了Na2O2和CO2反应产生了
氧气
氧气
;②“饱和的澄清石灰水变浑浊”说明Na2O2和CO2反应
放出
放出
(填“吸收”或“放出”)热量,使棉花满足了燃烧条件.水煤气是将水蒸气通过灼热的焦炭而生成的气体,主要成分是一氧化碳、氢气及少量
的二氧化碳和水蒸气.某课题组同学为验证水煤气的成分,做了以下准备:
(一)资料收集:①H2+CuO
Cu+H2O ②CO+CuO
Cu+CO2 ③无水硫酸铜遇水由白色变为蓝色
(二)设计实验装置
请分析上面信息后回答:
①你认为验证水煤气中各成分的顺序依次是
A.H2O、CO2、H2、CO B.H2O、CO、H2、CO
C.CO、H2O、H2、CO2 D.CO、H2、CO、H2O
②装置C的目的是
③实验中两次用到装置B,前一次的目的是
④实验中两次用到装置A,后一次的作用是
⑤装置E内观察到的现象是
查看习题详情和答案>>
的二氧化碳和水蒸气.某课题组同学为验证水煤气的成分,做了以下准备:

(一)资料收集:①H2+CuO
| ||
| ||
(二)设计实验装置
请分析上面信息后回答:
①你认为验证水煤气中各成分的顺序依次是
A
A
(选填序号);A.H2O、CO2、H2、CO B.H2O、CO、H2、CO
C.CO、H2O、H2、CO2 D.CO、H2、CO、H2O
②装置C的目的是
除去水煤气中的二氧化碳
除去水煤气中的二氧化碳
,装置D的作用是除去水煤气中的水蒸气
除去水煤气中的水蒸气
;③实验中两次用到装置B,前一次的目的是
验证水煤气中二氧化碳的存在
验证水煤气中二氧化碳的存在
;④实验中两次用到装置A,后一次的作用是
检验水煤气中是否含有氢气
检验水煤气中是否含有氢气
.⑤装置E内观察到的现象是
黑色的氧化铜变成红色
黑色的氧化铜变成红色
.过氧化钠(Na2O2)是一种淡黄色粉末,可作为潜水艇或呼吸面具有供氧剂.人呼出气体的主要成分有氮氧、氧气、二氧化碳和水蒸气,二氧化碳和水能分别与Na2O2反应生成氧气.为了探究Na2O2在潜水艇中反应后的物质,明明同学设计了如图1所示模拟实验.

【猜想与假设】
(1)明明猜想生成的固体物质是:(Ⅰ)氢氧化钠(Ⅱ)碳酸钠(Ⅲ)氢氧化钠和碳酸钠.
【实验与验证】
明明通过以下实验探究来验证他的猜想:
①取少量反应后干燥管中的固体样品,置于试管中,向其中加入______,发现有气泡产生,该气体通入澄清石灰水,石灰水变浑浊,证明猜想(Ⅰ)不成立.
②已知碳酸钠的水溶液呈碱性.请根据部分物质的溶解性表(20℃)所提供的信息,将明明的探究过程填写完整.
于是明明得出结论:猜想(Ⅱ)不成立,猜想(Ⅲ)成立.
【反思与评价】
(2)你认为Na2O2与______填(“二氧化碳”或“水”)反应生成了碳酸钠.在上述实验装置中再增加一个装置,重复步骤①即可证明你的判断,请指出应增加装置的名称和位置.
【拓展与延伸】
(3)另取少量反应后干燥管中的固体样品,配制成溶液,向其中逐滴滴加稀盐酸,产生气体的质量与加入稀盐酸的质量的关系如图2所示.
①请解释开始滴加盐酸时没有产生气体的原因.
②计算该样品中碳酸钠的质量.
查看习题详情和答案>>

【猜想与假设】
(1)明明猜想生成的固体物质是:(Ⅰ)氢氧化钠(Ⅱ)碳酸钠(Ⅲ)氢氧化钠和碳酸钠.
【实验与验证】
明明通过以下实验探究来验证他的猜想:
①取少量反应后干燥管中的固体样品,置于试管中,向其中加入______,发现有气泡产生,该气体通入澄清石灰水,石灰水变浑浊,证明猜想(Ⅰ)不成立.
②已知碳酸钠的水溶液呈碱性.请根据部分物质的溶解性表(20℃)所提供的信息,将明明的探究过程填写完整.
| 实验目的 | 实验操作 | 现象或测定结果 | 结论或化学方程式 |
| 除去碳酸钠 | 取少量该固体样品溶于水配成溶液,滴加适量的______溶液,充分反应后过滤 | 有白色沉淀生成 | 有关反应的化学方程式为______ |
| 检验是否含有氢氧化钠 | 用PH试纸测定反应后溶液的酸碱度,操作方法是______ | pH>7 | 该样品中含有氢氧化钠 |
【反思与评价】
(2)你认为Na2O2与______填(“二氧化碳”或“水”)反应生成了碳酸钠.在上述实验装置中再增加一个装置,重复步骤①即可证明你的判断,请指出应增加装置的名称和位置.
【拓展与延伸】
(3)另取少量反应后干燥管中的固体样品,配制成溶液,向其中逐滴滴加稀盐酸,产生气体的质量与加入稀盐酸的质量的关系如图2所示.
①请解释开始滴加盐酸时没有产生气体的原因.
②计算该样品中碳酸钠的质量.
25、过氧化钠(Na2O2)是一种浅黄色固体.某次科技活动中,某化学兴趣小组的同学将包有Na2O2固体的棉花放入烧杯中(图1),缓慢倒入CO2后发现下面的蜡烛先熄灭,上面的后熄灭,同时也惊奇的发现棉花燃烧起来了.
Ⅰ.实验过程中“下面的蜡烛先熄灭,上面的后熄灭”的现象说明二氧化碳具有
Ⅱ.棉花为什么会燃烧呢?小组同学联想起物质燃烧的相关知识,推理出棉花要燃烧,除了满足“棉花是可燃物”这一条件外,还需满足另外两个条件是
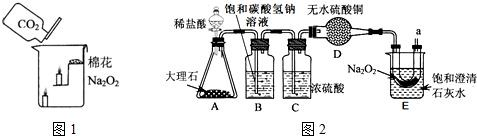
[提出问题]在实验中是如何给棉花燃烧提供上述条件的呢?
查阅资料:在常温下Na2O2和CO2、Na2O2和H2O均能发生化学反应.无水硫酸铜遇水由白色变成蓝色.
设计实验:经过讨论后,小组同学设计了图2的实验进行探究.
[实验步骤]
①按图2装配好装置,并检查其气密性;
②相关的试剂放入对应的仪器中;
③打开分液漏斗的活塞,把稀盐酸缓缓滴入锥形瓶内,并固定活塞位置;
④一段时间后,观察E中现象,再在a处放置一根带火星的小木条,观察现象.
[实验分析和结论](1)B装置的作用是
C装置的作用是
(2)E装置的烧杯内“饱和的澄清石灰水变浑浊”说明Na2O2和CO2反应中
(3)“小木条复燃”说明了Na2O2和CO2反应产生了
查看习题详情和答案>>
Ⅰ.实验过程中“下面的蜡烛先熄灭,上面的后熄灭”的现象说明二氧化碳具有
不助燃也不可燃
的性质.Ⅱ.棉花为什么会燃烧呢?小组同学联想起物质燃烧的相关知识,推理出棉花要燃烧,除了满足“棉花是可燃物”这一条件外,还需满足另外两个条件是
密度大于空气
、与氧气接触达到着火点
.
[提出问题]在实验中是如何给棉花燃烧提供上述条件的呢?
查阅资料:在常温下Na2O2和CO2、Na2O2和H2O均能发生化学反应.无水硫酸铜遇水由白色变成蓝色.
设计实验:经过讨论后,小组同学设计了图2的实验进行探究.
[实验步骤]
①按图2装配好装置,并检查其气密性;
②相关的试剂放入对应的仪器中;
③打开分液漏斗的活塞,把稀盐酸缓缓滴入锥形瓶内,并固定活塞位置;
④一段时间后,观察E中现象,再在a处放置一根带火星的小木条,观察现象.
[实验分析和结论](1)B装置的作用是
除去HCl
.C装置的作用是
除去中的水蒸气
;D装置的作用是
检验水蒸气是否除尽
.(2)E装置的烧杯内“饱和的澄清石灰水变浑浊”说明Na2O2和CO2反应中
放热
(填“吸收”或“放出”)热量,使氢氧化钙
溶解度减小
而析出.(3)“小木条复燃”说明了Na2O2和CO2反应产生了
氧气
,使棉花满足了燃烧条件.