摘要:乙方案: ①分别用上述两种方案制取80g硫酸铜.甲方案参加反应的硫酸的质量为98g.请计算乙方案中参加反应的硫酸的质量为多少?②通过对比这两种实验方案及计算结果.你认为选用哪种方案更好? ,请说明你的理由 .(5)通过对上述实验的对比与分析可知.探究某一化学问题时.除了应根据具体情况考虑恰当的实验装置外.还应考虑 等因素.
网址:http://m.1010jiajiao.com/timu_id_907692[举报]
(2013?苏州一模)实验室常用(a)~(e)装置制取和收集气体.

步骤一:选取药品与发生装置.实验室经常选用稀盐酸和
反应物,发生装置可选用如上图中的
步骤二:检查装置气密性.组装好仪器后,将导管末端浸末在水中,用手捂试管,
发现导管口
步骤三:反应并收集气体.收集二氧化碳可以用排水法或向上排空气法.到底哪种方法更好,甲、乙两同学分别用排水法和排空气法做如下实验研究(用的药品与发生装置一样)
A.甲收集到的二氧化碳纯度更高 B.产生气体速度不一样
C.气态分子间隔大,运动速度快,不同气体分子更易混合,不易分离
结论:综上所述,
反思:排水法收集二氧化碳仍有不足之处,请写出一点
[思考]丙同学对发生装置中的废液进行了研究.
(1)测出该废液的pH<7,则废液中存在的阳离子为
(2)向此废液滴加碳酸钠溶液至过量,则下列图象表示正确的为

(3)小明是一位爱动手做实验的同学,他找来塑料瓶和一些其他用品,制作成如图(f)的装置.图中去底塑料瓶和其相连导管的组合相当于实验室中的
查看习题详情和答案>>

步骤一:选取药品与发生装置.实验室经常选用稀盐酸和
大理石或石灰石
大理石或石灰石
(填药品名称)作为反应物,发生装置可选用如上图中的
b或f
b或f
.步骤二:检查装置气密性.组装好仪器后,将导管末端浸末在水中,用手捂试管,
发现导管口
有气泡
有气泡
,放手后有导管中有一小段水柱
导管中有一小段水柱
,则气密性良好.步骤三:反应并收集气体.收集二氧化碳可以用排水法或向上排空气法.到底哪种方法更好,甲、乙两同学分别用排水法和排空气法做如下实验研究(用的药品与发生装置一样)
| 1、比较收集时间:分别收集满一个集气瓶的二氧化碳,记录时间 | 甲:收集时间较短 乙:收集时间较长 |
原因: C C (选择填空,下同 ) |
| 2、比较收集到气体的浓度:分别向两个集气瓶中加入两滴管的澄清石灰水 | 甲:石灰水先变浑浊 乙:石灰水后变浑浊 |
原因: A A |
C.气态分子间隔大,运动速度快,不同气体分子更易混合,不易分离
结论:综上所述,
排水法
排水法
(填收集方法)收集二氧化碳更好.反思:排水法收集二氧化碳仍有不足之处,请写出一点
混有少量水蒸气或得不到干燥的二氧化碳(答案合理均可)
混有少量水蒸气或得不到干燥的二氧化碳(答案合理均可)
[思考]丙同学对发生装置中的废液进行了研究.
(1)测出该废液的pH<7,则废液中存在的阳离子为
Ca2+、H+
Ca2+、H+
.(2)向此废液滴加碳酸钠溶液至过量,则下列图象表示正确的为
B
B
.
(3)小明是一位爱动手做实验的同学,他找来塑料瓶和一些其他用品,制作成如图(f)的装置.图中去底塑料瓶和其相连导管的组合相当于实验室中的
长颈漏斗
长颈漏斗
(填一种仪器的名称).该装置作为制取二氧化碳气体发生装置的优点是可随时添加药品、可控制反应的开始和结束(答案合理均可)
可随时添加药品、可控制反应的开始和结束(答案合理均可)
.实验与探究--探究岩石的成分
春天到了.周日,小明与同学们一起去爬山,在山上采集了三种岩石样本.当地的农民伯伯说,三种岩石分别是花岗岩、大理石和石灰石.
探究一:岩石样本中是否都含有碳酸钙?
(1)请你设计实验方案进行探究,完成下列探究报告:
探究二:大理石和石灰石哪种样本中碳酸钙的含量高?
(2)构想假说:你对哪种样本中碳酸钙的含量高,构建的假说是
(3)设计实验:请用下列装置,设计实验,验证你的假说
(Ⅰ)指出上述装置中标示出的仪器名称:①
(Ⅱ)实验时,将A和B装置进行连接,思考:B装置广口瓶上方要放一定量植物油的原因是
(Ⅲ)你认为实验中必须控制的变量是
(4)获得结论:若用大理石和石灰石样本分别进行实验时,进入量筒中水的体积分别为40mL和38mL,则两种样本中碳酸钙含量较高的为
(5)交流反思:甲乙两同学对实验步骤产生了争议.在连接好仪器检查装置气密性后,甲同学认为:可直接加入样本和试剂,测量产生气体的量.乙同学认为:应先拆开各装置,在A装置中加入样本和试剂,在仪器②中的空气全部排净后,再连接好装置测量产生气体的量.你认为甲乙两同学的做法正确的是

查看习题详情和答案>>
春天到了.周日,小明与同学们一起去爬山,在山上采集了三种岩石样本.当地的农民伯伯说,三种岩石分别是花岗岩、大理石和石灰石.
探究一:岩石样本中是否都含有碳酸钙?
(1)请你设计实验方案进行探究,完成下列探究报告:
| 实验步骤 | 应得到的实验现象 | 结论与解释 |
取岩石样本,分别加入稀盐酸 取岩石样本,分别加入稀盐酸 |
大理石和石灰石样本中有气泡产生;花岗岩本样无现象 大理石和石灰石样本中有气泡产生;花岗岩本样无现象 |
大理石和石灰石样本中含有碳酸钙,发生反应的方程式为 CaCO3+2HCl═CaCl2+H2O+CO2↑ CaCO3+2HCl═CaCl2+H2O+CO2↑ 花岗岩本样中不含碳酸钙. |
(2)构想假说:你对哪种样本中碳酸钙的含量高,构建的假说是
大理石样本中碳酸钙的含量高
大理石样本中碳酸钙的含量高
(3)设计实验:请用下列装置,设计实验,验证你的假说
大理石样本中碳酸钙的含量高
大理石样本中碳酸钙的含量高
.(Ⅰ)指出上述装置中标示出的仪器名称:①
分液漏斗
分液漏斗
②锥形瓶
锥形瓶
(Ⅱ)实验时,将A和B装置进行连接,思考:B装置广口瓶上方要放一定量植物油的原因是
防止二氧化碳溶于水
防止二氧化碳溶于水
(Ⅲ)你认为实验中必须控制的变量是
稀盐酸的浓度,样本的颗粒大小
稀盐酸的浓度,样本的颗粒大小
(4)获得结论:若用大理石和石灰石样本分别进行实验时,进入量筒中水的体积分别为40mL和38mL,则两种样本中碳酸钙含量较高的为
大理石
大理石
(5)交流反思:甲乙两同学对实验步骤产生了争议.在连接好仪器检查装置气密性后,甲同学认为:可直接加入样本和试剂,测量产生气体的量.乙同学认为:应先拆开各装置,在A装置中加入样本和试剂,在仪器②中的空气全部排净后,再连接好装置测量产生气体的量.你认为甲乙两同学的做法正确的是
乙
乙
(填甲或乙)
某企业是一家以生产电缆类产品为主的地方明星企业。在电缆生产过程中,不可避免地会产生一定量的含铜废料(如:零碎电缆)。某化学兴趣小组的同学得知这一情况后,提出可以用含铜废料制备胆矾(CuSO4·5H2O)。
I、硫酸铜的制备
方案1:甲同学根据已学知识,提出了制备硫酸铜方案:

方案2:乙同学根据查阅资料找到了一种工业制备硫酸铜的流程:

(1)上述方案中的①、②、③三处,与铜或铜的化合物有关的化学反应方程式分别是:
①_________; ②__________; ③_________________;
(2)从环保角度对两套方案的不同部分进行比较,你认为方案________________(填1或2)更合理。理由是:__________________。
(3)方案2中,加入H2O2后要求温度控制在50℃到60℃加热的原因为______________
(4)若上述方案所用的稀硫酸溶质质量分数为36.8%,问每1L98%的浓硫酸(密度为1.84g/mL)能配制出这种稀硫酸______________g,需水___________________ L(水的密度为1.0g/mL)。在实验室中稀释浓硫酸时,是如何操作的:________________。
(5)兴趣小组同学一致指出,将滤液经蒸发、降温结晶等操作后,用少量95%的酒精淋洗后晾干,得硫酸铜晶体。晶体采用酒精淋洗的优点是 _______________。
II、硫酸铜晶体(CuSO4·xH2O)中结晶水(xH2O)含量的测定
在老师的指导下,学习小组取12.5g硫酸铜晶体(CuSO4·xH2O)进行热分解,获得相关数据,并绘制成固体质量一温度的关系如图。
I、硫酸铜的制备
方案1:甲同学根据已学知识,提出了制备硫酸铜方案:

方案2:乙同学根据查阅资料找到了一种工业制备硫酸铜的流程:

(1)上述方案中的①、②、③三处,与铜或铜的化合物有关的化学反应方程式分别是:
①_________; ②__________; ③_________________;
(2)从环保角度对两套方案的不同部分进行比较,你认为方案________________(填1或2)更合理。理由是:__________________。
(3)方案2中,加入H2O2后要求温度控制在50℃到60℃加热的原因为______________
(4)若上述方案所用的稀硫酸溶质质量分数为36.8%,问每1L98%的浓硫酸(密度为1.84g/mL)能配制出这种稀硫酸______________g,需水___________________ L(水的密度为1.0g/mL)。在实验室中稀释浓硫酸时,是如何操作的:________________。
(5)兴趣小组同学一致指出,将滤液经蒸发、降温结晶等操作后,用少量95%的酒精淋洗后晾干,得硫酸铜晶体。晶体采用酒精淋洗的优点是 _______________。
II、硫酸铜晶体(CuSO4·xH2O)中结晶水(xH2O)含量的测定
在老师的指导下,学习小组取12.5g硫酸铜晶体(CuSO4·xH2O)进行热分解,获得相关数据,并绘制成固体质量一温度的关系如图。

(1)在加热过程中,随着水分的失去,固体颜色将由蓝色逐渐变为____________色,最终变为黑色;
(2)650℃以上时,硫酸铜固体就会发生分解,生成黑色金属氧化物、二氧化硫及氧气,此反应的化学方程式为____________ ;
(3)根据图中数据,计算CuSO4·xH2O中x的值为_____________。(请写出计算过程)
(4)若将4.0g剩余固体继续加热到更高的温度,发现固体质量减少了0.4g后质量不再改变,写出此过程中可能发生反应的化学方程式:_____________。
Ⅲ、硫酸铜的应用波尔多液是用硫酸铜和石灰乳配成的一种天蓝色、粘稠的悬浊液,其有效成分是Cu4(OH)6SO4,其中铜元素的化合价为________________。碱式盐可以写成盐和碱的形式,例如碱式碳酸铜可以写成CuCO3·Cu(OH)2,则Cu4(OH)6SO4可以写成盐和碱的形式为______________,其杀菌机理可看作是Cu2+使病原菌失去活性,这说明病原菌的主体是__________________(填一种有机物名称)。
查看习题详情和答案>>
(2)650℃以上时,硫酸铜固体就会发生分解,生成黑色金属氧化物、二氧化硫及氧气,此反应的化学方程式为____________ ;
(3)根据图中数据,计算CuSO4·xH2O中x的值为_____________。(请写出计算过程)
(4)若将4.0g剩余固体继续加热到更高的温度,发现固体质量减少了0.4g后质量不再改变,写出此过程中可能发生反应的化学方程式:_____________。
Ⅲ、硫酸铜的应用波尔多液是用硫酸铜和石灰乳配成的一种天蓝色、粘稠的悬浊液,其有效成分是Cu4(OH)6SO4,其中铜元素的化合价为________________。碱式盐可以写成盐和碱的形式,例如碱式碳酸铜可以写成CuCO3·Cu(OH)2,则Cu4(OH)6SO4可以写成盐和碱的形式为______________,其杀菌机理可看作是Cu2+使病原菌失去活性,这说明病原菌的主体是__________________(填一种有机物名称)。
 某企业是一家以生产电缆类产品为主的地方明星企业.在电缆生产过程中,不可避免地会产生一定量的含铜废料(如:零碎电缆).某化学兴趣小组的同学得知这一情况后,提出可以用含铜废料制备胆矾(CuSO4?5H2O).
某企业是一家以生产电缆类产品为主的地方明星企业.在电缆生产过程中,不可避免地会产生一定量的含铜废料(如:零碎电缆).某化学兴趣小组的同学得知这一情况后,提出可以用含铜废料制备胆矾(CuSO4?5H2O).Ⅰ、硫酸铜的制备
方案1:甲同学根据已学知识,提出了制备硫酸铜方案:

方案2:乙同学根据查阅资料找到了一种工业制备硫酸铜的流程:

(1)上述方案中的①、②、③三处,与铜或铜的化合物有关的化学反应方程式分别是:
①
(2)从环保角度对两套方案的不同部分进行比较,你认为方案
(3)方案2中,加入H2O2后要求温度控制在50℃到60℃加热的原因为
(4)若上述方案所用的稀硫酸溶质质量分数为36.8%,问每1L98%的浓硫酸(密度为1.84g/mL)能配制出这种稀硫酸
(5)兴趣小组同学一致指出,将滤液经蒸发、降温结晶等操作后,用少量95%的酒精淋洗后晾干,得硫酸铜晶体.晶体采用酒精淋洗的优点是
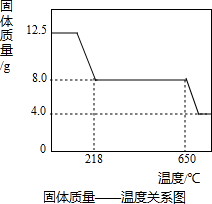
Ⅱ、硫酸铜晶体(CuSO4?xH2O)中结晶水(xH2O)含量的测定:在老师的指导下,学习小组取12.5g硫酸铜晶体(CuSO4?xH2O)进行热分解,获得相关数据,并绘制成固体质量-温度的关系如下图.
(1)在加热过程中,随着水分的失去,固体颜色将由蓝色逐渐变为
(2)650℃以上时,硫酸铜固体就会发生分解,生成黑色金属氧化物、二氧化硫及氧气,此反应的化学方程式为
(3)根据图中数据,计算CuSO4?xH2O中x的值为
(4)若将4.0g剩余固体继续加热到更高的温度,发现固体质量减少了0.4g后质量不再改变,写出此过程中可能发生反应的化学方程式:
Ⅲ、硫酸铜的应用
波尔多液是用硫酸铜和石灰乳配成的一种天蓝色、粘稠的悬浊液,其有效成分是Cu4(OH)6SO4,其中铜元素的化合价为
