摘要:40.下表是核电荷数为3-18的元素原子的核外电子排布示意图:
网址:http://m.1010jiajiao.com/timu_id_906611[举报]
下表是核电荷数为3~18的元素原子的核外电子排布示意图.

若将氢、氦也排入上表,已知氦元素原子的核外电子排布为![]() ,可得到以下两种形式:
,可得到以下两种形式:

你同意________种排列方式,针对氦元素说明你选择的理由________.
核电荷数为1~18的元素的原子结构示意图如图,回答下列问题:
(1)表中不同元素最本质的区别是 .
(2)在第三周期中,各原子结构的共同之处是 ,该周期中,各原子核外电子排布地变化规律是 .
(3)在第三周期中,元素类型的变化情况是:从左到右由 元素过渡到 元素,并以稀有气体元素结尾.
(4)核电荷数为12的元素失去两个电子后,形成的粒子的符号是 ,它的核外电子排布与
元素的原子核外电子排布相同.
查看习题详情和答案>>
(1)表中不同元素最本质的区别是
(2)在第三周期中,各原子结构的共同之处是
(3)在第三周期中,元素类型的变化情况是:从左到右由
(4)核电荷数为12的元素失去两个电子后,形成的粒子的符号是
元素的原子核外电子排布相同.
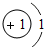 |
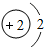 | ||||||
| 氢(H) | 氦(He) | ||||||
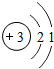 |
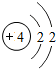 |
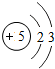 |
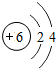 |
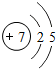 |
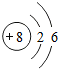 |
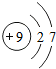 |
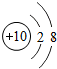 |
| 锂( Li) | 铍(Be) | 硼(B) | 碳(C) | 氮(N) | 氧(O) | 氟(F) | 氖(Ne) |
 |
 |
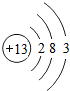 |
 |
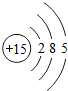 |
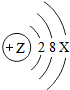 |
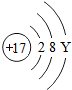 |
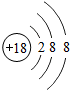 |
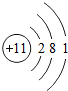
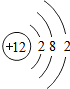
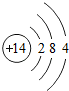
| 钠(Na) | 镁(Mg) | 铝(Al) | 硅(Si) | 磷(P) | 硫(S) | 氯(Cl) | 氩(Ar) |
核电荷数为1~18的元素的原子结构示意图等信息如下,回答下列问题:

(1)在第三周期中,各原子结构的共同之处是______;该周期中,各原子核外电子排布的变化规律是______.
(2)在第三周期中,元素类型的变化情况是:从左到右由______元素过渡到______元素,并以稀有气体元素结尾.
(3)写出核外电子排布与氖原子相同的阳离子和阴离子符号各一个:阳离子______,阴离子______.
(4)写出含有氮元素的常见单质、氧化物的化学式各一个:
(5)在元素周期表中,同一族(纵行)的元素具有相似的化学性质.则下列各组元素具有相似化学性质的是______(填序号).
A.C和NeB.Be和MgC.Al和SiD.F和Cl
(6)第11号元素与第17号元素组成的化合物是______(写化学式),构成该物质的微粒是______(选填“分子”、“原子”或“离子”).
查看习题详情和答案>>

(1)在第三周期中,各原子结构的共同之处是______;该周期中,各原子核外电子排布的变化规律是______.
(2)在第三周期中,元素类型的变化情况是:从左到右由______元素过渡到______元素,并以稀有气体元素结尾.
(3)写出核外电子排布与氖原子相同的阳离子和阴离子符号各一个:阳离子______,阴离子______.
(4)写出含有氮元素的常见单质、氧化物的化学式各一个:
| 物质的类别 | 单质 | 氧化物 |
| 物质的化学式 |
A.C和NeB.Be和MgC.Al和SiD.F和Cl
(6)第11号元素与第17号元素组成的化合物是______(写化学式),构成该物质的微粒是______(选填“分子”、“原子”或“离子”).
有人将核电荷数为1~18的元素排成了如下形式,请你分析表中各元素的原子结构后,将得出的结论填写在横线上:
(1)原子序数为17的元素名称是
(2)我发现如下规律:
①原子序数与元素原子核电荷数在数值上相等:
②
③
④
查看习题详情和答案>>
| 最外层电子数 电子层数 |
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 一 | H | He | ||||||
| 二 | Li | Be | B | C | N | O | F | Ne |
| 三 | Na | Mg | Al | Si | P | S | Cl | Ar |
氯
氯
,在化学反应中,该元素的原子容易得
得
填(“得”或“失”)电子;原子序数为13的元素属于金属
金属
元素(填:“金属”或“非金属”)(2)我发现如下规律:
①原子序数与元素原子核电荷数在数值上相等:
②
同周期元素原子的电子层数相同
同周期元素原子的电子层数相同
③
同周期元素原子的电子层数相同
同周期元素原子的电子层数相同
④
随着核电荷数的递增,元素原子最外层电子的排布呈现周期性的变化
随着核电荷数的递增,元素原子最外层电子的排布呈现周期性的变化
.