摘要:C.Fe2O3Fe (OH)3 D.Na2CO3NaOH
网址:http://m.1010jiajiao.com/timu_id_903273[举报]
某兴趣小组的同学为分析一种石灰石样品中碳酸钙的质量分数,取20g样品放入烧杯,把60g稀盐酸分三次加入烧杯,使其充分反应(样品中所含杂质既不溶于水也不与稀盐酸反应),实验流程及数据如下(所有实验数据都不包括烧杯的质量,且不考虑
H2O和HCl的挥发;操作X包括搅拌、过滤、洗涤、干燥、称量):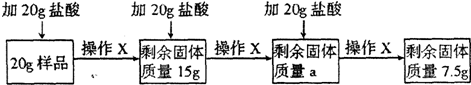
请回答:
(1)CaCO3中Ca与C的质量比为
(2)实验时判断已充分反应的现象是
(3)第三次反应过滤后所得溶液的pH
A.CaO B.CaCO3 C.Ca(OH)2 D.CaCl2
(4)计算所用稀盐酸中溶质的质量分数(写出计算过程)
查看习题详情和答案>>
H2O和HCl的挥发;操作X包括搅拌、过滤、洗涤、干燥、称量):

请回答:
(1)CaCO3中Ca与C的质量比为
10:3
10:3
;(2)实验时判断已充分反应的现象是
不再产生气泡
不再产生气泡
:其中a为10
10
g;样品中碳酸钙的质量分数为62.5%
62.5%
;(3)第三次反应过滤后所得溶液的pH
<
<
7(填“>”、“<”或“=”);为使该溶液显中性且得到尽可能多的CaCl2,最后可向烧杯中加入过量的B
B
(填序号)A.CaO B.CaCO3 C.Ca(OH)2 D.CaCl2
(4)计算所用稀盐酸中溶质的质量分数(写出计算过程)
 32、A、B、C、D、E、X、Y、Z都是初中化学中常见的物质,其中A为氧化物,它们具有如图所示的相互转化关系:试用化学式回答:
32、A、B、C、D、E、X、Y、Z都是初中化学中常见的物质,其中A为氧化物,它们具有如图所示的相互转化关系:试用化学式回答: