摘要:A.CuCu(OH)2 B.ZnAg
网址:http://m.1010jiajiao.com/timu_id_903272[举报]
氯碱厂电解饱和食盐水溶液制取NaOH的工艺流程示意图如下:
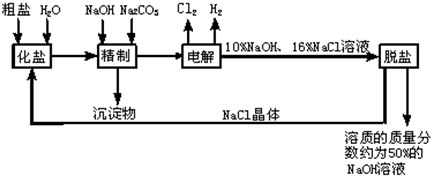
依据图,完成下列填空:
(1)粗盐中含有的较多的可溶性杂质(氯化镁、氯化钙、硫酸钠等)和
(2)工业食盐含有较多杂质,精制过程中加NaOH的作用是
(3)在电解过程中,发生反应的化学方程式为
(4)粗盐中硫酸钠含量较高,必须添加钡试剂除去硫酸根离子,该钡试剂可以是
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(5)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH反应,Cl2和NaOH溶液充分接触,产物是NaClO和氯化钠和水,请写出Cl2和NaOH溶液反应的化学方程式
查看习题详情和答案>>

依据图,完成下列填空:
(1)粗盐中含有的较多的可溶性杂质(氯化镁、氯化钙、硫酸钠等)和
不溶性杂质
不溶性杂质
.(2)工业食盐含有较多杂质,精制过程中加NaOH的作用是
除去氯化镁杂质
除去氯化镁杂质
.(3)在电解过程中,发生反应的化学方程式为
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
,电解后溶液的pH
| ||
升高
升高
.(填“升高”、“不变”、“降低”)(4)粗盐中硫酸钠含量较高,必须添加钡试剂除去硫酸根离子,该钡试剂可以是
A、C
A、C
.A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(5)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH反应,Cl2和NaOH溶液充分接触,产物是NaClO和氯化钠和水,请写出Cl2和NaOH溶液反应的化学方程式
2NaOH+Cl2═NaClO+NaCl+H2O
2NaOH+Cl2═NaClO+NaCl+H2O
.
氯碱厂电解饱和食盐水溶液制取NaOH的工艺流程示意图如图:
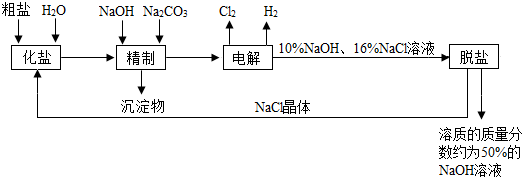
依据图,完成下列填空:
(1)粗盐中含有的较多的可溶性杂质(氯化镁、氯化钙、硫酸钠等)和 ,请用适当的数字和符号填空
②2个氯分子 ③粗盐中含有的一种阳离子
④零价的氢元素 ⑤硫酸钠
(2)工业食盐含有较多杂质,精制过程中加NaOH的作用是 .
(3)在电解过程中,发生反应的化学方程式为 ,
电解后溶液的pH .(填“升高”、“不变”、“降低”)
(4)粗盐中硫酸钠含量较高,必须添加钡试剂除去硫酸根离子,该钡试剂可以是 .
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(5)为了有效地除去氯化镁、氯化钙、硫酸钠,加入试剂的合理顺序为 .
A.先加入NaOH,后加入Na2CO3,再加入钡试剂
B.先加入NaOH,后加入钡试剂,再加入Na2CO3
C.先加入钡试剂,后加入NaOH,再加入Na2CO3
D.先加入钡试剂,后加入Na2CO3,再加入NaOH
(6)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过 (填写操作名称)、冷却、过滤除去NaCl.
(7)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH反应,Cl2和NaOH溶液充分接触,产物是NaClO和氯化钠和水,请写出Cl2和NaOH溶液反应的化学方程式 .
查看习题详情和答案>>

依据图,完成下列填空:
(1)粗盐中含有的较多的可溶性杂质(氯化镁、氯化钙、硫酸钠等)和
②2个氯分子
④零价的氢元素
(2)工业食盐含有较多杂质,精制过程中加NaOH的作用是
(3)在电解过程中,发生反应的化学方程式为
电解后溶液的pH
(4)粗盐中硫酸钠含量较高,必须添加钡试剂除去硫酸根离子,该钡试剂可以是
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(5)为了有效地除去氯化镁、氯化钙、硫酸钠,加入试剂的合理顺序为
A.先加入NaOH,后加入Na2CO3,再加入钡试剂
B.先加入NaOH,后加入钡试剂,再加入Na2CO3
C.先加入钡试剂,后加入NaOH,再加入Na2CO3
D.先加入钡试剂,后加入Na2CO3,再加入NaOH
(6)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过
(7)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH反应,Cl2和NaOH溶液充分接触,产物是NaClO和氯化钠和水,请写出Cl2和NaOH溶液反应的化学方程式
 如图所示,锥形瓶中盛有气体X,胶头滴管中盛有液体Y.若挤压胶头滴管使液体滴入瓶中,振荡一段时间后可见小气球a膨胀鼓起.下列各组X、Y物质不会出现上述现象的是( ) 如图所示,锥形瓶中盛有气体X,胶头滴管中盛有液体Y.若挤压胶头滴管使液体滴入瓶中,振荡一段时间后可见小气球a膨胀鼓起.下列各组X、Y物质不会出现上述现象的是( )
|
查看习题详情和答案>>
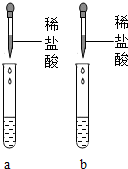 (2012?泉州模拟)在初三化学实验复习课上,老师提供了三瓶无色溶液,其中一瓶是稀盐酸,另外两瓶没有贴标签,分别是碳酸钠溶液和氢氧化钠溶液.
(2012?泉州模拟)在初三化学实验复习课上,老师提供了三瓶无色溶液,其中一瓶是稀盐酸,另外两瓶没有贴标签,分别是碳酸钠溶液和氢氧化钠溶液.复习内容一:鉴别两瓶没有贴标签无色溶液
同学们设计了实验方案,分别取样于试管a、b两支试管中,再进行如图所示的实验操作.
(1)观察有1支试管中有
气泡
气泡
产生,证明该溶液是碳酸钠溶液.(2)写出试管a或b中发生反应的化学方程式:
Na2CO3+2HCl=2NaCl+H2O+CO2↑
Na2CO3+2HCl=2NaCl+H2O+CO2↑
(写一个即可).实验结束后,老师要求同学们把鉴别后所得的溶液倒入盛回收液的A烧杯或B烧杯中.复习内容二:探究回收液中,影响溶液酸碱性的溶质成分
(3)小明同学取少量A烧杯的回收液,滴入紫色石蕊试液,石蕊试液变红,从而证明A烧杯的回收液呈
酸
酸
性.根据实验结果,你认为A烧杯的回收液中必含有的溶质是HCl、NaCl
HCl、NaCl
.(4)小影同学用玻璃棒蘸取B烧杯中的回收液滴在 pH试纸上,测得pH=9,证明B烧杯中的回收液呈
碱
碱
性.根据实验结果,小影猜想B烧杯回收液中可能含有的溶质是:①氢氧化钠;②碳酸钠;③氢氧化钠和碳酸钠.【查阅资料】CaCl2溶液呈中性,可与碳酸钠溶液发生如下反应:Na2CO3+CaCl2=2NaCl+CaCO3↓
【查阅资料】
| 实验步骤 | 实验现象 | 实验结论 |
| Ⅰ.取少量B烧杯中的回收液于试管中,滴入饱和氢氧化钙溶液. | 产生白色沉淀 | B烧杯中的回收液中含有 碳酸钠 碳酸钠 |
| Ⅱ.①另取少量B烧杯中的回收液于试管中,滴入足量的 CaCl2 CaCl2 溶液.②过滤,往滤液中滴加 酚酞试液 酚酞试液 |
①产生白色沉淀. ② 酚酞变红色(或无变化) 酚酞变红色(或无变化) |
B烧杯中的回收液中 有氢氧化钠(或没有氢氧化钠) 有氢氧化钠(或没有氢氧化钠) |
③(或②)
③(或②)
是正确的.【能力提升】
(6)老师把A、B两烧杯中的回收液混合在一起,并测得混合液的pH=4,要求同学们选择下列其中一种试剂,通过加入过量的该试剂,以调节废液的pH=7,你认为他们应选择
C
C
(填标号).A.Ca(OH)2 B.CaO C.CaCO3 D.H2SO4.
(2013?高淳县二模)氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:

依据上图,完成下列填空:
(1)电解时发生的主要化学方程式
(2)工业食盐含Ca2+、Mg2+等杂质,加入NaOH、Na2CO3的目的就是为了除去这些杂质,但如果精制时发现其中SO42-含量也较高,必须添加含钡离子的试剂(简称钡试剂)除去SO42-,该试剂可以是
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(3)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(4)NaOH和NaCl的溶解度如下表所示:
脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过
(5)电解时,若与电源正、负极相连的两极区域没有分隔,电解产物就变为了NaClO和H2,相应的化学方程式为
查看习题详情和答案>>

依据上图,完成下列填空:
(1)电解时发生的主要化学方程式
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
;
| ||
(2)工业食盐含Ca2+、Mg2+等杂质,加入NaOH、Na2CO3的目的就是为了除去这些杂质,但如果精制时发现其中SO42-含量也较高,必须添加含钡离子的试剂(简称钡试剂)除去SO42-,该试剂可以是
ac
ac
(选填:a、b、c).a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(3)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为
bc
bc
(选填:a、b、c);a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(4)NaOH和NaCl的溶解度如下表所示:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| NaCl溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39.0 | 39.8 |
| NaOH溶解度/g | 42 | 51 | 109 | 119 | 129 | 145 | 174 | 299 | 314 | 329 | 347 |
蒸发结晶
蒸发结晶
(填操作名称)、冷却等操作除去大部分NaCl.(5)电解时,若与电源正、负极相连的两极区域没有分隔,电解产物就变为了NaClO和H2,相应的化学方程式为
NaCl+H2O
NaClO+H2↑
| ||
NaCl+H2O
NaClO+H2↑
.
| ||