摘要:7g(1)Na2CO3溶解度曲线为 (2)欲使接近饱和的Na2CO3溶液变饱和.可采用的方法是 (3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O= 2NaHCO3,根据以上信息.向20℃饱和NaHCO3溶液中通入足量CO2气体.可观察到的现象是 .
网址:http://m.1010jiajiao.com/timu_id_903167[举报]
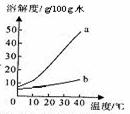
以下是Na2CO3,NaHCO3的溶解度表及溶解度曲线。根据图表回答下列问题:

| 10 | 20 | 30 | 40 | |
|
| 12.5g | 21.5g | 39.7g | 49.0g |
|
| 8.1g | 9.6g | 11.1g | 12.7g |
(1)Na2CO3溶解度曲线为 (填a或b)
(2)欲使接近饱和的Na2CO3溶液变饱和,可采用的方法是 (只写一种)
(3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O= 2NaHCO3,根据以上信息,向20℃饱和NaHCO3溶液中通入足量CO2气体,可观察到的现象是 。
查看习题详情和答案>>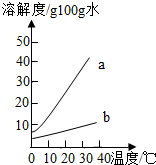 以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.
以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.(1)Na2CO3溶解度曲线为
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3的溶解度(g/100g水) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3的溶解度(g/100g水) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
Ⅰ.冷却结晶Ⅱ.蒸发结晶Ⅲ.溶解过滤
(3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是
(4)40℃时的100.0g Na2CO3的饱和溶液中含有
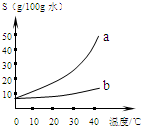 以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.
以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.(1)Na2CO3溶解度曲线为
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3的溶解度(g/100g水) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3的溶解度(g/100g水) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
①冷却热饱和溶液 ②蒸发溶剂 ③溶解过滤
(3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是
(4)40℃时的100g Na2CO3的饱和溶液中含有
(5)若将30%的碳酸钠溶液100g,稀释到10%,需要加水
以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.
(1)Na2CO3溶解度曲线为 (填a或b).
(2)要除去NaHCO3固体中的少量Na2CO3,应采用的物理方法是 (填写编号).
Ⅰ.冷却结晶Ⅱ.蒸发结晶Ⅲ.溶解过滤
(3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是 .
(4)40℃时的100.0g Na2CO3的饱和溶液中含有 g溶质,该溶液的溶质质量分数为 ,配制该溶液需要 石碱和 mL水.(计算结果精确到0.1)
 查看习题详情和答案>>
查看习题详情和答案>>
(1)Na2CO3溶解度曲线为 (填a或b).
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3的溶解度(g/100g水) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3的溶解度(g/100g水) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
Ⅰ.冷却结晶Ⅱ.蒸发结晶Ⅲ.溶解过滤
(3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是 .
(4)40℃时的100.0g Na2CO3的饱和溶液中含有 g溶质,该溶液的溶质质量分数为 ,配制该溶液需要 石碱和 mL水.(计算结果精确到0.1)
 查看习题详情和答案>>
查看习题详情和答案>>
以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线。
(1)Na2CO3溶解度曲线为 (填a或b)。
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3的溶解度(g/100g水) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3的溶解度(g/100g水) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
(2)要除去NaHCO3固体中的少量Na2CO3,应采用的物理方法是 (填写编号)。
Ⅰ. 冷却结晶 Ⅱ. 蒸发结晶 Ⅲ. 溶解过滤
(3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是 。
(4)40℃时的100.0g Na2CO3的饱和溶液中含有 g溶质,该溶液的溶质质量分数为 %,配制该溶液需要 g石碱和 mL水。(计算结果精确到0.1)