网址:http://m.1010jiajiao.com/timu_id_902305[举报]
草酸晶体(H2C2O4? 2 H2O )熔点较低,加热会熔化、气化和分解。草酸(H2C2O4)受热会分解,它与氢氧化钙的反应为H2C2O4 + Ca ( OH )2=== CaC2O4(白色)+ 2H2O。甲、乙两同学对草酸受热分解的产物作如下探究:
(l)猜想与假设:
第一种:草酸分解生成CO2和H2 ,第二种:草酸分解生成CO2、CO 和H2O;
第三种:草酸分解:H2C2O2![]() CO2↑+H2O(未配平)
CO2↑+H2O(未配平)
有同学从理论上就可判断第三种假设不成立,老师也认为这一判断是正确的,该同学判断的理论依据是
(2)设计与实验:
甲、乙两同学分别设计了下图所示的A 、B 两套实验装置(图中铁架台略去).

① 甲同学按A 装置实验,观察到澄清石灰水变浑浊,认为此现象是由草酸晶体受热分解产生的CO2所导致,此判断 (填“严密”或“不严密”) .
② B装置图方框内的仪器未画完整,请你帮他画完整。
乙同学按B装置实验,看到无水硫酸铜由白变蓝,洗气瓶中溶液变浑浊,在尖嘴管口点燃剩余气体,火焰上方罩一个 烧杯,有白色固体生成,证明产物中有 ;换一干、冷的烧杯罩在火焰上方,内壁无现象,证明产物中无H2。
(3)结论与思考:
①草酸受热分解的化学方程式为:
②若省略B装置方框内的仪器,整套装置也能证明产物中有CO2(假设每步反应均完全),方法是:
查看习题详情和答案>>(1)加热分解草酸晶体最适宜的装置是
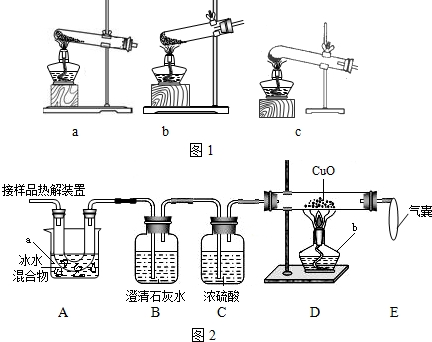
(2)图2是验证热分解产物中含CO,CO2的装置
①仪器a和b的名称分别是
②证明存在CO2的现象是
| ||
| ||
③装置A的作用是
(3)为测定样品中草酸晶体的质量分数,设计两种如下方案.
| 熔点 | 沸点 | 热稳定性 | 与碱反应 |
| 101°C~102°C | 150°C~160°C升华 | 100.1°C失去结晶水,175°C分解成CO2,CO,H2O | 与Ca(OH)2反应产生白色沉淀(CaC2O4) |
②称取8.75g草酸晶体样品配制50.00g溶液,取10.00g溶液加适量的稀硫酸,然后滴加25.00g3.16%KMnO4溶液,恰好反应完全.
(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)则KMnO4溶液显
【资料1】草酸晶体(H2C2O4?3H2O)在浓硫酸作用下受热分解,化学方程式为:
H2C2O4?3H2O
| 浓硫酸 |
| △ |
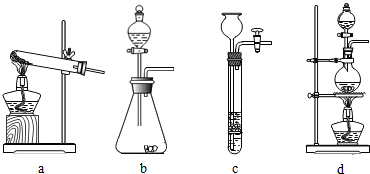
(1)下列可用作草酸分解制取气体的装置是
【问题讨论】用下图所示装置进行实验:
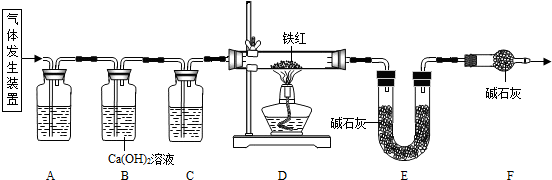
(2)实验前应先
(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是
a.浓硫酸 b.澄清石灰水 c.氢氧化钠溶液
(4)B装置的作用是
(5)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:①加热前
(6)写出D装置中所发生反应的一个化学方程式
| ||
| ||
【数据分析与计算】
【资料2】铁的常见氧化物中铁的质量分数:
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
①D中充分反应后得到Fe粉的质量为mg,则
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是
【实验反思】
反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会
反思2:请指出【问题讨论】中实验装置的一个明显缺陷
某研究小组欲检验草酸晶体样品分解产物并测定器质量分数(假设杂质不参与反应).草酸晶体(H2C2O4•2H2O)的理化性质见表.
(1)加热分解草酸晶体最适宜的装置是 (填图1字母序号).

(2)图2是验证热分解产物中含CO,CO2的装置
①仪器a和b的名称分别是 和 .
②证明存在CO2的现象是 ,证明存在CO的现象是 ,D中反应的化学方程式是 .
③装置A的作用是 ,气囊的作用是 .
(3)为测定样品中草酸晶体的质量分数,设计两种如下方案.
|
熔点 |
沸点 |
热稳定性 |
与碱反应 |
|
101°C~102°C |
150°C~160°C升华 |
100.1°C失去结晶水,175°C分解成CO2,CO,H2O |
与Ca(OH)2反应产生白色沉淀(CaC2O4) |
①称一定量样品用上图装置进行实验,测得装置D反应前后的质量差,由此计算出的实验结果比实际值偏低,排除仪器和操作的因素,其原因可能有:CO未完全反应、 .
②称取8.75g草酸晶体样品配制50.00g溶液,取10.00g溶液加适量的稀硫酸,然后滴加25.00g3.16%KMnO4溶液,恰好反应完全.
(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)则KMnO4溶液显 色,25.00g3.16%KMnO4溶液中KMnO4的质量 g.请计算样品中的质量分数.[写出计算过程,M2(H2C2O4)=90,M2(H2C2O4•2H2O)=126,M2(KMnO4)=158].
查看习题详情和答案>>
某研究小组欲检验草酸晶体样品分解产物并测定器质量分数(假设杂质不参与反应).草酸晶体(H2C2O4•2H2O)的理化性质见表.
(1)加热分解草酸晶体最适宜的装置是 (填图1字母序号).

(2)图2是验证热分解产物中含CO,CO2的装置
①仪器a和b的名称分别是 和 .
②证明存在CO2的现象是 ,证明存在CO的现象是 ,D中反应的化学方程式是 .
③装置A的作用是 ,气囊的作用是 .
(3)为测定样品中草酸晶体的质量分数,设计两种如下方案.
|
熔点 |
沸点 |
热稳定性 |
与碱反应 |
|
101°C~102°C |
150°C~160°C升华 |
100.1°C失去结晶水,175°C分解成CO2,CO,H2O |
与Ca(OH)2反应产生白色沉淀(CaC2O4) |
①称一定量样品用上图装置进行实验,测得装置D反应前后的质量差,由此计算出的实验结果比实际值偏低,排除仪器和操作的因素,其原因可能有:CO未完全反应、 .
②称取8.75g草酸晶体样品配制50.00g溶液,取10.00g溶液加适量的稀硫酸,然后滴加25.00g3.16%KMnO4溶液,恰好反应完全.
(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)则KMnO4溶液显 色,25.00g3.16%KMnO4溶液中KMnO4的质量 g.请计算样品中的质量分数.[写出计算过程,M2(H2C2O4)=90,M2(H2C2O4•2H2O)=126,M2(KMnO4)=158].
查看习题详情和答案>>