网址:http://m.1010jiajiao.com/timu_id_897804[举报]
某化学兴趣小组提出可以用含铜废料制备蓝色胆矾(CuSO4·XH2O)。
查阅资料:
Ⅰ 过氧化氢在常温下会缓慢分解为氧气和水。对其水溶液加热、光照或加催化剂(如MnO2)都会促进其分解。
Ⅱ CuSO4·XH2O易溶于水难溶于酒精,加热时会逐步失去结晶水,最终生成CuSO4。
Ⅲ 白色粉末CuSO4易与水化合生成CuSO4·XH2O
I、硫酸铜晶体的制备
方案1:毛毛同学根据已学知识,提出了制备硫酸铜方案:

方案2:方舟同学查阅资料归纳了一种工业制备硫酸铜的流程:

(1)上述方案1中加热搅拌的作用是 ,形成蓝色溶液的化学反应方程式是: 。
(2)方案2中,加入H2O2后要求温度控制在50℃到60℃是为了防止 。
(3)从环保角度对两套方案的不同部分进行比较,你认为方案 (填1或2)更合理。理由是: 。
(4)方案中“一系列操作”依次为:过滤、、冷却结晶、(填序号)。
A.蒸发浓缩 B.加水稀释 C.加水溶解 D.过滤
(5)溶液M、N都是CuSO4的 (选填“饱和”、“不饱和”或“不一定饱和”)溶液,向其中加入无水CuSO4,均会析出硫酸铜晶体,这是因为 。
⑹所得硫酸铜晶体需要洗涤后晾干,最合适的洗涤试剂是 。
A.冷蒸馏水 B. 95%的酒精 C.热蒸馏水
II、硫酸铜晶体(CuSO4·xH2O)中结晶水(xH2O)含量的测定

学习小组取12.5g硫酸铜晶体(CuSO4·xH2O)进行加热分解,获得相关数据,并绘制成固体质量一温度的关系图。
(7) 258℃时,固体完全变成白色粉末。根据图中数据,计算CuSO4·xH2O中x的值为 。(请写出计算过程,3分)
(8)加热过程中,硫酸铜晶体分步失去结晶水。请写出45℃到110℃时反应方程式
(9) 580℃以上时,硫酸铜粉末就会发生分解,生成黑色金属氧化物、二氧化硫及氧气,此反应的化学方程式为
查看习题详情和答案>>
③碳酸钠溶液与澄清石灰水反应.实验结束后,同学们将所有废液倒入同一个干净的废液缸,为确定缸中废液的组成进行下列实验.请根据现象判断填空(水、酚酞不作考虑,填写的物质范围应不超出这三个实验):
(1)取适量废液缸中的废液加入烧杯中,静置后观察发现底部有白色沉淀且上层清液呈红色.该白色沉淀一定是
(2)取少量上层清液于试管中,加入过量氯化钡溶液,静置后观察发现有白色沉淀,溶液呈红色.则此上层清液中一定有
(3)某同学认为此上层清液中一定还含有NaCl且无需进行实验验证,你认为此结论
 请你参与某学习小组的探究活动,并回答相关问题.
请你参与某学习小组的探究活动,并回答相关问题.
某化学兴趣小组的同学把氢氧化钠的片状固体放在表面皿中,离开实验室,一天后进行观察.
【发现问题】原来的片状固体变成了白色粉末状固体了.
【提出问题】白色粉末状固体物质是什么?
【建立假设】______.
[设计实验]请你来完成以下实验,把相关内容填写在表格中
| 实验方法及操作 | 可能观察到的现象 | 实验结论 |
| ______ | 有气泡产生 | ______ |
(1)有人分析,该白色粉末也有可能为______.
(2)氢氧化钠固体露置在空气中一段时间后,发生了潮解,这个现象说明了空气中含有______,
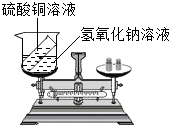
(3)有人设计如图所示的实验来验证质量守恒定律:把装有硫酸铜溶液的小试管放入盛有氢氧化钠溶液的烧杯中,将烧杯放到托盘天平上,用砝码平衡.取下烧杯并将其倾斜,使两种溶液混合反应再把烧杯放到天平上,观察天平是否平衡.你认为上述实设计是否严密?______,请说明理由______.
(4)将部分变质的氢氧化钠全部变为氢氧化钠的化学反应方程式______.
(5)将20g不纯的氢氧化钠固体样品(杂质不溶于水也不参加反应)与一定量的稀硫酸恰好完全反应,最终得到溶质质量分数为10%的溶液142g.求:
(1)样品中氢氧化钠的质量;
(2)加入的稀硫酸的溶质质量分数. 查看习题详情和答案>>
 |
2011年是国际化学年(IYC2011),其宗旨是“增进公众对化学重要性的认识,鼓励青年人热爱化学,学习和研究化学”。某校化学兴趣小组的同学,对课本中一氧化碳还原氧化铁实验作了绿色化改进后制取单质铁(K1,K2是活塞):
(1)关闭K1、开启K2,可以验证CO还原Fe2O3的产物。
①这是关于气体的实验,实验前必须对装置进行
② CO还原Fe2O3的化学方程式为
③在e处点燃气体的目的是
(2)关闭K2,开启K1,可以将d口出来的气体再从a通人装置而循环使用。
① c瓶中应装 (填序号)。
A.澄清石灰水 B.水C.石蕊溶液 D.浓硫酸
②反应完后(假设b瓶中NaOH全部转化为纯碱),要从b瓶中溶液得到纯碱固体,必要的实验操作为转移、 结晶。
③该实验这样改进的主要优点是
查看习题详情和答案>>某化学兴趣小组的同学把氢氧化钠的片状固体放在表面皿中,离开实验室,一天后进行观察.
【发现问题】原来的片状固体变成了白色粉末状固体了.
【提出问题】白色粉末状固体物质是什么?
【建立假设】______.
[设计实验]请你来完成以下实验,把相关内容填写在表格中
| 实验方法及操作 | 可能观察到的现象 | 实验结论 |
| ______ | 有气泡产生 | ______ |
(1)有人分析,该白色粉末也有可能为______.
(2)氢氧化钠固体露置在空气中一段时间后,发生了潮解,这个现象说明了空气中含有______,
(3)有人设计如图所示的实验来验证质量守恒定律:把装有硫酸铜溶液的小试管放入盛有氢氧化钠溶液的烧杯中,将烧杯放到托盘天平上,用砝码平衡.取下烧杯并将其倾斜,使两种溶液混合反应再把烧杯放到天平上,观察天平是否平衡.你认为上述实设计是否严密?______,请说明理由______.
(4)将部分变质的氢氧化钠全部变为氢氧化钠的化学反应方程式______.
(5)将20g不纯的氢氧化钠固体样品(杂质不溶于水也不参加反应)与一定量的稀硫酸恰好完全反应,最终得到溶质质量分数为10%的溶液142g.求:
(1)样品中氢氧化钠的质量;
(2)加入的稀硫酸的溶质质量分数.
 查看习题详情和答案>>
查看习题详情和答案>>