摘要:①瓶A中盛有的试剂是 . 用来吸收水.证明碱式碳酸铜加热分解的产物中有水.②瓶B中盛有的试剂是澄清石灰水.用来 .反应的化学方程式为 .③反应结束.熄灭酒精灯前.应 . (2)木炭和氧化铜反应.生成铜. 将木炭粉末和氧化铜粉末混合均匀.放进试管.加热充分反应.将试管中的粉末倒出.有铜生成.还有少量黑色粉末剩余.该小组同学设计方案验证剩余物质的成分.[查阅资料]部分内容如下:木炭和氧化铜都是黑色粉末.氧化铜与稀硫酸反应生成硫酸铜.木炭与稀硫酸不反应.[猜想与验证] 操作和药品现象分析和结论方案I取少量剩余黑色粉末.充分灼烧 ① .原剩余黑色粉末是氧化铜方案II② .③ .原剩余黑色粉末是氧化铜(3)某同学探究在实际反应中.木炭和氧化铜反应生成铜时反应物的最佳质量比.设计方案如下: 配方1配方2配方3配方4木炭质量(g)
网址:http://m.1010jiajiao.com/timu_id_892448[举报]
(2013?天桥区三模)如图所示为实验室中常见的气体的制备、干燥、净化、收集和性质实验的部分仪器,试根据题目要求
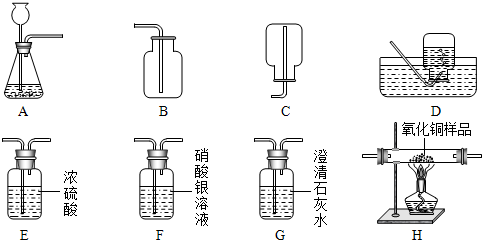
回答下列问题:
(1)用CaCO3固体和稀盐酸反应制取并收集干燥、纯净的二氧化碳.
①所选仪器的连接顺序为
②生成二氧化碳时所发生反应的化学方程式为
(2)小瑜同学欲用锌和稀硫酸反应制取氢气并用干燥的氢气测定某不纯氧化铜样品的纯度(杂质为单质铜),小瑜同学设计了实验方案,选择的装置按A→E1→H→E2→E3顺序连接,然后进行实验(H中发生反应的化学方程式为CuO+H2△Cu+H2O;E1、E2、E3为3个盛有浓硫酸的洗气瓶,假设试剂对气体的吸收均完全).
①装置A中发生反应的化学方程式为
②装置E1的作用是
③给氧化铜样品加热前,小瑜同学先向盛氧化铜样品的玻璃管中通入了一段时间的氢气.你认为他的操作是否正确,并说明理由
④小瑜通过测量反应前后E2装置的质量变化,来计算氧化铜样品的纯度.除此方法,你认为还可以通过测量来计算氧化铜样品纯度的方法是
查看习题详情和答案>>

回答下列问题:
(1)用CaCO3固体和稀盐酸反应制取并收集干燥、纯净的二氧化碳.
①所选仪器的连接顺序为
AFEB
AFEB
(填写仪器序号字母).②生成二氧化碳时所发生反应的化学方程式为
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.(2)小瑜同学欲用锌和稀硫酸反应制取氢气并用干燥的氢气测定某不纯氧化铜样品的纯度(杂质为单质铜),小瑜同学设计了实验方案,选择的装置按A→E1→H→E2→E3顺序连接,然后进行实验(H中发生反应的化学方程式为CuO+H2△Cu+H2O;E1、E2、E3为3个盛有浓硫酸的洗气瓶,假设试剂对气体的吸收均完全).
①装置A中发生反应的化学方程式为
Zn+H2SO4=ZnSO4+H2↑
Zn+H2SO4=ZnSO4+H2↑
.②装置E1的作用是
吸水干燥氢气
吸水干燥氢气
.③给氧化铜样品加热前,小瑜同学先向盛氧化铜样品的玻璃管中通入了一段时间的氢气.你认为他的操作是否正确,并说明理由
正确,先通入氢气,赶走装置中的空气,避免发生爆炸
正确,先通入氢气,赶走装置中的空气,避免发生爆炸
.④小瑜通过测量反应前后E2装置的质量变化,来计算氧化铜样品的纯度.除此方法,你认为还可以通过测量来计算氧化铜样品纯度的方法是
称量氧化铜样品反应前后的质量,通过差值计算纯度
称量氧化铜样品反应前后的质量,通过差值计算纯度
.反应一段时间后先停止对玻璃管的加热并持续通入氢气至玻璃管冷却后,将被测样品取出,发现红色固体中存在少量黑色固体,则小瑜测得的氧化铜样品纯度与实际值比较将偏小
偏小
(填“偏大”、“偏小”、“基本一致”之一).下列说法不科学的是
- A.一般未受污染的天然降水的pH为5.6
- B.长期盛放NaOH溶液的试剂瓶不易打开,是因为NaOH与瓶中的CO2反应导致瓶内气体减少形成“负压”
- C.严格地讲实验室使用“通风橱”防污染是不负责任的,因实验产生的有害气体没有得到转化或吸收
- D.变瘪的乒乓球放入热水中能鼓起来,是因为分子受热膨胀变大