摘要:某校课外小组同学在实验室验证上述反应.(1)加热分解碱式碳酸铜.生成氧化铜.装置如下图所示.
网址:http://m.1010jiajiao.com/timu_id_892447[举报]
某校化学课外兴趣小组的小刚和小强同学到实验室去做探究实验时,他们意外发现实验桌上有一瓶敞口放置的氢氧化钠固体。根据所学化学知识,他们认为此瓶氢氧化钠固体变质了,接着他们对这瓶氢氧化钠固体变质情况进行了探究。提出问题:氢氧化钠固体变质程度如何?查阅资料:
(1)20℃部分物质的溶解性表
(1)20℃部分物质的溶解性表

(2)氯化钙和氯化钠溶液呈中性,不能使无色酚酞变色猜想与假设:
小刚猜想:氢氧化钠可能部分变质,生成了碳酸钠。
小强猜想:_____________。
实验探究:小刚和小强设计探究实验方案,证明了他们各自的猜想。
探究过程如下:
小刚猜想:氢氧化钠可能部分变质,生成了碳酸钠。
小强猜想:_____________。
实验探究:小刚和小强设计探究实验方案,证明了他们各自的猜想。
探究过程如下:

得出结论:小刚的猜想正确。表达与交流
(1)用化学方程式表示氢氧化钠变质的原因:___________。
(2)在实验室里氢氧化钠需要密封保存。药品密封保存的原因很多,请你写出浓盐酸需要密封能够保存的原因_____________。
查看习题详情和答案>>
(1)用化学方程式表示氢氧化钠变质的原因:___________。
(2)在实验室里氢氧化钠需要密封保存。药品密封保存的原因很多,请你写出浓盐酸需要密封能够保存的原因_____________。
(2010?临沂)某校化学课外兴趣小组的小刚和小强同学到实验室去做探究实验时,他们意外发现实验桌上有一瓶敞口放置的氢氧化钠固体.根据所学化学知识,他们认为此瓶氢氧化钠固体变质了,接着他们对这瓶氢氧化钠固体变质情况进行了探究.
[提出问题]:氢氧化钠固体变质程度如何?
[查阅资料]:
(1)20℃部分物质的溶解性表
(2)氯化钙和氯化钠溶液呈中性,不能使无色酚酞变色
[猜想与假设]:
小刚猜想:氢氧化钠可能部分变质,生成了碳酸钠.
小强猜想:
[实验探究]:小刚和小强设计探究实验方案,证明了他们各自的猜想.探究过程如下:
[得出结论]:小刚的猜想正确.
[表达与交流]:
(1)用化学方程式表示氢氧化钠变质的原因
(2)在实验室里氢氧化钠需要密封保存.药品密封保存的原因很多,请你写出浓盐酸需要密封能够保存的原因
查看习题详情和答案>>
[提出问题]:氢氧化钠固体变质程度如何?
[查阅资料]:
(1)20℃部分物质的溶解性表
| OH- | NO3- | Cl- | SO42- | CO32- | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 溶 | 微 | 不 |
[猜想与假设]:
小刚猜想:氢氧化钠可能部分变质,生成了碳酸钠.
小强猜想:
氢氧化钠完全变质
氢氧化钠完全变质
.[实验探究]:小刚和小强设计探究实验方案,证明了他们各自的猜想.探究过程如下:
| 实验步骤 | 实验操作 | 实验现象 | 实验结论或化学方程式 |
| 步 骤 一 | 取样品,加水配制成溶液,并向其中滴加适量氯化钙溶液,充分反应后过滤 | 有 白色沉淀 白色沉淀 生成 | 氢氧化钠已变质.写出加入氯化钙溶液后发生反应的化学方程式 Na2CO3+CaCl2=CaCO3↓+2NaCl Na2CO3+CaCl2=CaCO3↓+2NaCl . |
| 步 骤 二 | 取上述少量滤液于试管中,滴加无色酚酞溶液 | 酚酞溶液变 为 红 红 色 | 氢氧化钠部分变质 |
[得出结论]:小刚的猜想正确.
[表达与交流]:
(1)用化学方程式表示氢氧化钠变质的原因
CO2+2NaOH=Na2CO3+H2O
CO2+2NaOH=Na2CO3+H2O
.(2)在实验室里氢氧化钠需要密封保存.药品密封保存的原因很多,请你写出浓盐酸需要密封能够保存的原因
浓盐酸易挥发
浓盐酸易挥发
.(7分)孔雀石主要成分是碱式碳酸铜[Cu2(OH)2CO3],绿色并具有浓淡的条状花纹(见右图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料。某校课外小组同学欲在实验室验证碱式碳酸铜制铜的反应原理。
【查阅资料】
1.Cu2(OH)2CO3  2CuO+CO2 + H2O
2CuO+CO2 + H2O
2CuO+C 2Cu + CO2 ↑
2Cu + CO2 ↑
2.CuO为黑色固体,化学性质和氧化铁相似。
(1)实验l:加热分解碱式碳酸铜。装置如图所示。
①A中固体的变化为____。
②欲证明反应后有水生成,B中所盛试剂为____。
③反应结束时的操作应该是____,理由是____。
(2)实验2:木炭和氧化铜反应。
将木炭粉末和氧化铜粉末混合均匀,放进试管加热,反应后将试管中的粉末倒出,有铜生成,还有少量黑色粉末剩余。该小组同学设计方案验证黑色粉末的成分。
【作出猜想】
剩余黑色粉末可能是:①氧化铜;②木炭;③木炭和氧化铜。
【实验验证】填写下表。
| 实验操作及现象 | 实验结论 |
| | 该黑色粉末为氧化铜 |
| | 配方l | 配方2 | 配方3 | 配方4 |
| 木炭质量(g) | 0.4 | 0.5 | 0.6 | 0.7 |
| 氧化铜质量(g) | 8 | 8 | 8 | 8 |
(7分)孔雀石主要成分是碱式碳酸铜[Cu2(OH)2CO3],绿色并具有浓淡的条状花纹(见右图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料。某校课外小组同学欲在实验室验证碱式碳酸铜制铜的反应原理。

【查阅资料】
1.Cu2(OH)2CO3 2CuO+CO2 + H2O
2CuO+CO2 + H2O
2CuO+C 2Cu + CO2 ↑
2Cu + CO2 ↑
2.CuO为黑色固体,化学性质和氧化铁相似。
(1)实验l:加热分解碱式碳酸铜。装置如图所示。

①A中固体的变化为____。
②欲证明反应后有水生成,B中所盛试剂为____。
③反应结束时的操作应该是____,理由是____。
(2)实验2:木炭和氧化铜反应。
将木炭粉末和氧化铜粉末混合均匀,放进试管加热,反应后将试管中的粉末倒出,有铜生成,还有少量黑色粉末剩余。该小组同学设计方案验证黑色粉末的成分。
【作出猜想】
剩余黑色粉末可能是:①氧化铜;②木炭;③木炭和氧化铜。
【实验验证】填写下表。
(3)某同学探究在实际反应中,木炭和氧化铜反应生成铜时反应物的最佳质量比,设计方案如下:
上述设计方案的主要研究方法是__________________。

【查阅资料】
1.Cu2(OH)2CO3
 2CuO+CO2 + H2O
2CuO+CO2 + H2O2CuO+C
 2Cu + CO2 ↑
2Cu + CO2 ↑2.CuO为黑色固体,化学性质和氧化铁相似。
(1)实验l:加热分解碱式碳酸铜。装置如图所示。

①A中固体的变化为____。
②欲证明反应后有水生成,B中所盛试剂为____。
③反应结束时的操作应该是____,理由是____。
(2)实验2:木炭和氧化铜反应。
将木炭粉末和氧化铜粉末混合均匀,放进试管加热,反应后将试管中的粉末倒出,有铜生成,还有少量黑色粉末剩余。该小组同学设计方案验证黑色粉末的成分。
【作出猜想】
剩余黑色粉末可能是:①氧化铜;②木炭;③木炭和氧化铜。
【实验验证】填写下表。
| 实验操作及现象 | 实验结论 |
| | 该黑色粉末为氧化铜 |
| | 配方l | 配方2 | 配方3 | 配方4 |
| 木炭质量(g) | 0.4 | 0.5 | 0.6 | 0.7 |
| 氧化铜质量(g) | 8 | 8 | 8 | 8 |
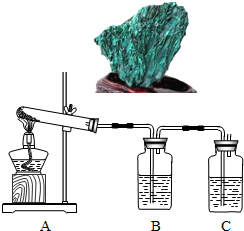 孔雀石主要成分是碱式碳酸铜[Cu2(OH)2CO3],绿色并具有浓淡的条状花纹(见右图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料.某校课外小组同学欲在实验室验证碱式碳酸铜制铜的反应原理.
孔雀石主要成分是碱式碳酸铜[Cu2(OH)2CO3],绿色并具有浓淡的条状花纹(见右图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料.某校课外小组同学欲在实验室验证碱式碳酸铜制铜的反应原理.
查阅资料:①Cu2(OH)2CO3 2CuO+CO2↑+H2O 2CuO+C
2CuO+CO2↑+H2O 2CuO+C 2Cu+CO2↑
2Cu+CO2↑
②CuO为黑色固体,化学性质和氧化铁相似.
(1)实验l:加热分解碱式碳酸铜.装置如图所示.
①A中固体的变化为______.
②欲证明反应后有水生成,B中所盛试剂为______.
③反应结束时的操作应该是______,理由是______.
(2)实验2:木炭和氧化铜反应.
将木炭粉末和氧化铜粉末混合均匀,放进试管加热,反应后将试管中的粉末倒出,有铜生成,还有少量黑色粉末剩余.该小组同学设计方案验证黑色粉末的成分.
做出猜想:剩余黑色粉末可能是:①氧化铜;②木炭;③木炭和氧化铜.
实验验证:填写下表.
| 实验操作及现象 | 实验结论 |
| 该黑色粉末为氧化铜 |
| 配方l | 配方2 | 配方3 | 配方4 | |
| 木炭质量(g) | 0.4 | 0.5 | 0.6 | 0.7 |
| 氧化铜质量(g) | 8 | 8 | 8 | 8 |