网址:http://m.1010jiajiao.com/timu_id_885597[举报]

I.实验操作步骤如下:
①检查装置的气密性.
②装入药品,连接好仪器.
③夹紧弹簧夹,加热白磷,观察现象.
④等燃烧结束,试管冷却后打开弹簧夹,观察现象.
II.实验现象记录:
在步骤③中加热时观察到白磷燃烧,产生
在步骤④中待装置冷却后,打开弹簧夹,观察到活塞慢慢向
Ⅲ.实验结论:氧气占空气的体积分数约为
| 1 |
| 5 |
| 1 |
| 5 |
(二)另有化学兴趣小组的同学对实验室制备氧气的条件进行探究.
Ⅰ.为探究不同催化剂对氯酸钾分解速率的影响,甲组设计了以下两个对比实验:在相同的温度下,比较两组实验产生O2的快慢.
①将3.0g KClO3与1.0g MnO2均匀混合加热.
②将x g KClO3与1.0g CuO均匀混合加热.
(1)试写出实验①中所发生反应的化学方程式
| ||
| △ |
| ||
| △ |
(2)实验②中x的值应为
Ⅱ.为探究是否使用催化剂对双氧水(H2O2)分解速率的影响,乙组采用如图2装置,进行有催化剂和无催化剂时的对比实验.
实验中应记录的数据主要是反应时间和
Ⅲ.为探究的双氧水(H2O2)浓度对其分解速率的影响,丙组设计了以下实验.实验
数据记录如下:
| 序号 | 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 |
| ① | 50.0g | 1% | 0.1g | 9mL |
| ② | 50.0g | 2% | 0.1g | 16mL |
| ③ | 50.0g | 4% | 0.1g | 31mL |

(2)丙组实验获得的结论:在相同条件下,

I.实验操作步骤如下:
①检查装置的气密性.
②装入药品,连接好仪器.
③夹紧弹簧夹,加热白磷,观察现象.
④等燃烧结束,试管冷却后打开弹簧夹,观察现象.
II.实验现象记录:
在步骤③中加热时观察到白磷燃烧,产生______.活塞开始时向______移动(填“左”或“右”或“不”).
在步骤④中待装置冷却后,打开弹簧夹,观察到活塞慢慢向______移动(填“左”或“右”),最终停在约______ mL刻度处(取整数值).
Ⅲ.实验结论:氧气占空气的体积分数约为______.
(二)另有化学兴趣小组的同学对实验室制备氧气的条件进行探究.
Ⅰ.为探究不同催化剂对氯酸钾分解速率的影响,甲组设计了以下两个对比实验:在相同的温度下,比较两组实验产生O2的快慢.
①将3.0g KClO3与1.0g MnO2均匀混合加热.
②将x g KClO3与1.0g CuO均匀混合加热.
(1)试写出实验①中所发生反应的化学方程式______;
(2)实验②中x的值应为______.
Ⅱ.为探究是否使用催化剂对双氧水(H2O2)分解速率的影响,乙组采用如图2装置,进行有催化剂和无催化剂时的对比实验.
实验中应记录的数据主要是反应时间和______,可以通过比较单位时间内在______ 中(填仪器名称)的物质质量变化的多与少,达到实验目的.
Ⅲ.为探究的双氧水(H2O2)浓度对其分解速率的影响,丙组设计了以下实验.实验
数据记录如下:
| 序号 | 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 |
| ① | 50.0g | 1% | 0.1g | 9mL |
| ② | 50.0g | 2% | 0.1g | 16mL |
| ③ | 50.0g | 4% | 0.1g | 31mL |

(2)丙组实验获得的结论:在相同条件下,______,双氧水分解得越快.
(1)下列实验操作或对实验事实的叙述中存在错误的是__ ____(填序号)
A、用50 mL酸式滴定管准确量取25.00 mL 酸性KMnO4溶液,放入锥形瓶中待用
B、在测定硫酸铜晶体的结晶水时,将灼烧硫酸铜晶体的坩埚放在空气中冷却,然后称量
C、中和热的测定所需的玻璃仪器有烧杯、温度计、量筒
D、实验室中进行的下列实验需水浴加热:①乙酸乙酯的制备②葡萄糖的银镜反应
E、配制1 mol?L-1的NaOH溶液时,下列操作会造成所配浓度偏低:①溶解后烧杯未多次洗涤 ②定容时仰视刻度线 ③容量瓶中原有少许蒸馏水
F、实验室配制氯化亚铁溶液时,将氯化亚铁先溶解在盐酸中,然后用蒸馏水稀释并加入少量铁粉
G、容量瓶检漏:在容量瓶中注入适量的水,塞上玻璃瓶塞,左手五指托住瓶底,右手食指顶住瓶塞,反复倒置数次,观察是否漏水
H、不用其他试剂无法鉴别下列四种溶液:Na2CO3、Al2(SO4)3、NaCl、NaHSO4
I、可以用分液漏斗分离下列三组液态混合物:硝基苯和水、油酸和水、乙酸乙酯和乙醇
J、实验室保存少量液溴和白磷常用水封
(2)某研究性学习小组拟用明矾制取Al2(SO4)3晶体和K2SO4晶体。
①实验室除明矾外,已备好的用品有蒸馏水、氨水、pH试纸,还缺少的试剂有 。
②制得Al2(SO4)3与K2SO4物质的量之比小于 。
(3)“磨砂”是增加玻璃仪器密封性的一种处理工艺 ,可使仪器不漏液或不漏气。在下列仪器中:①试管;②分液漏斗;③细口试剂瓶;④广口试剂瓶;⑤集气瓶;⑥滴瓶;⑦酸式滴定管;⑧碱式滴定管,肯定用不到“磨砂” 处理的有 (填序号)。
(4)碱式氯化铜 (不溶于水的绿色结晶)是一种农药,化学式为:CuCl2·3Cu(OH)2·xH2 O。为验证其组成并确定X值,某学生设计了以下几步实验
①取a g碱式氯化铜的晶体制成粉末。
②将晶体加热至确认质量不再变化为止(铜仍为二价),冷却后称其质量为b g。
③另取a g碱式氯化铜的晶体,溶于足量硝酸中,得到溶液。
④向③得到的溶液中加入足量的硝酸银溶液,最后得到纯净固体,称量为c g。
若以上操作均正确,试回答下列问题:
A.将晶体制成粉末,所用的主要化学仪器是 (填仪器名称)。以上四步中,用到玻璃棒的步骤有 (填序号)
B.步骤②灼烧后得到的固体应为: 。
C.步骤④主要包括:加入足量硝酸银溶液→ → → 晾干→称量
查看习题详情和答案>>(1)生活中的燃烧
①着火点比较:蜂窝煤
②用水灭火的原理是
(2)金属在生活中用途广泛
①如图1下列生活用品,主要是由金属材料制成的是

| 品名:504双吸剂 成分:铁粉、NaCl、炭粉CaO等 |
②用铁锅烹饪食物时,会有少量铁屑在胃部转化为可被吸收的Fe2+,反应的化学方程式为
③用铝箔包装药物,主要利用了铝的
④铜具有很好的
(3)生活中的水和溶液
①处理自然水时,常用的混凝剂是
②欲配制500mL 0.9%的生理盐水(密度为1.0g/mL),需要NaCl的质量为
③图2是净化河水的简易装置,下列说法正确的是
A.净化后的水是纯净物 B.此装置能对水杀菌消毒
C.此装置能把硬水变为软水 D.活性炭能吸附水中的色素及异味
④KNO3可用作配制无土栽培营养液,下表提供了KNO3在不同温度时的溶解度:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
b.20℃时,将20gKNO3加入50g水中充分溶解,所得溶液的质量为
c.现有60℃时的KNO3饱和溶液210g,降温至20℃,会析出KNO3
(4)食品包装学问大
①我区特产--嘶马羊耳采用真空包装,延长了食品的保质期,原理是
②将N2充入包装袋内做保护气,是因为N2的化学性质
③图3是“504双吸剂”的标签,请问答下列问题:
a.其中至少含有
b.取少量双吸剂加入蒸馏水中,振荡后静置,测得上层清液的pH=9,若用pH试纸测定,具体操作是
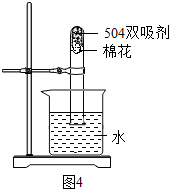
c.为测定此双吸剂的使用效果,取足量双吸剂做了如图4所示的实验,一段时间后,进入试管中水的体积
d.部分失效的双吸剂中,有红棕色固体,其主要是
e.此双吸剂中,NaCl的作用可能是
|