网址:http://m.1010jiajiao.com/timu_id_75411[举报]
生物答案:
1D 2B 3D 4B 5B
30、Ⅰ.(每空1分共计8分)(1)略 叶绿体片层结构薄膜;4
(2)CO2→C4→C3→(CH2O) (3)主动运输
(4)肝糖元 (5)磷脂; 脂蛋白; 合理膳食并注意吃一些含卵磷脂较多的食物
Ⅱ、(每空2分共计18分)(1)①实验前要先测甲、乙鼠的体温 ②实验要有重复性,仅用两只小白鼠进行实验有一定的偶然性
(2)赞同。先做不破坏下丘脑的实验,再做破坏下丘脑的实验,进行自身前后对照 (3)B、D A、C (4)甲状腺激素和肾上腺素 神经―体液 (5)①神经系统兴奋性降低,精神萎靡 ②食欲降低
31.(每空2分共计16分)(1)Bb//Bb、bb (2)BB和bb//Bb (3) 黑、红个体
全为纯合子//黑、红种牛为双亲的一方 (4) B栏中黑色纯合子基因型为BB,只
产生一种B配子,且栏中红色个体均为同一性别 (5) B栏中杂合黑色全为同一
性别,并且与红色个体为同一性别
化学答案:
6.C.7. D.8.B.9.C.10.D.11.C.12.A.13.D.
25.(每空3分)
 ⑴
N2H4(l)+2H2O2(l)==N2(g)+4H2O(g);△H= ―817.6KJ/mol
⑴
N2H4(l)+2H2O2(l)==N2(g)+4H2O(g);△H= ―817.6KJ/mol
CO2、C2H2、N2O(任写两种)
⑵
NH4+ + H2O  NH3 °H2O + H+
NH3 °H2O + H+
26.. Ⅰ①②⑦⑧ (4分)
(每空2分)
Ⅱ(1) 石灰乳原料丰富,成本低 (2) MgCl2(或氯化镁) 过滤 洗涤
 (3)制备干燥的HCl气体 (4)
MgCl2(熔融) Mg
+Cl2↑
(3)制备干燥的HCl气体 (4)
MgCl2(熔融) Mg
+Cl2↑
27.(每空2分)
(1)> (2)增大 (3)=,a=b+c (4) c
(5)>,由于始终保持较大压强,故反应物的转化率较高,生成的C3比恒容时多,则放出的热量也大。
28.(每空3分)
(1) (2)
(2) +2NaOH
+2NaOH
 +2NaBr
+2NaBr
(3) (4)羟基,羧基 (5)(6分)
(4)羟基,羧基 (5)(6分)

或

物理答案:
题号
14
15
16
17
18
19
20
21
答案
BD
C
A
B
D
C
C
BCD
 22.(17分)
22.(17分)
 (1)13.85 (5分)
(1)13.85 (5分)
(2)① (3分)
测量电路如图所示 (3分)
②  (2分)
(2分)
 (2分)
(2分)
③ 建议一:多测几组R、U数据,分别求出相应的I值,用U、I数据作出U―I图线,由图线的截距、斜率求出E、r 。
建议二:由 可推出
可推出 ,多测几组R、U数据,作
,多测几组R、U数据,作 ―
― 图线(为一直线),由图线的截距、斜率求出E、r 。
图线(为一直线),由图线的截距、斜率求出E、r 。
建议三:由 可推出
可推出 ,作
,作 ―
― 图线(为一直线),由图线的截距、斜率求出E、r 。 (2分)
图线(为一直线),由图线的截距、斜率求出E、r 。 (2分)
其他建议合理的同样给分。
因电表选错导致①、②不能得分的,第③题可参照评分标准酌情给分。
23.解:(1)设他们的最大速度为 ,乙的加速度为
,乙的加速度为 ,则
,则
 即
即
于是求得乙接棒时达到最大速度的80%需在接力区须奔跑的距离为
 (2)设乙应在距离甲为
(2)设乙应在距离甲为 时起跑,
时起跑,
由于 , 即
, 即 
所以 
24.解析:(1)当裸导线向左运动到离O点的距离为x, 裸导线中有电流的长度为y,则回路的电动势为: (2分)
(2分)
设回路的周长为L,则回路的总电阻为 (2分)
(2分)
根据欧姆定律可得回路中的电流为: (2分)
(2分)
根据平衡条件得: (2分)
(2分)
根据几何知识求得: ,
, (4分)
(4分)
由以上方程解得: (2分)
(2分)
(2)最终裸导线只能静止在O点,所以裸导线的动能将全部转化为焦耳热. (2分)
即 (3分)
(3分)
25.(20分) 解:(1)(8分)由题意可知:
m 、M之间的最大静摩擦力f=μ(mg+qE)=4N (2分)
m 、M一起运动的最大加速度 (2分)
(2分)
 (2分)
(2分)
 (2分)
(2分)
⑵(12分)








 S=
S=
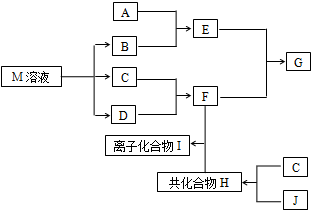
 短周期元素的单质C、D、J在通常状况下均为气态,且常见双原子单质分子,J分子共价键最多;H分子中含10个电子;物质M由同一短周期的X、Y两种元素组成,X原子最外层电子数是最内层电子数的1/2,Y元素最高正价与它的负价代数和为6.M与其它物质的转化关系如图(部分产物及反应条件已略去)则:
短周期元素的单质C、D、J在通常状况下均为气态,且常见双原子单质分子,J分子共价键最多;H分子中含10个电子;物质M由同一短周期的X、Y两种元素组成,X原子最外层电子数是最内层电子数的1/2,Y元素最高正价与它的负价代数和为6.M与其它物质的转化关系如图(部分产物及反应条件已略去)则:(1)X的离子结构示意图为




(2)若A是与X、Y同周期的一种常见金属单质,则A与B溶液反应的化学方程式是
(3)若A是一种常见酸性氧化物,且可用于制造玻璃,则E与F反应的离子方程式是
(4)将一定量F和H的水溶液混合使其溶液显碱性,则此溶液中离子浓度由大到小的顺序是
(5)汽油是一种可燃性液体,汽油-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液,该电池放电时的正极反应式为
 短周期元素的单质C、D、J在通常状况下均为气态,且常见双原子单质分子,J分子共价键最多;H分子中含10个电子;物质M由同一短周期的X、Y两种元素组成,X原子最外层电子数是最内层电子数的1/2,Y元素最高正价与它的负价代数和为6.M与其它物质的转化关系如图(部分产物及反应条件已略去)则:
短周期元素的单质C、D、J在通常状况下均为气态,且常见双原子单质分子,J分子共价键最多;H分子中含10个电子;物质M由同一短周期的X、Y两种元素组成,X原子最外层电子数是最内层电子数的1/2,Y元素最高正价与它的负价代数和为6.M与其它物质的转化关系如图(部分产物及反应条件已略去)则:
(1)X的离子结构示意图为______;J的电子式是______.
(2)若A是与X、Y同周期的一种常见金属单质,则A与B溶液反应的化学方程式是______.
(3)若A是一种常见酸性氧化物,且可用于制造玻璃,则E与F反应的离子方程式是______.
(4)将一定量F和H的水溶液混合使其溶液显碱性,则此溶液中离子浓度由大到小的顺序是______.
(5)汽油是一种可燃性液体,汽油-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液,该电池放电时的正极反应式为______.
查看习题详情和答案>>
(1)X的离子结构示意图为______;J的电子式是______.
(2)若A是与X、Y同周期的一种常见金属单质,则A与B溶液反应的化学方程式是______.
(3)若A是一种常见酸性氧化物,且可用于制造玻璃,则E与F反应的离子方程式是______.
(4)将一定量F和H的水溶液混合使其溶液显碱性,则此溶液中离子浓度由大到小的顺序是______.
(5)汽油是一种可燃性液体,汽油-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液,该电池放电时的正极反应式为______.
 查看习题详情和答案>>
查看习题详情和答案>>
| A | 单质在自然界中硬度最大 |
| B | 原子中s能级与p能级电子数相等且有单电子 |
| C | C同在B的下一周期,C的电离能数据(kJ?mol-1)为:I1=738 I2=1451 I3=7732 I4=10540 |
| D | 单质密度小,较好的延展性,广泛用于食品包装,D的氧化物是两性氧化物 |
| E | 单质是一种常见金属,与O元素能形成黑色和砖红色两种氧化物 |
(2)常温下,某气态单质甲分子与AB分子核外电子数相等,则一个甲分子中包含
(3)B的氢化物的熔沸点比与它同主族的下一周期元素的氢化物的熔沸点高,原因是
(4)通常情况下,A的燃烧热为a kJ?mol-1,C的燃烧热为b kJ?mol-1,则C与AO2反应生成A的热化学方程式为
(1)BE2的电子式是


(2)实验室制取B2A2的化学方程式是:
(3)常温下液态化合物甲只含上述元素中的两种,分子中原予个数比为1:1,仅用一个化学方程式表示甲既有氧化性又有还原性:
| ||
| ||
(4)电解质乙和丙由上述元素中的几种组成,l mol乙或丙中均含有20mol电子,丙可以抑制乙在水溶液中的电离,则丙中的化学键类型有
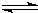 NH4++OH-
NH4++OH-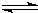 NH4++OH-
NH4++OH-(5)由A、B两元素形成的含18个电子的气态化合物,该化合物与氧气和KOH溶液可构成燃料电池,写出该燃料电池负极电极反应式: