摘要:K===0.90mol/L 水浴加热
网址:http://m.1010jiajiao.com/timu_id_577073[举报]
在硫酸铝、硫酸钾和明矾的混合液中,如果SO42-的浓度为0.4mol/L,当加入等体积0.4mol/L KOH溶液时,生成沉淀恰好完全溶解,则反应后混合溶液中K+浓度约为
[ ]
A、0.250mol/L
B、0.225mol/L
C、0.450mol/L
D、0.90mol/L
查看习题详情和答案>>
B、0.225mol/L
C、0.450mol/L
D、0.90mol/L
 在20L恒容的密闭容器中,加入3molSO3(g)和1mol氧气,在某温度下使其反应,反应至4min时,氧气的浓度为0.06mol/L,当反应到8min时,反应到达平衡.
在20L恒容的密闭容器中,加入3molSO3(g)和1mol氧气,在某温度下使其反应,反应至4min时,氧气的浓度为0.06mol/L,当反应到8min时,反应到达平衡.(1)0min-4min内生成O2的平均速率v(O2)=
0.025mol?L-1?min-1
0.025mol?L-1?min-1
mol/(L?min)(2)整个过程中,各物质的浓度与时间关系如图所示,则该温度下的平衡常数
K=
0.4mol?L-1
0.4mol?L-1
(3)若起始时按下表数据投料,相同温度下达到平衡时,三氧化硫浓度大于0.05mol/L的是
BD
BD
,此时的平衡常数与(2)小题比较等于
等于
(填“大于”、“小于”或“等于”)| A | B | C | D | |
| SO3 | 1mol | 3mol | 3mol | 0mol |
| SO2 | 2mol | 1.5mol | 0mol | 6mol |
| O2 | 2mol | 1mol | 0mol | 5mol |
①③④
①③④
(填序号)①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均分子量不再改变
④V正(SO3)=2V逆(O2)
⑤n(SO3):n(O2):n(SO2)=2:1:2.
 二甲醚(CH3OCH3)是一种高效、清洁,具有优良环保性能的新型燃料.工业上制备二甲醚时在催化反应室中(压强2.0~10.0MPa,温度230~280℃)进行的反应为:
二甲醚(CH3OCH3)是一种高效、清洁,具有优良环保性能的新型燃料.工业上制备二甲醚时在催化反应室中(压强2.0~10.0MPa,温度230~280℃)进行的反应为:①CO(g)+2H2(g)?CH3OH(g)△H1=-90.7kJ?mol-1,
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-23.5kJ?mol-1,
③CO(g)+H2O(g)?CO2(g)+H2(g)△H3=-41.2kJ?mol-1,
(1)催化反应室中总反应3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)的△H=
-246.1KJ/mol
-246.1KJ/mol
.(2)在温度和容积不变的条件下发生反应①,能说明该反应达到化学平衡状态的依据是
ab
ab
(多选扣分).a.容器中压强保持不变;b.混合气体中c(CO)不变;c.v正(CO)=v逆(H2);d.c(CH3OH)=c(CO)
(3)在2L的容器中加入amolCH3OH(g)发生反应②,达到平衡后若再加入amolCH3OH(g)重新达到平衡时,CH3OH的转化率
不变
不变
(填“增大”、“减小”或“不变”).(4)850℃时在一体积为10L的容器中通入一定量的CO和H2O(g)发生反应③,CO和H2O(g)浓度变化如图所示.
①0~4min的平均反应速率υ(CO)=
0.03mol/L?min
0.03mol/L?min
.②若温度不变,向该容器中加入4molCO、2molH2O、3molCO2(g)和3molH2(g),起始时D正
<
<
V逆(填“<”、“>”或“=”),请结合必要的计算说明理由Qc=
=
,K=
=1,因为Qc>K,平衡左移,V正<V逆
| 0.3,mol/L×0,3mol/L |
| 0.4mol/L×0.2mol/L |
| 9 |
| 8 |
| 0.12mol/L×0.12mol/L |
| 0.08mol/L×0.18mol/L |
Qc=
=
,K=
=1,因为Qc>K,平衡左移,V正<V逆
.| 0.3,mol/L×0,3mol/L |
| 0.4mol/L×0.2mol/L |
| 9 |
| 8 |
| 0.12mol/L×0.12mol/L |
| 0.08mol/L×0.18mol/L |
光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用CO与Cl2在活性炭催化下合成.
(1)实验室中常用来制备氯气的化学方程式为
(2)工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2和CO的燃烧热(△H)分别为-890.3kJ?mol-1、-285.8kJ?mol-1、-283.0kJ?mol-1,则生成1m3(标准状况)CO所需热量为
(3)实验室中可用氯仿(CHCl3)与双氧水直接反应制备光气,其反应的化学方程式为
(4)COCl2的分解反应为COCl2(g)=Cl2(g)+CO(g)△H=+108kJ?mol-1.反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如图所示(第10min到14min的浓度变化曲线未示出):

①计算反应在第8min时的平衡常数K=
②比较第2min反应温度T(2)与第8min反应温度T(8)的高低:T(2)
③若12min时反应于T(8)下重新达到平衡,则此时c(COCl2)=
④比较产物CO在2~3min、5~6min、12~13min时平均反应速率[平均反应速率分别以v(2~3)、v(5~6)、v(12~13)表示]的大小
⑤比较反应物COCl2在5~6min、15~16min时平均反应速率的大小:v(5~6)
查看习题详情和答案>>
(1)实验室中常用来制备氯气的化学方程式为
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
;
| ||
(2)工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2和CO的燃烧热(△H)分别为-890.3kJ?mol-1、-285.8kJ?mol-1、-283.0kJ?mol-1,则生成1m3(标准状况)CO所需热量为
5.52×103KJ
5.52×103KJ
;(3)实验室中可用氯仿(CHCl3)与双氧水直接反应制备光气,其反应的化学方程式为
CHCl3+H2O2=HCl+H2O+COCl2
CHCl3+H2O2=HCl+H2O+COCl2
;(4)COCl2的分解反应为COCl2(g)=Cl2(g)+CO(g)△H=+108kJ?mol-1.反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如图所示(第10min到14min的浓度变化曲线未示出):

①计算反应在第8min时的平衡常数K=
0.234mol?L-1
0.234mol?L-1
;②比较第2min反应温度T(2)与第8min反应温度T(8)的高低:T(2)
<
<
T(8)(填“>”、“<”或“=”)③若12min时反应于T(8)下重新达到平衡,则此时c(COCl2)=
0.031
0.031
mol?L-1④比较产物CO在2~3min、5~6min、12~13min时平均反应速率[平均反应速率分别以v(2~3)、v(5~6)、v(12~13)表示]的大小
v(5~6)>v(2~3)=v(12~13)
v(5~6)>v(2~3)=v(12~13)
;⑤比较反应物COCl2在5~6min、15~16min时平均反应速率的大小:v(5~6)
>
>
v(15~16)(填“>”、“<”或“=”),原因是在相同温度时,该反应的反应物的浓度越高,反应速率越大
在相同温度时,该反应的反应物的浓度越高,反应速率越大
.(2012?深圳二模)苯乙烷(  -C2H5)可生产塑料单体苯乙烯(
-C2H5)可生产塑料单体苯乙烯( -CH=CH2),其原理反应是:
-CH=CH2),其原理反应是:
 -C2H5(g)
-C2H5(g) 
 -CH=CH2(g)+H2(g);△H=+125kJ?mol-1.某温度下,将0.40mol
-CH=CH2(g)+H2(g);△H=+125kJ?mol-1.某温度下,将0.40mol  -C2H5(g)充入2L真空密闭容器中发生反应,测定该容器内的物质,得到数据如下表:
-C2H5(g)充入2L真空密闭容器中发生反应,测定该容器内的物质,得到数据如下表:
(1)n1=
(2)工业上常以高温水蒸气作为反应体系的稀释剂(不参与反应). -C2H5(g)的平衡转化率与水蒸气的用量、体系总压强的关系如图1所示.当其它条件不变时,水蒸气的用量越大,平衡转化率将
-C2H5(g)的平衡转化率与水蒸气的用量、体系总压强的关系如图1所示.当其它条件不变时,水蒸气的用量越大,平衡转化率将
(3)副产物H2用做氢氧燃料电池.写出酸性条件下,该电池正极的电极反应式
(4)在相同条件下,若最初向该容器中充入 -CH=CH2(g)和H2(g),假设在40min时达到上述同样的平衡状态,请在图2中画出并标明该条件下
-CH=CH2(g)和H2(g),假设在40min时达到上述同样的平衡状态,请在图2中画出并标明该条件下  -C2H5(g)和
-C2H5(g)和 -CH=CH2(g)的浓度c随时间t变化的曲线
-CH=CH2(g)的浓度c随时间t变化的曲线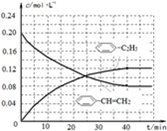
 .
.
查看习题详情和答案>>
 -C2H5)可生产塑料单体苯乙烯(
-C2H5)可生产塑料单体苯乙烯( -CH=CH2),其原理反应是:
-CH=CH2),其原理反应是: -C2H5(g)
-C2H5(g) 
 -CH=CH2(g)+H2(g);△H=+125kJ?mol-1.某温度下,将0.40mol
-CH=CH2(g)+H2(g);△H=+125kJ?mol-1.某温度下,将0.40mol  -C2H5(g)充入2L真空密闭容器中发生反应,测定该容器内的物质,得到数据如下表:
-C2H5(g)充入2L真空密闭容器中发生反应,测定该容器内的物质,得到数据如下表:
| 时间/min | 0 | 10 | 20 | 30 | 40 |
n( -C2H5)/mol -C2H5)/mol |
0.40 | 0.30 | 0.26 | n2 | n3 |
n( -CH=CH2)/mol -CH=CH2)/mol |
0.00 | 0.10 | n1 | 0.16 | 0.16 |
0.14
0.14
mol,计算该反应的平衡常数,K=0.053mol?L-1
0.053mol?L-1
.(2)工业上常以高温水蒸气作为反应体系的稀释剂(不参与反应).
 -C2H5(g)的平衡转化率与水蒸气的用量、体系总压强的关系如图1所示.当其它条件不变时,水蒸气的用量越大,平衡转化率将
-C2H5(g)的平衡转化率与水蒸气的用量、体系总压强的关系如图1所示.当其它条件不变时,水蒸气的用量越大,平衡转化率将越大
越大
(填“越大”、“越小”或“不变”),原因是体系总压强一定时,水蒸气的分压越大,平衡体系的分压越小,平衡向气体体积增大的方向移动;
体系总压强一定时,水蒸气的分压越大,平衡体系的分压越小,平衡向气体体积增大的方向移动;
.(3)副产物H2用做氢氧燃料电池.写出酸性条件下,该电池正极的电极反应式
O2+4H++4e-=2H2O
O2+4H++4e-=2H2O
.(4)在相同条件下,若最初向该容器中充入
 -CH=CH2(g)和H2(g),假设在40min时达到上述同样的平衡状态,请在图2中画出并标明该条件下
-CH=CH2(g)和H2(g),假设在40min时达到上述同样的平衡状态,请在图2中画出并标明该条件下  -C2H5(g)和
-C2H5(g)和 -CH=CH2(g)的浓度c随时间t变化的曲线
-CH=CH2(g)的浓度c随时间t变化的曲线
