摘要:6.对数据的分析归纳可得到科学的结论和规律.下列为某同学对数据的利用情况.其中不正确的是 A.根据非金属单质与氢气化合生成1mol产物时反应热的大小推测生成物的稳定性 B.用沸点数据推测用蒸馏法分离两种液体混合物的可能性 C.用熔点数据分析不同分子的稳定性 D.用原子半径数据推断某些原子氧化性或还原性的相对强弱
网址:http://m.1010jiajiao.com/timu_id_575846[举报]
一、选择题(本题共10分),每小题2分,选对得2分,选错得0分。
1―5DDCDB
二、选择题(本题共36分),每小题3分,选对得3分,选错得0分
6―10CDCAB 11―15BCDDC 16―17BD
三、选择题(本题共20分),每小题4分,若正确答案啼包括一个选项,选对得4分,错选若多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给4分,但只要选错一个,该小题就为0分。
18.AC 19.B 20.BD 21.AC 22.C
四、(本题共24分)
(1)3s23p4,14。(1分×2)
(2)2Al+2OH-+2H2O→2AlO2-+3H2↑,小于。(1分×2)
.files/image045.gif) ,吸。(1分×2)
,吸。(1分×2).files/image047.gif) (1分×2)
(1分×2).files/image049.jpg)
.files/image050.gif)
.files/image051.gif) (4)C6H5―CH―18OH+HCOOH HCO18O―CH―C6H5+H2O(2分)
(4)C6H5―CH―18OH+HCOOH HCO18O―CH―C6H5+H2O(2分).files/image053.jpg)
.files/image055.jpg)
.files/image057.jpg)
.files/image059.jpg)
 是导致汽车尾 气中含有NO的重要原因之一。
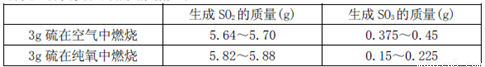
是导致汽车尾 气中含有NO的重要原因之一。 ,此反应为放热反应。在一定温度下,10L某密闭容器中发生上述反应,各物质的物质的量的变化情况如下表
,此反应为放热反应。在一定温度下,10L某密闭容器中发生上述反应,各物质的物质的量的变化情况如下表
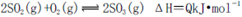 向右移动
向右移动
 向右移动
向右移动 向右移动
向右移动