网址:http://m.1010jiajiao.com/timu_id_573570[举报]
1、B 2、D 3、B 4、C 5、D 6.D 7.D 8.A 9.B 10.A 11.A 12.B 13.D
14、C 15、ACD 16、B 17、C 18、A 19、D 20、A 21、CD
22. (1)C ; 0.600 ;(2)0.92;2.76;7.22;6.78(3)(1)BCE (2)4.3
23.

 2424.
2424.
24.解:当加速电压为U1时电子到达O点速度为
 ,则
,则 =
= ① (2分)
① (2分)
电子在偏转电场时有 ② (2分)
② (2分)
 ③(1分)
③(1分)
当加速电压为U2时电子到达O点速度为
 ,则
,则 ④(2分)
④(2分)
电子刚飞出偏转时偏移量: ⑤(2分)
⑤(2分)  ⑥(1分)
⑥(1分)
如图,由三角形相似有 ⑦ (4分)
⑦ (4分)
所以  (2分)
(2分)  (2分)
(2分)
25.(1)A与B第一次碰前: (2分)
(2分)
A与B第一次碰撞  (2分)
(2分)
 (2分)
(2分)
所以
 (2分)
(2分)
(2)B、C第一次碰撞  所以
所以 即B碰后停下 (2分)
即B碰后停下 (2分)
BC第一次碰前 (2分)
(2分)
此时 (2分)
(2分)
AB第一次碰后到第二次相碰前  (2分)
(2分)
所以 (2分)
(2分)
第二次相碰前 =
= (2分)
(2分)
W= (2分)
(2分)
26.(10分)
⑴ F Al (各2分) ⑵  (3分)
(3分)
⑶ 2Al + 2OH― + 2H2O=2AlO2― + 3H2↑(3分)
27.(20分)
⑴ C D(2分)
⑵ A D(2分)
⑶ 压强更高,所需动力更大,对材料的强度和设备的制造要求也更高。(2分)
⑷ 合成氨反应是可逆反应,实际消耗的N2(或H2)少于10 mol(或30 mol)(2分)
⑸①将注射器取下置于盛水的水槽中,若水进入注射器,气体体积减少,则说明有氨气生成。(2分)
② A B D(2分)
⑹①上述待测氨水 确保氨水的浓度不发生改变(各1分)
② 0.6250 mol/L(2分)
③ A C (1分)
⑺ N2 + 6e―=2N3―(2分)
28.(18分)
⑴  (各2分) ⑵ NaNH2 + NH4Cl=NaCl +
2NH3 (2分)
(各2分) ⑵ NaNH2 + NH4Cl=NaCl +
2NH3 (2分)
⑶ ①②(各2分)
⑷  (3分) ⑸ 4 (2分) ⑹ 1
(2分)
(3分) ⑸ 4 (2分) ⑹ 1
(2分)
⑺ C6H15N3 O 3 + NH3→C6H12N4 + 3H2O(2分)
29.(12分)
⑴ ①②④(2分)
⑵ 羧基 碳碳双键(各2分)
⑶ (CH3)2 CHCH
⑷(CH3)2 CHCH2 O H+ HC O O H→(CH3)3 CC O O H +H2 O(2分)
30.(22分)
⑴CO2(2分)
⑵B处O2多于D处,D处CO2多于B处(2分)
⑶减少(2分) 增加(2分) 上升(2分)
⑷装置中CO2量越来越少,暗反应下降,导致ATP和NADPH积累,进而使光反应下降。(2分) 乳酸(2分)
⑸15NH3→氨基酸及蛋白质(或含15N的有机物)(2分)根瘤菌、大豆(2分)脱氨基(2分)
肝脏(1分) 尿素(1分)
Ⅱ.(8分)
⑴细胞核(1分) 蒸馏水(1分) 不同浓度的NaCl溶液(1分)
⑵核糖体、线粒体(2分)
⑶胰岛素(1分)
 ⑷骨髓中的造血干细胞
抗体(2分)
⑷骨髓中的造血干细胞
抗体(2分)
⑸⑼答案见右图。(2分)注:①缺少细胞膜、中心体、纺锤体或染色体数目不符等错误均不得分。②姐妹染色体形态应一致,每一条染色体的“两臂”应“甩向”赤道板,否则不得分。右图的“美观性”不作要求。
31.(12分)
⑴①实验前要先测定甲、乙鼠的体温 ②实验要有重复性,仅用两只小白鼠进行实验有一定的偶然性。③增加丙组与甲鼠处理方法相同但不破坏下丘脑。
⑵赞同。先做不破坏下丘脑的实验,再做破坏下丘脑后的实验,进行自身前后对照(2分)
⑶BD AC (2分,缺一不给分)
⑷甲状腺激素和肾上腺素(2分,缺一不给分)

在烷烃分子中的基团:-CH3、-CH2-、![]() 中的碳原子分别为伯、仲、叔、季碳原子,数目分别用n1、n2、n3、n4表示,如
中的碳原子分别为伯、仲、叔、季碳原子,数目分别用n1、n2、n3、n4表示,如 ,分子中n1=6,n2=1,n3=2,n4=1.相应的碳原子上的氢分别用伯氢、仲氢、叔氢加以区别,如下面所示:
,分子中n1=6,n2=1,n3=2,n4=1.相应的碳原子上的氢分别用伯氢、仲氢、叔氢加以区别,如下面所示:

(1)四种碳原子数之间的关系为n1=________.
(2)如果某烷烃分子中间时存在这四种基团,最少应为含有________个碳原子的烷烃,其结构简式有________种,它们分别是________.
(3)在烷烃的取代反应中,伯、仲、叔三种氢原子被取代的几率(机会)不同,但同类氢原子被取代的几率(机会)可视为相同.现将n mol 2-甲基丁烷(![]() )与适量溴代物和________mol HBr.若在上述溴的取代反应中,伯、仲、叔氢原子被溴原子取代的几率比为a∶b∶c,则生成的4种一溴代物中
)与适量溴代物和________mol HBr.若在上述溴的取代反应中,伯、仲、叔氢原子被溴原子取代的几率比为a∶b∶c,则生成的4种一溴代物中![]() Br所占的物质的量分数为________.
Br所占的物质的量分数为________.
只含碳、氢、氧的有机物,为便于研究其燃烧时,生成物与所需氧气的量的关系,可用通式(CxHy)m(H2O)n或(CxOy)m(H2O)n表示它们.(m、n、x、y均为正整数)
例如:CH3OH、C2H5OH、C3H7OH等物质可用通式(CH2)m(H2O)n表示,其m分别为1,2,3,n均为1.它们燃烧时所需的氧气和生成的二氧化碳的体积比均为3∶2.
(1)现有一类只含C、H、O的有机物.它们燃烧时所需消耗的氧气和生成的二氧化碳的体积比为5∶4(相同状况),按照上述要求,该类化合物的通式可表示为________
(2)写出这类化合物分子量最小的物质的结构简式________.
(3)写出这类化合物中生成CO2与H2O的物质的量之比为1∶1,且能发生水解反应的物质的分子式________,该物质能发生水解的同分异构体有________种.
(4)若某一类有机物可用通式(CxOy)m(H2O)n表示,则在相同的条件下,该类化合物完全燃烧时消耗的氧气体积为V1和生成的CO2体积为V2,则V1、V2必须满足的条件是________.
(5)现有一种有机物,它完全燃烧时,消耗氧气与生成CO2的体积比为3∶4,它具有两个羧基,其余的碳原子与相同的原子或原子团结合,取0.2625 g该化合物恰好能与2500 ml 0.1000 mol·L-1的NaOH完全中和,由此可知该化合物的分
子式应是________结构简式为________.
只含碳、氢、氧的有机物,为便于研究其燃烧时,生成物与所需氧气的量的关系,可用通式(CxHy)m(H2O)n或(CxOy)m(H2O)n表示它们.(m、n、x、y均为正整数)
例如:CH3OH、C2H5OH、C3H7OH等物质可用通式(CH2)m(H2O)n表示,其m分别为1,2,3,n均为1.它们燃烧时所需的氧气和生成的二氧化碳的体积比均为3∶2.
(1)现有一类只含C、H、O的有机物.它们燃烧时所需消耗的氧气和生成的二氧化碳的体积比为5∶4(相同状况),按照上述要求,该类化合物的通式可表示为________
(2)写出这类化合物分子量最小的物质的结构简式________.
(3)写出这类化合物中生成CO2与H2O的物质的量之比为1∶1,且能发生水解反应的物质的分子式________,该物质能发生水解的同分异构体有________种.
(4)若某一类有机物可用通式(CxOy)m(H2O)n表示,则在相同的条件下,该类化合物完全燃烧时消耗的氧气体积为V1和生成的CO2体积为V2,则V1、V2必须满足的条件是________.
(5)现有一种有机物,它完全燃烧时,消耗氧气与生成CO2的体积比为3∶4,它具有两个羧基,其余的碳原子与相同的原子或原子团结合,取0.2625 g该化合物恰好能与2500 ml 0.10 00 mol·L-1的NaOH完全中和,由此可知该化合物的分子式应是________结构简式为________.
(1)在当代人们的生活中,你所知道的利用太阳能辐射加热物体的方式有______(任举三例).
(2)在生物质能的利用过程中,可以制得重要的有机物乙醇.某校化学课外兴趣小组的学生为了验证乙醇的分子结构,设计如下实验程序:乙醇的组成元素的确定、分子式的确定、分子结构的确定.
(Ⅰ)他们决定用分析乙醇燃烧的产物来确定乙醇中含有C、H两种元素,简要说明他们的实验操作方法和现象:
①证明含有氢元素的实验操作方法和现象是______.
②证明含有碳元素的实验操作方法和现象是______.
(Ⅱ)用分析燃烧产物来证实乙醇中还含有氧元素时,需要取得一些实验数据,这些数据应该是______.
实验中他们可能会用到下列装置,请你将必需的相关装置的序号按从左到右排出合理的顺序(→表示气体的流向):______.

(Ⅲ)为确定乙醇的分子式,除(Ⅱ)中需要取得的数据外,你认为还是否需要测定乙醇的相对分子质量呢?______.
(Ⅳ)为确定乙醇的分子结构,他们先测定一定量无水乙醇和金属钠反应生成氢气的体积,选用了如下图所示的仪器装置(有的仪器配有双孔橡皮塞).则
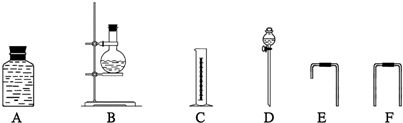
①这些仪器装置的合理的连接顺序是______接______接______接______接______接______(填代表各部分仪器装置的大写字母).
②由实验证明乙醇的分子结构是CH3CH2OH而不是CH3OCH3的理由是
______.
(3)开发新能源以缓解石油等的短缺引起的能源危机是一个重要课题.据报道,某地近年建设了一个年生产工业酒精500万吨的工厂,目的是为了将工业酒精与汽油混合作为汽车燃料而减少汽油的消耗量.已知生产酒精的方法有如下三种(用化学方程式表示):
方法一:CH2=CH2+H2O
| ||
| △ |
方法二:CH3-CH2Br+H2O
| ||
| △ |
方法三:(C6H10O5)n(淀粉)+n H2O
| 淀粉酶 |
C6H12O6(葡萄糖)
| 酒化酶 |
综合地看,你认为这三种方法中,较好的是______(填字母),理由是______.
A.方法一 B.方法二 C.方法三
你认为该工厂生产工业酒精用的是______(填“方法一”、“方法二”或“方法三”)而不是另外的两种方法的原因是_______.
(1)在当代人们的生活中,你所知道的利用太阳能辐射加热物体的方式有______(任举三例).
(2)在生物质能的利用过程中,可以制得重要的有机物乙醇.某校化学课外兴趣小组的学生为了验证乙醇的分子结构,设计如下实验程序:乙醇的组成元素的确定、分子式的确定、分子结构的确定.
(Ⅰ)他们决定用分析乙醇燃烧的产物来确定乙醇中含有C、H两种元素,简要说明他们的实验操作方法和现象:
①证明含有氢元素的实验操作方法和现象是______.
②证明含有碳元素的实验操作方法和现象是______.
(Ⅱ)用分析燃烧产物来证实乙醇中还含有氧元素时,需要取得一些实验数据,这些数据应该是______.
实验中他们可能会用到下列装置,请你将必需的相关装置的序号按从左到右排出合理的顺序(→表示气体的流向):______.

(Ⅲ)为确定乙醇的分子式,除(Ⅱ)中需要取得的数据外,你认为还是否需要测定乙醇的相对分子质量呢?______.
(Ⅳ)为确定乙醇的分子结构,他们先测定一定量无水乙醇和金属钠反应生成氢气的体积,选用了如下图所示的仪器装置(有的仪器配有双孔橡皮塞).则

①这些仪器装置的合理的连接顺序是______接______接______接______接______接______(填代表各部分仪器装置的大写字母).
②由实验证明乙醇的分子结构是CH3CH2OH而不是CH3OCH3的理由是
______.
(3)开发新能源以缓解石油等的短缺引起的能源危机是一个重要课题.据报道,某地近年建设了一个年生产工业酒精500万吨的工厂,目的是为了将工业酒精与汽油混合作为汽车燃料而减少汽油的消耗量.已知生产酒精的方法有如下三种(用化学方程式表示):
方法一:CH2=CH2+H2O
 CH3CH2OH
CH3CH2OH方法二:CH3-CH2Br+H2O
 CH3CH2OH+HBr
CH3CH2OH+HBr方法三:(C6H10O5)n(淀粉)+n H2O
 n C6H12O6(葡萄糖)
n C6H12O6(葡萄糖)C6H12O6(葡萄糖)
 2C2H5OH+2CO2↑
2C2H5OH+2CO2↑综合地看,你认为这三种方法中,较好的是______(填字母),理由是______.
A.方法一 B.方法二 C.方法三
你认为该工厂生产工业酒精用的是______(填“方法一”、“方法二”或“方法三”)而不是另外的两种方法的原因是_______.
查看习题详情和答案>>