摘要:18.A.B.C.D.E.F均为短周期元素.原子序数依次增大.A元素原子核内无中子.B元素原子核外最外层电子数是次外层电子数的2倍.C元素是地壳里含量最多的元素.D是短周期元素中金属性最强的元素.E与D元素的质子数之和为27.最外层电子数之差为5.F元素的最高价氧化物的水化物为最强酸.(1)推断B元素在元素周期表中的位置:第 周期 族.(2)画出F元素的原子结构示意图: (3)A.E元素形成化合物.其电子式为: (4)写出A与C元素形成10电子的一种微粒的化学式: (5)C.D元素可形成淡黄色的粉末.B.C元素可形成由极性键构成的非极性分子.则两化合物之间发生反应的化学方程式为
网址:http://m.1010jiajiao.com/timu_id_565531[举报]
一、选择题(本题包括5小题,每小题2分,共10分。)
题号
1
2
3
4
5
答案
C
B
D
A
B
二、选择题(本题包括12小题,每小题3分,共36分。)
题号
6
7
8
9
10
11
答案
C
A
C
A
D
B
题号
12
13
14
15
16
17
答案
A
B
D
B
C
B
三、填空题(本题包括5小题,共33分。)
18.(7分)
(1 ) 二(1分)ⅣA (1分)
(2) (1分)
(1分)
(3) (1分)
(1分)
(4)H2O 或 H3O+ 或 OH-(1分)
(5 ) 2 Na2O2 +2 CO2 == 2 Na2CO3 + O2 (2分)
19.(4分)
(1)④?②?③?① (2分)
(2)c (Na+)=c (Cl-) > c (OH-) > c (NH4+)> c (H+) (2分)
20.(10分)
(1)FeCl 3 (1分) HCl (1分)
(2)③⑥ (1分)(缺少或答错都无分)
 (3)Fe3++3SCN-=Fe(SCN)3;(2分) (其它合理系数给分,写成“ ” 不扣分)
(3)Fe3++3SCN-=Fe(SCN)3;(2分) (其它合理系数给分,写成“ ” 不扣分)
 (3)
(3)  Mn2++C12↑+2H2O
(2分)
Mn2++C12↑+2H2O
(2分)  HCO3-+OH-
HCO3-+OH-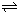 C2D4(g);△H<0.在恒温恒容条件下,将一定量CD2和C2D4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
C2D4(g);△H<0.在恒温恒容条件下,将一定量CD2和C2D4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.