网址:http://m.1010jiajiao.com/timu_id_560266[举报]
第Ⅰ卷(选择题共74分)
一.二选择题:
题号
1
2
3
4
5
6
7
8
答案
C
D
A
B
C
B
B
C
题号
9
10
11
12
13
14
15
16
17
18
答案
C
AC
BC
C
B
D
D
C
B、C
C
第Ⅱ卷(选择题共76分)
19.(1)AEF (2)AB (3)AF(或AE) (4)D
(5)安全瓶防止碱液倒吸 (2分×5)
20.(1)C(1分), B (1分)
(2)B(1分) 负极:2Cu-4e- =2Cu2+ (2分) 正极:2H2O+O2+4e- ==4OH-(2分)
21.离子方程式(略)(1)、(3);(1)中F-还原性很弱,不能使Fe3+还原为Fe2+;
(3)中F-不与SCN-反应,SCN-没有被消耗,所以当再加入足量的FeCl3溶液时,溶液又呈血红色。 (2分×3)
22.(1)弱电解质
(2)H5IO6
5 H5IO6 + 2Mn2+ = 11 H+ +2 MnO4― + 5 IO3― + 7 H2O (2分×3)
23.(1)山坡上;(2)碳酸钠溶液或碳酸氢钠溶液浸湿毛巾;
(3)肥皂水(或洗衣粉)浸湿毛巾;
(4)氢氧化钠溶液或者氢氧化钙溶液;
(5)浓氨水。(2分×5)[其它合理答案也可]
24.(1)A:H2S D:H2SO4 2H2S+3O2 == 2SO2+2H2O;
(2)A:NH3 4NH3+5O2 == 4NO + 6H2O
(3)三、ⅠA族、略
(4)S 2SO2+O2 2SO3;C(略); N2 2NO+O2==2NO2
2SO3;C(略); N2 2NO+O2==2NO2
[(1)、(2)方程式2分,其它各1分,以上条件略写出,但评分时要斟情扣分]
25.(1)NH4Cl ,①;(2)NH4Cl 和NH3?H2O(过量), NH4Cl 和HCl(过量)
(3)小于 ,大于 (1分×6)
26.解答:(1)AB (2分)(2)除去过量的铁屑(1分)(3) Fe2(SO4)3 ;废铁屑中含有氧化生成Fe2O3(或Fe3O4)被H2SO4溶解生成Fe2(SO4)3。FeSO4被空气氧化生成Fe2(SO4)3;取少许滤液,加KSCN溶液,观察溶液是否变血红色。(3分)
(4)解法一:若反应后得到的FeSO4在
x= ==34.17(mL)<50mL
==34.17(mL)<50mL
所以,蒸发后溶液尚未饱和. (3分)
解法二:若该溶液是饱和的,则其所含的 FeSO4溶质的质量为y 则
y==50×1.36× ==22.24(g)
==22.24(g)
按题意 H2SO4完全反应得到的 FeSO4的质量为:
0.5 × 200 ×10-3 ×152 =15.2
因
(5)C;(4)中求证
(
(6)(3分)解法一:
①(5)中所给
50.0ml ×
②设析出的FeSO4?7H2O的质量为X,则可列出
 =
= x=
x=
解法二:
 ×100%=17.0%
×100%=17.0%
则(50.0×1.30-x)× +
x×
+
x× =15.2
=15.2
x=11.0 (g)
海水淡化可采用膜分离技术,如图所示,对渗透膜右侧的海水加压,水分子可以通过渗透膜进入左侧淡化池,而海水中的各种离子不能通过渗透膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是( )

A.溶质的质量增加
B.溶剂的质量减少
C.溶液的质量不变
D.以上三种情况都有可能
查看习题详情和答案>>
(1)E的核外电子排布式是______,A、B、C、D的第一电离能由小到大的顺序为______.
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是______;
(3)A的最高价含氧酸根离子中,其中心原子采取______杂化,D的低价氧化物分子的空间构型是______.
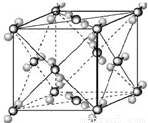
(4)A、E形成某种化合物的晶胞结构如下图所示,则其化学式为______;(每个球均表示1个原子)

(1)E的核外电子排布式是______,A、B、C、D的第一电离能由小到大的顺序为______.
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是______;
(3)A的最高价含氧酸根离子中,其中心原子采取______杂化,D的低价氧化物分子的空间构型是______.
(4)A、E形成某种化合物的晶胞结构如下图所示,则其化学式为______;(每个球均表示1个原子)
 查看习题详情和答案>>
查看习题详情和答案>>
试回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)基态Ga原子的核外电子排布式为______.
(2)A、B、C的第一电离能由大到小的顺序为______.
(3)B元素的单质分子中有______个π键,与其互为等电子体的物质的化学式可能为______(任写一种).
(4)上述A的氧化物分子的中心原子采取______杂化,其晶胞中微粒间的作用力为______.
(5)EH3分子的空间构型为______,其沸点与BH3相比______(填“高”或“低”),原因是______.
(6)向CuSO4溶液中逐滴加入BH3的水溶液,得到深蓝色的透明溶液.请写出该反应的离子方程式______.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)判断反应达到平衡状态的依据是(填字母序号,下同)
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的相对平均分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
(2)如表所列数据是反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为
(3)要提高CO的转化率,可以采取的措施是
a.升温b.加入催化剂c.增加CO的浓度
d.加入H2加压e.加入惰性气体加压f.分离出甲醇
(4)一定条件下,CO与H2在催化剂的作用下生成5molCH3OH的能量变化为454kJ.在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO、2molH2 | 1molCH3OH | 2molCH3OH | |
| 平衡时数据 | CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | akJ | bkJ | ckJ | |
| 体系压强(Pa) | p1 | p2 | p3 | |
| 反应物转化率 | α1 | α2 | α3 | |
A.2c1>c3B.a+b<90.8C.2p2<p3D.α1+α3<1.