摘要:据2K2Cr2O7-3 O2 可知.废水中化学耗氧量m(O2)= (0.1667mmol×1.5×32g/mol)÷0.1000L=80.0mg/L 八.
网址:http://m.1010jiajiao.com/timu_id_555514[举报]
![]() 水是生命之源,2005年12月发生在我省的北江水污染事件再次提醒人们保护水资源的必要性和紧迫性。
水是生命之源,2005年12月发生在我省的北江水污染事件再次提醒人们保护水资源的必要性和紧迫性。
![]() (1)据报道,北江水污染事件是由于某冶炼厂设备检修期间排放的废水所致,推测其主要污染物是 。如果有害废水已经在河流中扩散,为了尽量减少危害,对河水的处理应该采取的措施是
(1)据报道,北江水污染事件是由于某冶炼厂设备检修期间排放的废水所致,推测其主要污染物是 。如果有害废水已经在河流中扩散,为了尽量减少危害,对河水的处理应该采取的措施是
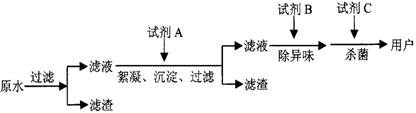
![]() (2)自来水的生产流程如图,其中的试剂A、B、C分别可以选择 、 、 。
(2)自来水的生产流程如图,其中的试剂A、B、C分别可以选择 、 、 。
(3)电镀厂排放的废水中含铬(以Cr2O72-形式存在),常用电解的方法处理。电解时,以铁为阳极,生成的Fe2+将Cr2O72-还原为Cr3+,产物再与电解时生成的OH-形成氢氧化物沉淀而除去。
①两个电极上发生的反应分别为:阳极 ,阴极 。
②溶液中发生的总反应为(用离子方程式表示) 。
(4)化学需氧量(COD)是水体质量的控制项目这一,它是量废水中还原性污染物的重要指标。COD是指用强氧化剂(我国采用K2Cr2O7)处理一定量水样时消耗的氧化剂的量,并换算成以O2作为氧化剂时,1L水样所消耗O2的质量(mg?L-1)。现取某池塘水样20.00mL,反应消耗10.00mL0.0400mol?L-1K2Cr2O7溶液(反应后转化为Cr3+)。该水样的COD为 mg?L-1。
查看习题详情和答案>> (2011?湖南二模)(1)已知可逆反应:M(g)+N(g)
(2011?湖南二模)(1)已知可逆反应:M(g)+N(g) P(g)+Q(g);△H>0,请回答下列问题:
P(g)+Q(g);△H>0,请回答下列问题:①在某温度下,反应物的起始浓度分别为:c(M)=1mol?L-1,c(N)=2.4mol?L-1,达到平衡后,M的转化率为60%,此时N的转化率为
25%
25%
.此反应的化学平衡常数K=0.5
0.5
.②若反应温度不变,反应物的起始浓度分别为:c(M)=4mol?L-1,c(N)=amol?L-1;达到平衡后,c(P)=2mol?L-1’a=
6
6
mol?L-1.(2)随着科学技术的进步,人们研制出了多种类型的甲醇质子交换膜燃料电池,以满足不同的需求.
①有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是:
A.CH3OH(g)+H2O(g)═CO2(g)+3H2(g);△H=+49.0kJ/mol
B.CH3OH(g)+3/O2(g)═CO2(g)+2H2O(g);△H=-676.7kJ/mol
由上述方程式可知,CH3OH的燃烧热
大于
大于
(填“大于”、“等于”或“小于”)676.7kJ/mol.已知水的气化热为44kJ/mol则氢气燃烧的热化学方程式为H2(g)+
O2(g)═H2O(l);△H=-285.9kJ/mol
| 1 |
| 2 |
H2(g)+
O2(g)═H2O(l);△H=-285.9kJ/mol
| 1 |
| 2 |
②图是某笔记本电脑用甲醇质子交换膜燃料电池的结构示意图.甲醇在催化剂作用下提供质子和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH3OH(g)+3O2═2CO2+4H2O.则c电极是
负极
负极
(填“正极”或“负极”),c电极上发生的电极反应是CH3OH-6e-=CO2+6H+
CH3OH-6e-=CO2+6H+
.金属单质及其化合物与工农业生产、日常生活有密切的联系.请回答下列问题:
(1)一定温度下,氧化铁可以与一氧化碳发生如下反应:
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g),△H=QkJ?mol-1
①该反应的平衡常数表达式K= ;
②该温度时,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,5min后,生成了单质铁11.2g,则这段时间内CO的反应速率为 ;
③达平衡后,若温度升高
的值增大,则Q 0(填“>”、“=”、“<”).
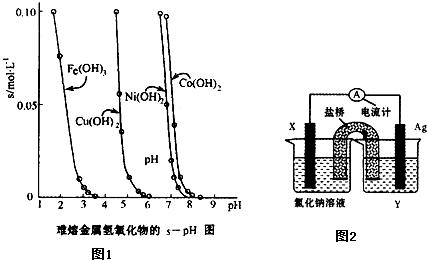
(2)工业常根据金属氢氧化物在酸中溶解度不同,通过控制溶液的pH,达到分离金属离子的目的.如图1是难溶金属的氢氧化物在不同pH下的溶解情况(s/mol?L-1).若要除去CuCl2溶液的少量Fe3+,应控制溶液的pH为 (填序号).
A.小于1 B.4左右 C.大于6 D.大于9
(3)某工业废水中含有Cu2+、Pb2+、Hg2+,若向工业废水中加入过量的FeS,当FeS、CuS、PbS和HgS共存时,溶液中c(Fe2+):c(Pb2+):c(Hg2+)= : : .已知:Ksp(FeS)=6.3×10-18mol2?L-2,Ksp(PbS)=3.4×10-28mol2?L-2Ksp(CuS)=1.3×10-36mol2?L-2,Ksp(HgS)=6.4×10-53mol2?L-2
(4)依据氧化还原反应:Cu2+(aq)+Fe(s)═Fe2+(aq)+Cu(s)设计成如图2所示的原电池,则关于该电池装置的说法中不正确的是 (填序号).
A.电极X的材料是Fe
B.电解质溶液Y是AgNO3溶液
C.原电池工作时,盐桥中的阴离子不断移向左池的氯化钠溶液中
D.原电池工作时,x电极反应为:O2+2H2O+4e-→4OH-.
查看习题详情和答案>>

(1)一定温度下,氧化铁可以与一氧化碳发生如下反应:
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g),△H=QkJ?mol-1
①该反应的平衡常数表达式K=
②该温度时,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,5min后,生成了单质铁11.2g,则这段时间内CO的反应速率为
③达平衡后,若温度升高
| [CO] | [CO2] |
(2)工业常根据金属氢氧化物在酸中溶解度不同,通过控制溶液的pH,达到分离金属离子的目的.如图1是难溶金属的氢氧化物在不同pH下的溶解情况(s/mol?L-1).若要除去CuCl2溶液的少量Fe3+,应控制溶液的pH为
A.小于1 B.4左右 C.大于6 D.大于9
(3)某工业废水中含有Cu2+、Pb2+、Hg2+,若向工业废水中加入过量的FeS,当FeS、CuS、PbS和HgS共存时,溶液中c(Fe2+):c(Pb2+):c(Hg2+)=
(4)依据氧化还原反应:Cu2+(aq)+Fe(s)═Fe2+(aq)+Cu(s)设计成如图2所示的原电池,则关于该电池装置的说法中不正确的是
A.电极X的材料是Fe
B.电解质溶液Y是AgNO3溶液
C.原电池工作时,盐桥中的阴离子不断移向左池的氯化钠溶液中
D.原电池工作时,x电极反应为:O2+2H2O+4e-→4OH-.
 下面是中学化学中常用玻璃仪器组成的实验装置图(根据需要可在其中加入液体或固体).
下面是中学化学中常用玻璃仪器组成的实验装置图(根据需要可在其中加入液体或固体).请回答下列问题:
(1)能用作干燥氨气的装置有
D、E
D、E
(填字母);(2)既能用于收集氯气又能用于收集一氧化氮气体的装置有
B
B
(填字母);(3)在氯气和铁反应实验中,能添加在制氯气和反应装置之间以除去氯气中氯化氢等杂质气体的装置有
A
A
(填字母);(4)能用于乙烯与溴水反应制二溴乙烷的实验装置有
A
A
(填字母);(5)若用C装置作二氧化硫与烧杯中氢氧化钠溶液反应的实验,则其中广口瓶的作用是
防止倒吸
防止倒吸
.(6)为比较Fe3+和Cu2+对H2O2分解的催化效果,某同学设计了下图所示的实验.

①可通过观察
根据2H2O2
2H2O+O2↑可知以生成气体的快慢来判断反应的快慢
| ||
根据2H2O2
2H2O+O2↑可知以生成气体的快慢来判断反应的快慢
现象来定性比较得出结论.
| ||
②有同学提出将CuSO4改为CuCl2更为合理,其理由是
由于CuSO4、FeCl3中的阴离子不同,不能排除阴离子的因素
由于CuSO4、FeCl3中的阴离子不同,不能排除阴离子的因素
,你认为还可以作何改进?将FeCl3改为Fe2(SO4)3
将FeCl3改为Fe2(SO4)3
﹒