摘要:⑵① 1 Cr2O72-+ 6Fe2++ 14 H+ 2Cr3++ 6 Fe3++ 7H2O ② 分析实验数据记录表.第一次实验数据有误.故剔除这一数据.
网址:http://m.1010jiajiao.com/timu_id_555511[举报]
(2010?朝阳区模拟)根据废水中所含有害物质的不同,工业上有多种废水的处理方法.
(1)①废水I若采用CO2处理,离子方程式是
②废水Ⅱ常用明矾处理.实践中发现废水中的c(HCO-3)越大,净水效果越好,这是因为
③废水Ⅲ中的汞元素存在如下转化(在空格上填相应的化学式):Hg2++
我国规定,Hg2+的排放标准不能超过0.05mg/L.若某工厂排放的废水1L中含Hg2+3×10-7mol,是否达到了排放标准
④废水Ⅳ常用Cl2氧化CN-成CO2和N2,若参加反应的Cl2与CN-的物质的量之比为5:2,则该反应的离子方程式为
(2)化学需氧量(COD)可量度水体受有机物污染的程度,它是指在一定条件下,用强氧化剂处理水样时所消耗的氧化刹的量,换算成氧的含量(以mg/L计).某研究性学习小组测定某水样的化学需氧量(COD),过程如下:
Ⅰ.取V1 mL水样于锥形瓶,加入10.00mL 0.2500mol/L K2Cr2O7溶液.
Ⅱ.加碎瓷片少许,然后慢慢加入硫酸酸化,混合均匀,加热.
Ⅲ.反应完毕后,冷却,加指示剂,用c mol/L的硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液 滴定.终点时消耗硫酸亚铁铵溶液V2 mL.
①I中,量取K2Cr207,溶液的仪器是
②Ⅱ中,碎瓷片的作用是
③Ⅲ中,发生的反应为:Cr2O72-+6Fe2++14H+═2Cr3++6Fe3+7H2O由此可知,该水样的化学需氧量COD=
(用含c、V1、V2的表达式表示).
查看习题详情和答案>>

(1)①废水I若采用CO2处理,离子方程式是
OH-+CO2=HCO3-
OH-+CO2=HCO3-
.②废水Ⅱ常用明矾处理.实践中发现废水中的c(HCO-3)越大,净水效果越好,这是因为
HCO3-会促进Al3+的水解,生成更多的Al(OH)3,净水效果增强
HCO3-会促进Al3+的水解,生成更多的Al(OH)3,净水效果增强
.③废水Ⅲ中的汞元素存在如下转化(在空格上填相应的化学式):Hg2++
CH4
CH4
═CH3Hg++H+我国规定,Hg2+的排放标准不能超过0.05mg/L.若某工厂排放的废水1L中含Hg2+3×10-7mol,是否达到了排放标准
否
否
(填“是”或“否”).④废水Ⅳ常用Cl2氧化CN-成CO2和N2,若参加反应的Cl2与CN-的物质的量之比为5:2,则该反应的离子方程式为
5Cl2+2CN-+4H2O=10Cl-+2CO2+N2+8H+
5Cl2+2CN-+4H2O=10Cl-+2CO2+N2+8H+
.(2)化学需氧量(COD)可量度水体受有机物污染的程度,它是指在一定条件下,用强氧化剂处理水样时所消耗的氧化刹的量,换算成氧的含量(以mg/L计).某研究性学习小组测定某水样的化学需氧量(COD),过程如下:
Ⅰ.取V1 mL水样于锥形瓶,加入10.00mL 0.2500mol/L K2Cr2O7溶液.
Ⅱ.加碎瓷片少许,然后慢慢加入硫酸酸化,混合均匀,加热.
Ⅲ.反应完毕后,冷却,加指示剂,用c mol/L的硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液 滴定.终点时消耗硫酸亚铁铵溶液V2 mL.
①I中,量取K2Cr207,溶液的仪器是
酸式滴定管(或移液管)
酸式滴定管(或移液管)
.②Ⅱ中,碎瓷片的作用是
防止暴沸
防止暴沸
.③Ⅲ中,发生的反应为:Cr2O72-+6Fe2++14H+═2Cr3++6Fe3+7H2O由此可知,该水样的化学需氧量COD=
| 8000×(15-cV2) |
| V1 |
| 8000×(15-cV2) |
| V1 |
硫酸是一种重要的化学试剂.某实验小组的同学利用浓硫酸进行如下实验.请按要求回答下列问题.
I.制取二氧化疏并探究其性质
(1)装置A中发生反应的化学方程式为 .上述装置中适于收集二氧化硫气体的是(填字母) .
(2)将一收集满二氧化硫气体的小试管倒置于滴有紫色石蕊溶液的水中,可观察到的现象是 .
(3)上述实验所产生的二氧化硫尾气可选用E装置来吸收,该反应的化学方程式为 .
Ⅱ.处理含正六价铬的废水样液(+6价Cr的含量为78mg/L).实验步骤如下:
①取1L废水加入一定量1.8mol/LH2SO4溶液使样液酸化
②加入一定量的绿矾(FeSO4?7H2O),将正六价铬转化为正三价铬离子
③加入过量的石灰水,使正三价铬离子转化为Cr(OH)3沉淀
④过滤,除去沉淀物
(1)配制步骤①中所需H2SO4溶液100mL,需用18mol/L H2SO4溶液的体积是 mL.
(2)步骤②中反应的离子方程式为14H++Cr2O72-+6Fe2+═2Cr3++6Fe3++7H2O此反应中氧化剂和还原剂物质的量之比为 .
(3)步骤④分离出的沉淀物中含有Cr(OH)3、CaSO4和 .
(4)处理1L该废水样液至少需要绿矾 g.
查看习题详情和答案>>

I.制取二氧化疏并探究其性质
(1)装置A中发生反应的化学方程式为
(2)将一收集满二氧化硫气体的小试管倒置于滴有紫色石蕊溶液的水中,可观察到的现象是
(3)上述实验所产生的二氧化硫尾气可选用E装置来吸收,该反应的化学方程式为
Ⅱ.处理含正六价铬的废水样液(+6价Cr的含量为78mg/L).实验步骤如下:
①取1L废水加入一定量1.8mol/LH2SO4溶液使样液酸化
②加入一定量的绿矾(FeSO4?7H2O),将正六价铬转化为正三价铬离子
③加入过量的石灰水,使正三价铬离子转化为Cr(OH)3沉淀
④过滤,除去沉淀物
(1)配制步骤①中所需H2SO4溶液100mL,需用18mol/L H2SO4溶液的体积是
(2)步骤②中反应的离子方程式为14H++Cr2O72-+6Fe2+═2Cr3++6Fe3++7H2O此反应中氧化剂和还原剂物质的量之比为
(3)步骤④分离出的沉淀物中含有Cr(OH)3、CaSO4和
(4)处理1L该废水样液至少需要绿矾
欲降低废水中重金属元素铬的毒性,可将Cr2O72-转化为Cr(OH)3沉淀除去.已知:
(1)某含铬废水处理的主要流程如图所示: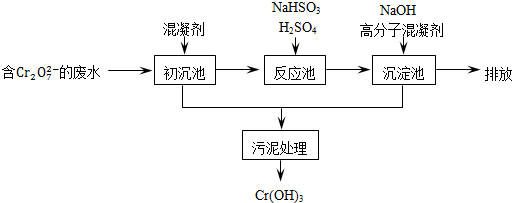
①初沉池中加入的混凝剂是K2SO4﹒Al2(SO4)3﹒24H2O,用离子方程式表示其反应原理是
②反应池中发生主要反应的离子方程式是Cr2O72-+3HSO3-+5H+═2Cr3++3SO42-+4H2O.根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是
(2)工业可用电解法来处理含 Cr2O72-废水.实验室利用如图模拟处理含Cr2O72-的废水,阳极反应式是Fe-2e-═Fe2+,阴极反应式是2H++2e-═H2↑.Fe2+与酸性溶液中的Cr2O72-反应的离子方程式是
查看习题详情和答案>>
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.2 |
| Cr3+ | 6.0 | 8.0 |

①初沉池中加入的混凝剂是K2SO4﹒Al2(SO4)3﹒24H2O,用离子方程式表示其反应原理是
Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
.②反应池中发生主要反应的离子方程式是Cr2O72-+3HSO3-+5H+═2Cr3++3SO42-+4H2O.根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是
Cr3++3OH-═Cr(OH)3↓、H++OH-═H2O
Cr3++3OH-═Cr(OH)3↓、H++OH-═H2O
.证明Cr3+沉淀完全的方法是测定溶液的pH,若pH≥8,则证明Cr3+沉淀完全
测定溶液的pH,若pH≥8,则证明Cr3+沉淀完全
.
(2)工业可用电解法来处理含 Cr2O72-废水.实验室利用如图模拟处理含Cr2O72-的废水,阳极反应式是Fe-2e-═Fe2+,阴极反应式是2H++2e-═H2↑.Fe2+与酸性溶液中的Cr2O72-反应的离子方程式是
Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O
Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O
,得到的金属阳离子在阴极区可沉淀完全,从水的电离平衡角度解释其原因是阴极反应消耗了水中的H+,打破了水的电离平衡,促进了水的电离,使溶液中OH-浓度增大,溶液的碱性增强
阴极反应消耗了水中的H+,打破了水的电离平衡,促进了水的电离,使溶液中OH-浓度增大,溶液的碱性增强
.用电解法处理该溶液中0.01mol Cr2O72-时,至少得到沉淀的质量是8.48
8.48
g.电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72+6Fe2++14H+═2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去,下列说法不正确的是( )
查看习题详情和答案>>
黄铁矿主要成分是FeS2.某硫酸厂在进行黄铁矿成分测定时,取0.1000g样品在空气中充分灼烧,将生成的SO2气体与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000mol/L的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00mL.
已知:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
(1)接触室中发生反应的化学方程式是
(2)样品中FeS2的质量分数是(假设杂质不参加反应)
(3)每160gSO3气体与H2O化合放出260.6kJ的热量,该反应的热化学方程是
(4)煅烧10t上述黄铁矿,理论上产生SO2的体积(标准状况)为
查看习题详情和答案>>
已知:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
(1)接触室中发生反应的化学方程式是
2SO2+O2
2SO3
| 催化剂 |
2SO2+O2
2SO3
.| 催化剂 |
(2)样品中FeS2的质量分数是(假设杂质不参加反应)
90.00%
90.00%
.(3)每160gSO3气体与H2O化合放出260.6kJ的热量,该反应的热化学方程是
SO3(g)+H2O(l)=H2SO4(l);△H=-130.3kJ/mol
SO3(g)+H2O(l)=H2SO4(l);△H=-130.3kJ/mol
.(4)煅烧10t上述黄铁矿,理论上产生SO2的体积(标准状况)为
3.36×106
3.36×106
L,制得98%的硫酸质量为15
15
t.