摘要:27.将标况下1.12LCO2通入含有2gNaOH的水溶液中.完全反应并得到2L溶液.则对于该溶液表述正确的是 A.c (Na+)=c (HCO3-) + c (CO32-) + c (H2CO3)B.c (Na+) + c (H+) = c (HCO3-) + c (CO32-) +c (OH-)C.HCO3- 的电离程度大于HCO3-的水解程度D.存在的平衡体系有:
网址:http://m.1010jiajiao.com/timu_id_554648[举报]
将标况下2.24LCO2通入150mL 1mol?L-1的NaOH溶液中,下列说法正确的是( )
A.c(Na+)=c(HCO3-)+c(CO32-)
B.c(HCO3-)>c(CO32-)
C.c(HCO3-)=c(CO32-)
D.c(HCO3-)<c(CO32-)
查看习题详情和答案>>
A.c(Na+)=c(HCO3-)+c(CO32-)
B.c(HCO3-)>c(CO32-)
C.c(HCO3-)=c(CO32-)
D.c(HCO3-)<c(CO32-)
查看习题详情和答案>>
将标况下2.24LCO2通入150mL 1mol?L-1的NaOH溶液中,下列说法正确的是( )
查看习题详情和答案>>
| A.c(Na+)=c(HCO3-)+c(CO32-) | B.c(HCO3-)>c(CO32-) |
| C.c(HCO3-)=c(CO32-) | D.c(HCO3-)<c(CO32-) |
(2013?潍坊模拟)明矾石的主要成分是K2SO4?Al2(SO4)3?2Al2O3?6H2O,还含有少量Fe2O3杂质.利用明矾石制备氢氧化铝的流程如下:

(1)焙烧炉中发生反应的化学方程式为2Al2(SO4)3+3S
2Al2O3+9SO2,该反应的氧化剂是
(2)将标况下1.12L炉气通入100mL0.5mol/L NaOH溶液中,得到一种酸性溶液,则该溶液中各种离子浓度由大到小的排列顺序为
(3)孰料溶解时反应的离子方程式为
(4)检验废渣中含有Fe2O3所需的试剂是
(5)母液中溶质主要成分的化学式为
查看习题详情和答案>>

(1)焙烧炉中发生反应的化学方程式为2Al2(SO4)3+3S
| ||
. |
Al2(SO4)3
Al2(SO4)3
,若生成1molAl2O3,则转移的电子数为3.612×1024
3.612×1024
.(2)将标况下1.12L炉气通入100mL0.5mol/L NaOH溶液中,得到一种酸性溶液,则该溶液中各种离子浓度由大到小的排列顺序为
c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)
c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)
.(3)孰料溶解时反应的离子方程式为
Al2O3+2OH-=2AlO2-+H2O
Al2O3+2OH-=2AlO2-+H2O
.(4)检验废渣中含有Fe2O3所需的试剂是
盐酸、KSCN溶液
盐酸、KSCN溶液
.(5)母液中溶质主要成分的化学式为
K2SO4、Na2SO4
K2SO4、Na2SO4
,溶液调节pH后经过滤、洗涤可得Al(OH)3沉淀,证明沉淀已洗涤干净的实验操作和现象是取最后的洗涤液于试管中,滴加BaCl2溶液,若无白色沉淀生成则已洗涤干净
取最后的洗涤液于试管中,滴加BaCl2溶液,若无白色沉淀生成则已洗涤干净
.明矾石的主要成分是K2SO4?Al2(SO4)3?2Al2O3?6H2O,还含有少量Fe2O3杂质.利用明矾石制备氢氧化铝的流程如下:
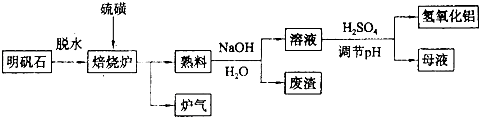
(1)焙烧炉中发生反应的化学方程式为2Al2(SO4)3+3S
2Al2O3+9SO2,该反应的氧化剂是 ,若生成1mol Al2O3,则转移的电子数为 .
(2)将标况下1.12L炉气通入100mL 0.5mol/L NaOH溶液中,得到一种酸性溶液,则该溶液中各种离子浓度由大到小的排列顺序为 .
(3)熟料溶解时反应的离子方程式为 .
(4)检验废渣中含有Fe2O3所需的试剂是 .
(5)母液中溶质主要成分的化学式为 .Al(OH)3是两性氢氧化物,写出Al(OH)3显两性的电离的离子方程式 .
查看习题详情和答案>>

(1)焙烧炉中发生反应的化学方程式为2Al2(SO4)3+3S
| ||
(2)将标况下1.12L炉气通入100mL 0.5mol/L NaOH溶液中,得到一种酸性溶液,则该溶液中各种离子浓度由大到小的排列顺序为
(3)熟料溶解时反应的离子方程式为
(4)检验废渣中含有Fe2O3所需的试剂是
(5)母液中溶质主要成分的化学式为