网址:http://m.1010jiajiao.com/timu_id_543660[举报]
2009年曲靖一中年高考冲刺卷理综(一)
一、选择题
1.D 2.C 3.B 4.D 5.B 6.D 7.A8.D 9.D 10.A 11.B 12.D 13.B
二、选择题
14.A 15.CD 16.B 17.C 18.BC19.CD 20.B 21.B
三、非选择题
22.(18分)
(1)8.0;4.1(每空3分)
(2)①(6分)如下图

②(6分) 分别表示电压表
分别表示电压表 、
、 的读数,
的读数, 表示
表示 内阻
内阻
23.(15分)
(1)小球带负电(2分)
带电小球处于平衡状态,有 ①
① ②
②
(2)小球在竖直平面内沿圆弧摆下,做圆周运动。(或沿圆弧摆下然后沿圆弧来回运动)带电小球到最


低点时速度最大,设小球的最大速度为 小球摆下过程中重力做正功,电场力做负功,由动能定理得
小球摆下过程中重力做正功,电场力做负功,由动能定理得 ③ 联立①③式得
③ 联立①③式得


 24.(19分)
24.(19分)
 (1)摩托车运动员由高台水平飞出由平抛运动规律;
(1)摩托车运动员由高台水平飞出由平抛运动规律;
 水平方向
水平方向 ①
①
 竖直方向
竖直方向 ②
②
 联立式①②得
联立式①②得
 (2)摩托车运动员由坡底冲上高台,根据动能定理
(2)摩托车运动员由坡底冲上高台,根据动能定理

 ③
③
 将
将 代入到式③得
代入到式③得
 (3)从高台水平飞到地面,
由机械能守恒定律
(3)从高台水平飞到地面,
由机械能守恒定律

 ④
④
 解得
解得
 25.(20分)
25.(20分)
 (1)在子弹射入小车的过程中,由子弹、线圈和小车组成的系统动量守恒。有
(1)在子弹射入小车的过程中,由子弹、线圈和小车组成的系统动量守恒。有


 解得子弹的质量
解得子弹的质量
 (2)当
(2)当 时,由图象中可知线圈右边切割磁感线的速度
时,由图象中可知线圈右边切割磁感线的速度 由闭合电路欧姆定律得
由闭合电路欧姆定律得
 线圈中的电流
线圈中的电流
 解得
解得
 (3)由图可知,从
(3)由图可知,从 开始,线圈进入磁场,线圈中有感应电流,受安培力作用,小车做减速运动,速度
开始,线圈进入磁场,线圈中有感应电流,受安培力作用,小车做减速运动,速度 随位移
随位移 减小,当
减小,当 时,线圈完全进入磁场,线圈中感应电流消失,小车做匀速运动,因此线圈长为
时,线圈完全进入磁场,线圈中感应电流消失,小车做匀速运动,因此线圈长为 。
。


 解得
解得
 (4)由图象可知,线圈左边离开磁场时,小车的速度为
(4)由图象可知,线圈左边离开磁场时,小车的速度为 ,线圈进入磁场和离开磁场时,克服安培力做功,线圈的动能减少,转化成电能消耗在线圈上产生电热,
,线圈进入磁场和离开磁场时,克服安培力做功,线圈的动能减少,转化成电能消耗在线圈上产生电热,


 解得线圈电阻发热量
解得线圈电阻发热量
 26.(16分)(1)
26.(16分)(1) (2)
(2) 极性、非极性、直线型
极性、非极性、直线型
 (3)
(3) (4)
(4) ,(5)
,(5)
 27.(18分) (1)①
27.(18分) (1)①
 ②碱石灰(或
②碱石灰(或 或生石灰)
或生石灰)
 ③极易溶于水,水溶液呈碱性 ④B
③极易溶于水,水溶液呈碱性 ④B
 (2)让空气通过灼热的铜网 ①混合
(2)让空气通过灼热的铜网 ①混合 并使其干燥 ②观察导气管口气泡数量,调查气体流量,使
并使其干燥 ②观察导气管口气泡数量,调查气体流量,使 达最佳混合比1:3 将湿润的红色石蕊试纸靠近出气管口,试纸变量,说明气体为
达最佳混合比1:3 将湿润的红色石蕊试纸靠近出气管口,试纸变量,说明气体为 (其他合理答案同样给分)
(其他合理答案同样给分)
(3)
28.(12分) (1)

(2)家成反应 强见的醇溶液、加热

(1)基因突变和交叉互换
(2)
(3)①基因通过控制酶的合成来控制代谢从而控制性状 ②人工合成
(4)①杂交:选择亲本中多对雌雄个体进行杂交 ②测交:选择 中的棕色小香猪与白色小香猪测交,不出现性状分离和即为纯合
中的棕色小香猪与白色小香猪测交,不出现性状分离和即为纯合
(5)调查方案②统计具有该性状小香猪的性别比例
结果:①若表现该隐性性状的个体中,雄性与雌性数量基因相等,则 基因位于常染色体上
基因位于常染色体上
②若表现该隐性性状的个体中,雄性多于雌性。则 基因位于X染色体上
基因位于X染色体上
③若表现该隐性性状的个体全是雄性,则 基因位于
基因位于 染色体。
染色体。
Ⅰ.(1)配制250mL0.1mol/L盐酸溶液需要浓盐酸(密度为1.2g/mL,质量分数为36.5%)的体积为
(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用量筒量取所需的浓盐酸,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(3)配制物质的量浓度的溶液,造成浓度偏高的操作是
A.溶解后的溶液未冷至室温就转入容量瓶中;
B.洗涤烧杯和玻棒的溶液未转入容量瓶中;
C.定容时眼睛俯视刻度线;
D.定容时眼睛仰视刻度线;
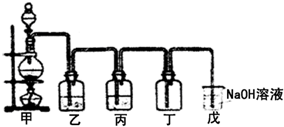
Ⅱ.(1)某学生设计的用该浓盐酸与二氧化锰反应制取并收集干燥纯净的氯气的装置如图:

①写出甲中发生反应的离子方程式:
②乙中盛的试剂是
丙中盛的试剂是
(2)如果将过量二氧化锰与20mL该浓盐酸混合加热,充分反应后理论上可生成标况下的氯气的体积为
①
(3)若将制得的少量氯气通入无色的饱和碘化钾溶液中,溶液变
(4)若将制得的氯气制成饱和氯水,则实验室保存饱和氯水的方法是
实验室用浓盐酸配制250mL0.1mol/L的盐酸溶液:☆
Ⅰ.(1)配制250mL0.1mol/L盐酸溶液需要浓盐酸(密度为1.2g/mL,质量分数为36.5%)的体积为______.
(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)______.
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用量筒量取所需的浓盐酸,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(3)配制物质的量浓度的溶液,造成浓度偏高的操作是______.
A.溶解后的溶液未冷至室温就转入容量瓶中;
B.洗涤烧杯和玻棒的溶液未转入容量瓶中;
C.定容时眼睛俯视刻度线;
D.定容时眼睛仰视刻度线;
Ⅱ.(1)某学生设计的用该浓盐酸与二氧化锰反应制取并收集干燥纯净的氯气的装置如图:
①写出甲中发生反应的离子方程式:______
②乙中盛的试剂是______;作用是______.
丙中盛的试剂是______.
(2)如果将过量二氧化锰与20mL该浓盐酸混合加热,充分反应后理论上可生成标况下的氯气的体积为______mL,而实际值明显少于理论值,其主要原因有:
①______;②______.
(3)若将制得的少量氯气通入无色的饱和碘化钾溶液中,溶液变______色,其离子方程式是______,向所得溶液中加入四氯化碳,振荡后静置,则溶液分为两层,下层是显______色,这种操作叫做______.
(4)若将制得的氯气制成饱和氯水,则实验室保存饱和氯水的方法是______.
查看习题详情和答案>>
Ⅰ.(1)配制250mL0.1mol/L盐酸溶液需要浓盐酸(密度为1.2g/mL,质量分数为36.5%)的体积为______.
(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)______.
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用量筒量取所需的浓盐酸,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(3)配制物质的量浓度的溶液,造成浓度偏高的操作是______.
A.溶解后的溶液未冷至室温就转入容量瓶中;
B.洗涤烧杯和玻棒的溶液未转入容量瓶中;
C.定容时眼睛俯视刻度线;
D.定容时眼睛仰视刻度线;
Ⅱ.(1)某学生设计的用该浓盐酸与二氧化锰反应制取并收集干燥纯净的氯气的装置如图:

①写出甲中发生反应的离子方程式:______
②乙中盛的试剂是______;作用是______.
丙中盛的试剂是______.
(2)如果将过量二氧化锰与20mL该浓盐酸混合加热,充分反应后理论上可生成标况下的氯气的体积为______mL,而实际值明显少于理论值,其主要原因有:
①______;②______.
(3)若将制得的少量氯气通入无色的饱和碘化钾溶液中,溶液变______色,其离子方程式是______,向所得溶液中加入四氯化碳,振荡后静置,则溶液分为两层,下层是显______色,这种操作叫做______.
(4)若将制得的氯气制成饱和氯水,则实验室保存饱和氯水的方法是______.
①实验室装置和所用样品都正确的是(填“甲”、“乙”、“丙”)
②写出实验室制氨气的化学反应方程式
③检验试管里是否收集满了氨气的方法是:
第一种方法是:将一块湿润的
第二种方法是:用玻璃棒沾取浓盐酸或者浓硝酸,放在试管口,如果试管里收集满了氨气,观察到的现象是
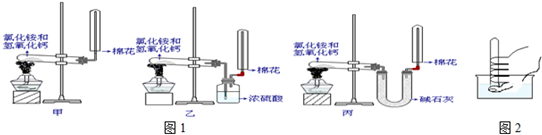
④上述装置中,其中的一个装置肯定收集不到氨气,其原因是(用化学反应方程式表示)
⑤为了检验NH3的某种性质,某同学将盛满NH3的试管移入水槽的水里,放开拇指如图2,观察到的现象是
⑥氨气可被氧气催化氧化,这个反应是工业制硝酸的基础,写出该反应化学方程式
(1)实验室可用甲酸与浓硫酸共热制备一氧化碳:HCOOH浓硫酸========H2O+CO↑,实验的部分装置如下图所示。制备时先加热浓硫酸至80℃—90℃,再逐滴滴入甲酸。


Ⅰ制备CO Ⅱ Ⅲ收集CO
①从下图挑选所需的仪器,画出Ⅰ中所缺的气体发生装置(添加必要的塞子、玻璃管、胶皮管,固定装置不用画),并标明容器中的试剂。





分液漏斗 长颈漏斗 蒸馏烧瓶 集气瓶 温度计
②装置Ⅱ的作用是 。
(2)实验室可用甲酸制备甲酸铜。其方法是先用硫酸铜和碳酸氢钠作用制得碱式碳酸铜,然后再与甲酸斥制得四水甲酸铜[Cu(HCOO)2·4H2O]晶体。相关的化学方程式是:
2CuSO4+4 NaHCO3="=" Cu(OH)2·CuCO3↓+3CO2↑+2Na2SO4+H2O
Cu(OH)2·CuCO3+4HCOOH+ 5H2O="=2" Cu(HCOO)2·4H2O+ CO2↑
实验步骤如下:
Ⅰ、碱式碳酸铜的制备:



③步骤ⅰ是将一定量CuSO4·5H2O晶体和NaHCO3固体一起放到研钵中研磨,其目的是 。
④步骤ⅱ是在搅拌下将固体混合物分多次缓慢加入热水中,反应温度控制在70℃—80℃,如果看到 (填写实验现象),说明温度过高。
Ⅱ、甲酸铜的制备:
将Cu(OH)2·CuCO3固体放入烧杯中,加入一定量热的蒸馏水,再逐滴加入甲酸至碱式碳酸铜恰好全部溶解,趁热过滤除去少量不溶性杂质。在通风橱中蒸发滤液至原体积的1/3时,冷却析出晶体,过滤,再用少量无水乙醇洗涤晶体2—3次,晾干,得到产品。
⑤“趁热过滤”中,必须“趁热”的原因是 。
⑥用乙醇洗涤晶体的目的是 。