摘要:C.5.6 g铁投入浓硫酸中.生成的气体分子数为0.1 NA
网址:http://m.1010jiajiao.com/timu_id_542779[举报]
I.硫酸铜是一种应用极其广泛的化工原料.以下是某工厂用含铁废铜为原料生产胆矾(CuSO4?5H2O)的生产流程示意图: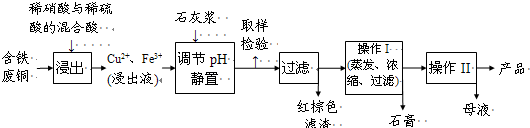
胆矾和石膏在不同温度下的溶解度(g/100g水)见下表.
请回答下列问题:
(1)红棕色滤渣的主要成分是
(2)写出浸出过程中生成硫酸铜的化学方程式
(3)操作I的操作温度应该控制在
(4)从溶液中分离出硫酸铜晶体的操作II应为
(5)取样检验是为了确认Fe3+是否除净.有同学设计了以下两种方案,在实验室分别对所取样品按下列方案进行操作:
方案一:取样于试管→滴加KSCN溶液;
方案二:径向层析→喷KSCN溶液
①你认为上述两种方案设计更合理的是
②指出你认为不合理的方案存在的问题
(6)反应产物中的NO可以循环使用,用化学方程式表示循环使用的方案
II.(12分)复印机使用的墨粉主要成份是Fe3O4,图是氧化沉淀法生产Fe3O4的工艺: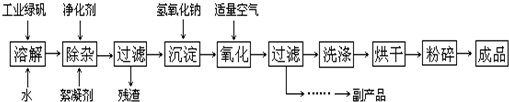
已知:
①工业绿矾中FeSO4的含量为52.5%,其中的杂质不参与反应;
②Fe(OH)2+2Fe(OH)3═Fe3O4?4H2O
请回答下列问题:
(1)铁的常见氧化物有
(2)Fe3O4与盐酸反应的化学方程式是:
(3)在工艺流程中,通入适量空气“氧化”时的化学方程式是:
(4)生产中可获得的副产品是
a.过滤 b.加热浓缩 c.冷却 d.结晶 e.洗涤
(5)在生产过程中,若工业绿矾的投料速率是12.16kg/h,为使产品较纯,鼓入空气的速率应为
查看习题详情和答案>>

胆矾和石膏在不同温度下的溶解度(g/100g水)见下表.
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
(1)红棕色滤渣的主要成分是
Fe(OH)3
Fe(OH)3
;(2)写出浸出过程中生成硫酸铜的化学方程式
3Cu+2HNO3+3H2SO4=3CuSO4+2NO↑+4H2O
3Cu+2HNO3+3H2SO4=3CuSO4+2NO↑+4H2O
;(3)操作I的操作温度应该控制在
100
100
℃左右;(4)从溶液中分离出硫酸铜晶体的操作II应为
冷却结晶、过滤
冷却结晶、过滤
、洗涤、干燥;(5)取样检验是为了确认Fe3+是否除净.有同学设计了以下两种方案,在实验室分别对所取样品按下列方案进行操作:
方案一:取样于试管→滴加KSCN溶液;
方案二:径向层析→喷KSCN溶液
①你认为上述两种方案设计更合理的是
方案二
方案二
;②指出你认为不合理的方案存在的问题
Cu2+的蓝色对检验有干扰
Cu2+的蓝色对检验有干扰
;(6)反应产物中的NO可以循环使用,用化学方程式表示循环使用的方案
4NO+3O2+H2O=4HNO3
4NO+3O2+H2O=4HNO3
.II.(12分)复印机使用的墨粉主要成份是Fe3O4,图是氧化沉淀法生产Fe3O4的工艺:

已知:
①工业绿矾中FeSO4的含量为52.5%,其中的杂质不参与反应;
②Fe(OH)2+2Fe(OH)3═Fe3O4?4H2O
请回答下列问题:
(1)铁的常见氧化物有
FeO、Fe2O3、Fe3O4
FeO、Fe2O3、Fe3O4
;(2)Fe3O4与盐酸反应的化学方程式是:
Fe3O4+8HCl=FeCl2+2FeCl3+4H2O
Fe3O4+8HCl=FeCl2+2FeCl3+4H2O
,检验反应后的溶液中含Fe3+的方法:取待测液少许于试管中,加入适量的KSCN溶液,若溶液显血红色,则证明含Fe3+
取待测液少许于试管中,加入适量的KSCN溶液,若溶液显血红色,则证明含Fe3+
;(3)在工艺流程中,通入适量空气“氧化”时的化学方程式是:
4Fe(OH)2+2H2O+O2=4Fe(OH)3
4Fe(OH)2+2H2O+O2=4Fe(OH)3
;(4)生产中可获得的副产品是
Na2SO4?10H2O
Na2SO4?10H2O
,提取该副产品的操作顺序是:bcdae
bcdae
(填写序号)a.过滤 b.加热浓缩 c.冷却 d.结晶 e.洗涤
(5)在生产过程中,若工业绿矾的投料速率是12.16kg/h,为使产品较纯,鼓入空气的速率应为
0.784
0.784
m3/h(假设反应在标准状态下进行,空气中O2占20%).
在众多的化学反应现象中,化学振荡现象最为令人惊奇,化学振荡实验很多,其中酸与铁丝的反应就是其中一例.某合作小组的同学查阅文献资料后,拟做铁丝与酸的化学振荡实验并进行探究.
实验步骤:
①将2cm左右的铁丝夹成多段,放在培养皿中,先用热的碳酸钠溶液除去铁丝表面的油污,蒸馏水冲洗后,再用某种试剂X浸泡到有大量气泡时取出,用蒸馏水冲洗干净.
②在细口瓶中加入30mL1.0mol/L的H3PO4、3mL30%的H2O2溶液,将处理后的铁丝放入其中.
③观察现象:铁丝表面产生气泡,随后消失,再产生气泡,再消失的周而往复的化学振荡现象出现,振荡周期约20秒,可维持数小时.
试回答下列问题:
(1)步骤①中,用试剂X可除去铁钉表面的铁的氧化物或镀层,所用的试剂X可能是 (选填序号:A.NaOH B.盐酸C.酒精).
(2)对振荡中产生的气体的成分,甲、乙两同学分别提出了假设,丙同学进行了验证.
甲同学认为是H2,其可能的理由是: .
乙同学认为是O2,其可能的理由是: .
丙同学在细口瓶中插入数据采集器氧气传感器,密封进行实验一小时,结果发现瓶中氧气的百分含量呈现逐渐减小的趋势,从而证明产生的气体是 .
(3)丁同学猜想酸与铁丝振荡体系中的反应机理及过程:
(a) Fe+2H+→Fe2++H2 (b)2Fe2++H2O2+H2O→Fe2O3+4H+
(c)Fe2O3+6H+→2Fe3++3H2O (d)2Fe3++H2→2Fe2++2H+,依据过程:
(a)→(b)→(c)→(d)→(a)…周而复始.
依据此机理,四步反应总的反应方程式为: .
(4)戊同学对本次实验中的所用铁钉中单质铁的含量进行测定,他们先配制一定物质的量浓度的硫酸,然后将一定质量的铁与硫酸(加入适量的铜粉)充分反应,并收集产生的气体,有关数据如下表:
所配硫酸的物质的量浓度为: mol/L;铁钉中单质铁的质量分数为 .
查看习题详情和答案>>
实验步骤:
①将2cm左右的铁丝夹成多段,放在培养皿中,先用热的碳酸钠溶液除去铁丝表面的油污,蒸馏水冲洗后,再用某种试剂X浸泡到有大量气泡时取出,用蒸馏水冲洗干净.
②在细口瓶中加入30mL1.0mol/L的H3PO4、3mL30%的H2O2溶液,将处理后的铁丝放入其中.
③观察现象:铁丝表面产生气泡,随后消失,再产生气泡,再消失的周而往复的化学振荡现象出现,振荡周期约20秒,可维持数小时.
试回答下列问题:
(1)步骤①中,用试剂X可除去铁钉表面的铁的氧化物或镀层,所用的试剂X可能是
(2)对振荡中产生的气体的成分,甲、乙两同学分别提出了假设,丙同学进行了验证.
甲同学认为是H2,其可能的理由是:
乙同学认为是O2,其可能的理由是:
丙同学在细口瓶中插入数据采集器氧气传感器,密封进行实验一小时,结果发现瓶中氧气的百分含量呈现逐渐减小的趋势,从而证明产生的气体是
(3)丁同学猜想酸与铁丝振荡体系中的反应机理及过程:
(a) Fe+2H+→Fe2++H2 (b)2Fe2++H2O2+H2O→Fe2O3+4H+
(c)Fe2O3+6H+→2Fe3++3H2O (d)2Fe3++H2→2Fe2++2H+,依据过程:
(a)→(b)→(c)→(d)→(a)…周而复始.
依据此机理,四步反应总的反应方程式为:
(4)戊同学对本次实验中的所用铁钉中单质铁的含量进行测定,他们先配制一定物质的量浓度的硫酸,然后将一定质量的铁与硫酸(加入适量的铜粉)充分反应,并收集产生的气体,有关数据如下表:
| ① | ② | ③ | |
| 硫酸溶液体积/mL | 50 | 50 | 50 |
| 称取铁钉质量/g | 5.0 | 6.0 | 7.0 |
| 再投入铜粉质量/g | 1.0 | 1.0 | 1.0 |
| 标准状况下的体积/L | 1.97 | 2.24 | 2.24 |
用NA表示阿伏加德罗常数的值,下列叙述中正确的是
A.0.1mol/L的NaOH溶液中钠离子数为0.1 NA
B.1.8 g重水(D2O)中,含有的质子数为0.1NA
C.5.6 g铁投入浓硫酸中,生成的气体分子数为0.1 NA
D.标准状况下,560 mL甲烷和甲醛的混合气体中,含有的共用电子对数为0.1 NA
查看习题详情和答案>>以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如下表。
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8× 10-19 10-19 |
| AlAsO4 | 1.6×1 0-16 0-16 |
| FeAsO4 | 5.7×10-21 |
| 污染物 | H2SO4 | As |
| 浓度 | 28.42 g/L | 1.6 g·L-1 |
| 排放标准 | pH 6~9 | 0.5 mg·L-1 |
回答以下问题:
⑴该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)= ▲ mol·L-1。
⑵写出难溶物Ca3(AsO4)2的Ksp表达式:Ksp[Ca3(AsO4)2]= ▲ ,若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol·L-1,c(AsO43-)的最大是 ▲ mol·L-1。
⑶工厂排放出的酸性废水中的三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸),写出该反应的离子方程式 ▲ 。
⑷在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为 ▲ ;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为 ▲ 。 查看习题详情和答案>>
以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如下表。
表1.几种砷酸盐的Ksp 表2.工厂污染物排放浓度及允许排放标准
回答以下问题:
⑴该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)= ▲ mol·L-1。
⑵写出难溶物Ca3(AsO4)2的Ksp表达式:Ksp[Ca3(AsO4)2]= ▲ ,若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol·L-1,c(AsO43-)的最大是 ▲ mol·L-1。
⑶工厂排放出的酸性废水中的三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸),写出该反应的离子方程式 ▲ 。
⑷在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为 ▲ ;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为 ▲ 。
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8× 10-19 10-19 |
| AlAsO4 | 1.6×1 0-16 0-16 |
| FeAsO4 | 5.7×10-21 |
| 污染物 | H2SO4 | As |
| 浓度 | 28.42 g/L | 1.6 g·L-1 |
| 排放标准 | pH 6~9 | 0.5 mg·L-1 |
回答以下问题:
⑴该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)= ▲ mol·L-1。
⑵写出难溶物Ca3(AsO4)2的Ksp表达式:Ksp[Ca3(AsO4)2]= ▲ ,若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol·L-1,c(AsO43-)的最大是 ▲ mol·L-1。
⑶工厂排放出的酸性废水中的三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸),写出该反应的离子方程式 ▲ 。
⑷在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为 ▲ ;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为 ▲ 。