网址:http://m.1010jiajiao.com/timu_id_500331[举报]
(1)氯元素的原子结构示意图为


(2)氯、硫、磷三种元素对应的气态氢化物中,稳定性由强到弱的顺序为
(3)含有氯元素的常见物质转化关系如图:
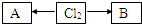 ,A、B中氯元素化合价的代数和为0,且均是共价化合物,A为强电解质,B具有漂白性,写出A→Cl2的化学反应方程式
,A、B中氯元素化合价的代数和为0,且均是共价化合物,A为强电解质,B具有漂白性,写出A→Cl2的化学反应方程式
| ||
| ||
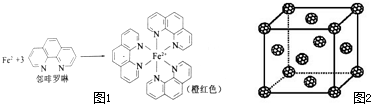 元素周期表中第四周期的金属元素在生产和科研中有非常重要的使用价值.
元素周期表中第四周期的金属元素在生产和科研中有非常重要的使用价值.(1)测定土壤中铁的含量时需先将三价铁还原为二价铁,再采用邻啡罗啉作显色剂,用比色法测定,若土壤中含有高氯酸盐时会对测定有干扰.相关的反应如下:
4FeCl3+2NH2OH?HCl→4FeCl2+N2O↑+6HCl+H2O
①Fe2+在基态时,核外电子排布式
②羟胺中(NH2OH)采用SP3杂化的原子有
③Fe2+与邻啡罗啉形成的配合物中,配位数为
(2)向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体,该晶体中含有的化学键类型是
(3)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+,已知NF3与NH3的空间构型都是三角锥形,但NF3 不易与Cu2+形成配离子,其原因是
(4)配合物Ni(CO)4常温下呈液态,易溶于CCl4、苯等有机溶剂.固态Ni(CO)4属于
(5)如果把晶胞顶点与最近三个面心所围成的空隙叫做四面体空隙,第四周 期电负性最小的原子可作为容体掺入C60 晶体的空隙中,形成具有良好的超导性的掺杂C60 化合物.现把C60抽象成质点,该晶体的晶胞结构如图2所示,若每个四面体空隙填入一个原子,则全部填满C60 晶体的四面体空隙后,所形成的掺杂C60 化合物的化学式为
| 元素 | A | B | C |
| 性质结构信息 | 单质在氯气中燃烧火焰呈黄色并产生大量白烟,所得产物的阳离子与D的阳离子电子数相同. | 单质是带有金属光泽的灰黑色固体,是信息技术的关键材料. | 最高价氧化物的水化物与其气态氢化物反应得到离子化合物D. |
(2)C的气态氢化物的电子式
(3)D的水溶液呈
(1)氯元素的最高价氧化物为无色液体,0.25 mol 该物质与一定量水混合得到一种稀溶液,并放出Q kJ 的热量。写出该反应的热化学方程式: 。
(2)已知:Fe2O3(s) + 3/2C(s) = 3/2CO2(g) + 2 Fe(s) ΔH =234.1 kJ·mol-1
C(s) + O2(g) = CO2(g) ΔH = —393.5 kJ·mol-1
则2 Fe(s)+ 3/2O2(g) = Fe2O3(s) 的ΔH是 kJ·mol-1。
(3)意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如下图所示。已知断裂1moIN-N吸收167kJ热量,生成1molN≡N放出942kJ。根据以上信息和数据,写出N4气体转变为N2的热化学方程式: 。
(4)下图是丙烷(C3H8)、二甲醚(CH3OCH3)燃烧过程中能量变化图,其中x为各自反应中对应的系数。根据该图写出二甲醚燃烧的热化学方程式: 。
(1)氯元素的最高价氧化物为无色液体,0.25 mol 该物质与一定量水混合得到一种稀溶液,并放出Q kJ 的热量。写出该反应的热化学方程式: 。
(2)已知:Fe2O3(s) + 3/2C(s) = 3/2CO2(g) + 2 Fe(s) ΔH =234.1 kJ·mol-1
C(s) + O2(g) = CO2(g) ΔH = —393.5 kJ·mol-1
则2 Fe(s)+ 3/2O2(g) = Fe2O3(s) 的ΔH是 kJ·mol-1。
(3)意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如下图所示。已知断裂1moIN-N吸收167kJ热量,生成1molN≡N放出942kJ。根据以上信息和数据,写出N4气体转变为N2的热化学方程式: 。

(4)下图是丙烷(C3H8)、二甲醚(CH3OCH3)燃烧过程中能量变化图,其中x为各自反应中对应的系数。根据该图写出二甲醚燃烧的热化学方程式: 。
查看习题详情和答案>>