网址:http://m.1010jiajiao.com/timu_id_499562[举报]
1.D 2.C 3.C 4.B 5.C 6.C 7.BC 8.BD 9.AC 10.D 11.C
12.BD 13.AC 14.A 15.B 16.D 17.B 18.D 19.B 20.D
21.D 22.C w.w.w.k.s.5.u.c.o.m
23.(1)促进,A (2)甲大
乙用氯化铵溶液稀释后,[ ]增大很多,使
]增大很多,使 的电离平衡向抑制电离的方向移动;
的电离平衡向抑制电离的方向移动; 发生水解,使稀释后的乙溶液的[
发生水解,使稀释后的乙溶液的[ ]增大
]增大
24.(1)第一种组合 A:NaOH B:
第二种组合 A: B:
B:
(2)由于 电离出
电离出 ,使水的电离平衡:
,使水的电离平衡:

 向左移动,使水的电离度小于纯水中水的电离度,而
向左移动,使水的电离度小于纯水中水的电离度,而 溶液中由于
溶液中由于


由于 电离出的
电离出的 与
与 结合生成弱电解质
结合生成弱电解质 ,从而促进水的电离,使水的电离度比纯水中的大.
,从而促进水的电离,使水的电离度比纯水中的大.
25.(1)偏高;空气中的氧气溶于样品中
(2)偏高;使 溶液浓度变低,消耗体积偏大
溶液浓度变低,消耗体积偏大
(3)偏高;使最后读取体积数比实际消耗 溶液体积数大
溶液体积数大
(4)
26.(1)增大w.w.w.k.s.5.u.c.o.m
(2)K值越大,酸性越强
(3)

(4) 上一级电离产生的
上一级电离产生的 对下一级电离有抑制作用
对下一级电离有抑制作用
(5)
27.(1) 和
和 水解均呈弱酸性,可除去金属表面的氧化物
水解均呈弱酸性,可除去金属表面的氧化物
(2) 水溶液中[
水溶液中[ ]很小,不会生成沉淀(或弱酸不能生成强酸).加入氨水时,
]很小,不会生成沉淀(或弱酸不能生成强酸).加入氨水时,

 ,使
,使 电离平衡右移,[
电离平衡右移,[ ]增大,产生沉淀(或
]增大,产生沉淀(或 与
与 生成
生成 ,使[
,使[ ]增大
]增大
(3)在HCl气流中, 抑制
抑制 水解,从而可得到
水解,从而可得到 无水物
无水物
(4)能. ,降低[
,降低[ ],其水解平衡左移,碱性减弱
],其水解平衡左移,碱性减弱
(5) 水解呈碱性,
水解呈碱性, 水解呈酸性,二者混合施用,会促进水解,大量生成易挥发的
水解呈酸性,二者混合施用,会促进水解,大量生成易挥发的 ,从而使氮肥降低肥效
,从而使氮肥降低肥效
 电离呈酸性,与
电离呈酸性,与 混合施用,会产生
混合施用,会产生 或
或 沉淀而丧失肥效.
沉淀而丧失肥效.
硫铵(即硫酸铵)水解呈酸性,长期施用土壤会板结酸化,加消石灰可调节酸度,防止板结.
28.(1)造成测定数值偏高w.w.w.k.s.5.u.c.o.m
(2)
(3)
29.(1) ;
; 、
、
(2)1.90 2.67 5.20
(3)130
分析:(1)因为在浊液中加入HCl溶液至10 mL,沉淀质量一直为 形式存在,继续加入HCl溶液,
形式存在,继续加入HCl溶液, 转变为
转变为 沉淀,加至30 mL时,
沉淀,加至30 mL时, 全部转变为
全部转变为 ,所以在A点的沉淀物为
,所以在A点的沉淀物为 ,在A至B点间,沉淀物为
,在A至B点间,沉淀物为 和
和 的混合物.当加入的HCl溶液超过30 mL时,
的混合物.当加入的HCl溶液超过30 mL时, 和
和 同时溶解.w.w.w.k.s.5.u.c.o.m
同时溶解.w.w.w.k.s.5.u.c.o.m
(2)原混合物中:
 的质量
的质量


 的质量
的质量
NaOH:
①浊液中存在的:
1×0.01 mol
② 消耗的:
消耗的:


③ 消耗的:
消耗的:

0.02 mol×4=0.08 mol
NaOH总质量
(3)从B点开始, 消耗的HCl:0.02 mol×3=0.06 mol
消耗的HCl:0.02 mol×3=0.06 mol
 消耗的HCl:0.02 mol×2=0.04 mol
消耗的HCl:0.02 mol×2=0.04 mol
所消耗HCl溶液的体积为:
Q点HCl溶液总量为:30 mL+100 mL=130 mL
30.(1)
(2)

根据 
过量 为:
为:
20.00 mL水样消耗 为
为
根据得电子数目相等,则有
相当于 为:
为:
 ,即该水样的
,即该水样的
(3)
(4)A,
 www.ks5u.com
www.ks5u.com
| 催化剂 |
| 催化剂 |
| Cu |
| △ |
| Cu |
| △ |
| 催化剂 |
| 催化剂 |
 B.电解原理在化学工业中广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
B.电解原理在化学工业中广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入酚汰试液,则
①Y电极上的电极反应式为
②在X电极附近观察到的现象是
③要使电解后溶液恢复到电解前的状态,则需加入(或通入)
(2)如果要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是
②电解完成后,硫酸铜溶液的浓度
(3)若X、Y都是铜电极,a是浓度均为2mol?L-1的AgNO3与Cu(NO3)2的混合溶液1L,电解一段时间后X电极上有3.2g铜析出,此时直流电源已输出
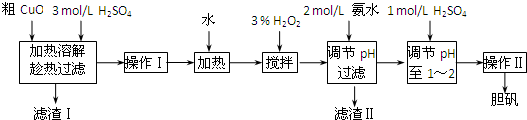
Fe3+、Fe2+、Cu2+转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
(2)加入2mol/L氨水后,溶液的pH应在
(3)经操作Ⅰ得到粗胆矾,经操作Ⅱ得到精制胆矾.两步操作相同,都包括
(4)调节溶液的pH常选用稀酸或稀碱,而不用浓酸、浓碱,理由是
(1)甲组用凝胶-溶胶法,它们用结晶氢氧化铝、烧碱、CO2及盐酸为试剂生产,其中涉及的氢氧化铝与烧碱反应的化学方程式为:
(2)乙组采用不足量酸溶法,原料主要是铝加工的下脚料铝屑、铝灰和铝渣等,反应原理为:2Al+(6-n)HCl+nH2O=Al2(OH)nCl6-n+3H2↑.该制备方法工艺简单、成本低,利用本身是放热反应,故不需要加热,可能缺点有:
(3)丙组拟用高岭土(Al2O3?2SiO2?2H2O)等为原料,经焙烧、盐酸浸取、聚合、熟化、蒸发、干燥等步骤得到固体PAC.其中液体PAC蒸发时,适宜在110℃左右,你认为适宜的加热方法是
(4)丁组同学对甲、乙、丙组同学制得的样品进行定性实验,请你补充下列实验报告
| 实验序号 | 实验步骤 | 实验现象 | 结论 |
| ① | 用激光笔照射甲组制得的PAC溶液 | 光亮的通路 | |
| ② | 取乙组制得的样品少许加入铝试剂阿罗明拿 | 变成玫瑰红色 | |
| ③ | 取丙组样品少许,溶于适量的水制得的淡黄色透明液体中加入氟化铵 |

实验室制备NaFeEDTA?3H2O步骤如下:
①把0.4g(0.01mol)NaOH溶于10mL蒸馏水,然后再加入3.8g(0.01mol)Na2H2EDTA?2H2O,把溶液微热,直至固体完全溶解.
②用含有氯化铜杂质的氯化铁提纯并制得FeCl3?6H2O.称取2.5g(0.009mol)FeCl3?6H2O溶于5mL,蒸馏水中(并加1滴盐酸).
③将①、②制得的两溶液混合
④加热溶液至沸腾,蒸发浓缩直至大部分粉末状的固体析出.
⑤冷却、采用右图装置减压过滤,先用冰水洗涤再用乙醇洗涤.
⑥将固体凉干,称得制得的淡黄色粉末2.8g.
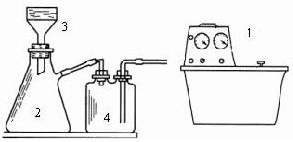
试回答下列问题
(1)在步骤①中,不能加入过量的碱,是因为
(2)将含有氯化铜杂质的氯化铁溶液分离可用的简单方法是
(3)步骤⑤中用冰水和乙醇洗涤的目的是,
(4)本实验得到的是粉末状淡黄色的粉末,没有得到块状的晶体,可能的原因是:
(5)检验某品牌酱油中是否加有NaFeEDTA?3H2O,先取20mL酱油加入10mL75%乙醇,将所得沉淀物溶于水,并用某盐酸调到pH<0.5,破坏配合物,然后加入某种铵盐检验,该铵盐是
(6)本次实验的NaFeEDTA?3H2O的实际产率为: