网址:http://m.1010jiajiao.com/timu_id_499404[举报]
1.C 2.C 3.B 4.D 5.D 6.B 7.D 8.BC 9.BC 10.CD 11.A
12.BC 13.C 14.A 15.B 16.C 17.A 18.C 19.C 20.B 21.D 22.C
23.146,即 的式量=146,求得n=5
的式量=146,求得n=5
则赖氨酸的结构简式为

生成的二肽的结构简式为

或
24.B: ;
;
D: ;
;
25.(1)

(2)

(3)
26.(1)

 CH=CHCOOH
CH=CHCOOH 
(2)氧化 消去 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
(3)解:




27.(1) (2)0.96,0.08
(2)0.96,0.08
(2)
(3)

29.解:C分子中 ,最简式为CH因C中含42个电子,故C为
,最简式为CH因C中含42个电子,故C为 ,盐B为
,盐B为
A分子中 ,∴ A为
,∴ A为
(1) (2)144 (3)
(2)144 (3)
30.解析:(1)1 mol的D与银氨溶液反应,析出 且D的组成符合
且D的组成符合 的分子式,说明该分子中有一个氧原子,且含两个醛基,则该分子应为甲醛
的分子式,说明该分子中有一个氧原子,且含两个醛基,则该分子应为甲醛 ,若D为甲醛,则C应为甲醇.
,若D为甲醛,则C应为甲醇.
(2)由题知B为不饱和酸,可与 反应,也可与
反应,也可与 反应.又∵ 0.02 mol B可与
反应.又∵ 0.02 mol B可与 反应,说明B中只含一个C=C,可设B的分子式为
反应,说明B中只含一个C=C,可设B的分子式为
(3) ,那么A应为:
,那么A应为:
又∵ 0.5 mol C可与0.5 mol B反应,而1mol A和B的混合物与0.5 mol C反应,分离出1 mol A,说明A和B的混合物中,A、B各占0.5 mol.
∴ 有0.5(12n+2n-1+12+32+15)+0.5?(12n+2n-1+12+33)=79
解之n=2
∴ B为 ,即
,即
A为
答案:
A为丙烯酸甲酯( )
)
B为丙烯酸( )
)
C为甲醇( )
)
D为甲醛(HCHO)
 w.w.w.k.s.5www.ks5u.com
w.w.w.k.s.5www.ks5u.com
(1)A的氢化物沸点比同族元素其他氢化物沸点高的原因是
(2)研究表明,B、C能形成一种三原子分子,且该分子中所有原子都达到8电子稳定结构,则该分子的结构式为
(3)A、D两元素最高价氧化物对应的水化物能发生反应,其离子方程式为
(4)E的氢化物常做野外生氢剂,只要将其与H2O混合立即产生大量的H2,写出该反应的化学方程式
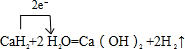
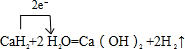
①它们位于三个不同短周期,核电荷数依次增大 ②B与F同主族.
③B、C分别都能与D按原子个数比1:1或1:2形成化合物.
④A、E分别都能与D按原子个数比1:1或2:1形成化合物.
| I1 | I2 | I3 | I4 | … |
| 496 | 4562 | 6912 | 9540 | … |
(1)写出只含有A、B、D、E四种元素的两种无水盐的化学式
(2)B2A2分子中存在
(3)人们通常把拆开1mol某化学键所吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可以用于计算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.下表列出了上述部分元素形成的化学键的键能:
| 化学键 | F-D | F-F | B-B | F-B | C-D | D-D |
| 键能/kJ?mol-1 | 460 | 176 | 347.7 | 347 | 745 | 497.3 |
①它们位于三个不同短周期,核电荷数依次增大 ②B与F同主族.
③B、C分别都能与D按原子个数比1:1或1:2形成化合物.
④A、E分别都能与D按原子个数比1:1或2:1形成化合物.
| I1 | I2 | I3 | I4 | … |
| 496 | 4562 | 6912 | 9540 | … |
(1)写出只含有A、B、D、E四种元素的两种无水盐的化学式 、 .
(2)B2A2分子中存在 个σ键, 个π键.
(3)人们通常把拆开1mol某化学键所吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可以用于计算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.下表列出了上述部分元素形成的化学键的键能:
| 化学键 | F-D | F-F | B-B | F-B | C-D | D-D |
| 键能/kJ?mol-1 | 460 | 176 | 347.7 | 347 | 745 | 497.3 |
氯只有35Cl和37Cl两种稳定同位素,它们在氯气中的原子数之比35Cl∶37Cl为3∶1,则分子量为70、72、74的氯气分子数之比不可能是
[ ]
有A、B、C、D、E、F六种元素,已知:
①它们位于三个不同短周期,核电荷数依次增大
②B与F同主族.
③B、C分别都能与D按原子个数比1∶1或1∶2形成化合物,C、D元素在空气中大量存在.
④A、E分别都能与D按原子个数比1∶1或2∶1形成化合物.
⑤E元素的电离能数据如下表(kJ·mol-1):
(1)写出只含有A、B、D、E四种元素的一种无水盐的化学式________.
(2)B2A2分子中存在________个σ键,________个π键.
(3)比较元素电负性大小关系:B________C;比较元素第一电离能大小关系:C________D.(填<或>)
(4)人们通常把拆开1 mol某化学键所吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可以用于计算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.下表列出了上述部分元素形成的化学键的键能:
试计算1 mol F单质晶体燃烧时的反应热ΔH=________(要写单位).


