网址:http://m.1010jiajiao.com/timu_id_495455[举报]
选择题答案表:
题号
1
2
3
4
5
6
7
8
答案
A
C
A
C
C
A
D
D
题号
9
10
11
12
13
14
答案
B
AD
C
D
BD
AD
15、(12分)Ⅰ(4分)①②④⑥
Ⅱ(8分)⑴用冰水冷却有利于析出更多的晶体,黑暗可以防止晶体分解(2分)
⑵过滤、洗涤(1分)
⑶100mL容量瓶、酸式滴定管(2分) (紫)红(1分) ⑷3 (2分)
 16、(8分(1)NaClO(1分)(2)
16、(8分(1)NaClO(1分)(2) (1分)
(1分)
(3)2NaCl +2H2O
 H2↑+ Cl2↑+2NaOH (2分) 氯碱工业(1分)
H2↑+ Cl2↑+2NaOH (2分) 氯碱工业(1分)
(4)2Fe3+ + 3ClO? + 10OH? = 2FeO42? + 3Cl? + 5H2O(2分)
②本身被还原成Fe3+而发生水解生成Fe(OH)3胶体吸附水中杂质以达到净化水的目的。(1分)
17、(10分)(1)FeSO4?7H2O (写FeSO4晶体也给分)
(2)防止Fe2+氧化; 取副产品甲少许溶于水,滴加适量KSCN溶液,观察溶液是否变为血红色。
(3)稀盐酸(或稀硫酸等) (4)TiO2  Ti+O2↑
(每空2分,共10分)
Ti+O2↑
(每空2分,共10分)
18、(10分)⑴2NO3-+5Mg+6H2O==N2↑+5Mg(OH)2+2OH-(2分)
⑵①快速方便易行(2分,相近合理答案也给分)
②空白对照实验(2分,相近合理答案也给分)
③将水样先稀释一定倍数后再重复实验(2分)
⑶ 800 (2分)
19、(12分)(1)加成 (1分)(2)13(2分)
(3)(4分) (4)(5分)
(4)(5分)

20、(10分)⑴ 0.01 mol?L-1(2分) 不变(1分)
⑵ <(2分)
⑶ 设焙烧炉中消耗空气的物质的量为5x,鼓风炉中消耗空气物质的量为5y,则:
 Zn(g)+CO2(g)
Zn(g)+CO2(g)
y 2y 1mol 2y×62.5% 1mol
2y×62.5%=1mol y=0.8mol 5y=4mol(2分)
2ZnS + 3O2 = 2ZnO + 2SO2 △n
2mol 1mol
1mol 0.5mol
4x/(5x-0.5mol)=82.5% x=3.3mol 5x=16.5mol(2分)
5x+5y=4mol+16.5mol=20.5mol
V(空气)=20.5×
 21、(12分)
21、(12分)
(1)CD(2分) (2) H3AsO4(1分);第四周期元素,原子核外只有四个电子层。按能量最低原理,4s上排2个电子,3d上排10个电子,4p上排6个电子,共对应18种元素,若4d排电子,就出现了第五电子层,就不是第四周期元素了,所以第四周期只有18种元素。(2分) (2)+3(1分);正四面体(1分);3d74s2(1分) (3)BC(2分)
(4)N2O或CO2或CS2或BeCl2;SCN-或OCN-(2分)
| 时间(s) n(mol) | 20 | 40 | 60 | 80 | 100 | |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
②计算在80℃时该反应的平衡常数K=______;
③反应进行至100s后将反应混合物的温度降低,混合气体的颜色(填“变浅”、“变深”或“不变”)______;
④要增大该反应的K值,可采取的措施有(填序号)______
A.增大N2O4的起始浓度B.向混合气体中通入NO2 C.使用高效催化剂 D.升高温度
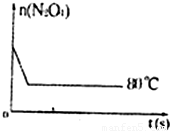
⑤如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线______.
(2)难溶电解质在水溶液中存在着电离平衡.在常温下,溶液里各离子浓度以它们化学计量数为方次的乘积是一个常数,叫溶度积常数(Ksp).例如Cu(OH)2(S)?Cu2+(aq)+2OH-(aq),Ksp=c(Cu2+)?[c(OH-)]2=2×10-20当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解.若某CuSO4溶液里c(Cu2+)=0.02mol/L,如果生成Cu(OH)2沉淀,应调整溶液pH,使之大于______;
要使0.2mol/L的CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,使溶液pH值为______.
(3)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色.则该溶液呈______性.在分析该溶液遇酚酞呈红色原因时,甲同学认为是配制溶液所用的纯碱样品中混有NaOH所致;乙同学认为是溶液中Na2CO3电离出的CO32-水解所致.请你设计一个简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论)
______.
 查看习题详情和答案>>
查看习题详情和答案>>
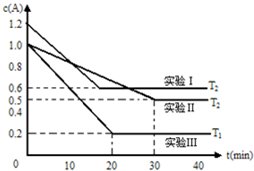 恒容体系,发生如下反应2A(g)?B(g)+xC(?)△H,起始时B、C物质的量浓度为0,A的物质的量浓度随时间变化如图(某课外活动小组一共进行了如图所示的三个实验,其中T1、T2表示不同的反应温度):
恒容体系,发生如下反应2A(g)?B(g)+xC(?)△H,起始时B、C物质的量浓度为0,A的物质的量浓度随时间变化如图(某课外活动小组一共进行了如图所示的三个实验,其中T1、T2表示不同的反应温度):(1)在实验Ⅲ中,0~20min的时间内,v(B)=
(2)根据以上实验事实,完成以下填空:x=
(3)在实验Ⅱ中,当化学反应进行到35min时,下列关于反应体系中的有关说法,正确的是
a.单位时间内生成n mol B的同时生成2n mol A
b.单位时间内生成n mol C的同时消耗2n mol A
c.用A、B、C表示的反应速率的比为2:1:2
d.混合气体中反应物A与生成物B的体积分数之比为2:1
e.混合气体中B与C的物质的量相等
(4)该反应的化学平衡常数表达式K=
| c(B)?c(C) |
| c2(A) |
| c(B)?c(C) |
| c2(A) |
(5)T1℃时,保持容器的体积不变,若充入amolA、bmolB、cmolC,达到平衡时C的体积分数为0.4,则a、b、c的取值可以是
a.a=2、b=1、c=2 b.a=0.5、b=1.7、c=1.7
c.a=1、b=1、c=1 d.a=x、b=c=2x(x>0)
e.b=c、a为大于0的任意值.
(1)向合成塔中按1:4的物质的量之比充入N2、H2进行氨的合成,图A为T0C时平衡混合物中氨气的体积分数与压强(P)的关系图.

①写出工业上合成氨的化学方程式
| ||
| 高温高压 |
| ||
| 高温高压 |
②图A中氨气的体积分数为15.00%时,H2的转化率=
③图B中T=500°C,温度为4500C对应的曲线是
④由图象知,增大压强可提高原料的利用率,从生产实际考虑增大压强需解决的问题是
(2)合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为:
CH4(g)+H2O
 CO(g)+3H2(g);△H=+QkJ/mol(Q>0)
CO(g)+3H2(g);△H=+QkJ/mol(Q>0)(3)一定温度下,在2L容器中发生上述反应,各物质的物质的量变化如下表
| 时间/min | CH4(mol) | H20( mol) | CO (mol) | H2 (mol) |
| 0 | 0.40 | 1.00 | 0 | 0 |
| 5 | X1 | X2 | X3 | 0.60 |
| 7 | Y1 | Y2 | 0.20 | Y3 |
| 10 | 0.21 | 0.81 | 0.19 | 0.62 |
前5min平均反应速率v(CH4)=
②反应在7~10min之间,CO的物质的量减少的原因可能是
a?减少CH4 b?降低温度c?增大压强d?充入H2
③若保持温度不变,向1L容器中起始充入0.15mol CH4.0.45mol H2O.

