网址:http://m.1010jiajiao.com/timu_id_494934[举报]
一.选择题(每小题3分,共48分)
题号
1
2
3
4
5
6
7
8
答案
D
D
B
D
C
B
D
C
题号
9
10
11
12
13
14
15
16
答案
C
D
D
A
B
B
D
A
二.填空题(30分)
17.(6分)(1)释放(2分)
(2)-( b - a) kJ?mol-1(2分)
(3)N2(g)+3H2(g)=2NH3(1) △H=-2(b+c -a)kJ?mol-1(2分)
18.(共8分 ) (1)0.05 (2)③⑤ ④ (3)
19.(共10分) (1)②⑤⑥,①④,
(2)②⑤⑥,NH4++H2O NH3?H2O+H+、ClO-+H2O
NH3?H2O+H+、ClO-+H2O HClO+OH-、HCO
HClO+OH-、HCO +H2O
+H2O H2CO3+OH-。(任写一个)
H2CO3+OH-。(任写一个)
(3)④②③⑥⑤① (每空2分)
20.(8分)>, Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
=, 2Al3++3SO42-+3Ba2++6OH-=3BaSO4↓+2Al(OH)3↓(每空2分)
21.(10分) (1)①酸 大于 ②酚酞 、甲基橙 ③24.60 (4分)
(2) (24.60ml×ca mol.L-1)/Vml(2分)
(3)无影响 偏低 偏高 偏低 (4分)
22.(10分) (1)2CuSO4+2NaOH=Cu2(OH)2SO4↓+Na2SO4 (2分)
(2)将浅绿色的浊液过滤,并把得到的绿色沉淀用蒸馏水多次洗涤,至洗涤液中用BaCl2溶液检验不出SO42-后(1分),用足量稀盐酸溶解绿色沉淀,此时再用BaCl2溶液检验,溶液中有白色沉淀生成,表示浅绿色沉淀中有SO42-。(1分)
(3)Cu2(OH)2SO4+2NaOH=2 Cu(OH)2↓+Na2SO4 (2分),沉淀溶解平衡中,溶解度小的沉淀会转化为溶解度更小的沉淀(2分)
(4) (2分)
(2分)
(1)磷元素的原子结构示意图是


(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:
2Ca3(PO4)2+6SiO2═6CaSiO3+P4O10 10C+P4O10═P4+10CO
每生成1molP4时,就有
(3)硫代硫酸钠(Na2S2O3)是常用的还原剂.在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素C完全氧化,剩余的I2用Na2S2O3溶液滴定,可测定溶液中维生素C的含量.发生的反应为:C6H8O6+I2═C6H6O6+2H++2I- 2S2O32-+I2═S4O62-+2I-
在一定体积的某维生素C溶液中加入a mol?L-1I2溶液V1mL,充分反应后,用Na2S2O3溶液滴定剩余的I2,消耗b mol?L-1Na2S2O3溶液V2mL.该溶液中维生素C的物质的量是
| aV1-0.5bV 2 |
| 1000 |
| aV1-0.5bV 2 |
| 1000 |
II、稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位.
(4)铈(Ce)是地壳中含量最高的稀土元素.在加热条件下CeCl3易发生水解,无水CeCl3可用加热CeCl3?6H2O和NH4Cl固体混合物的方法来制备.其中NH4Cl的作用是
(5)在某强酸性混合稀土溶液中加入H2O2,调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离.完成反应的离子方程式:
□Ce3++□H2O2+□H2O═□Ce(OH)4↓+□
M2++2OH-
 M(OH)2
M(OH)2  2H++MO22-
2H++MO22-回答以下题目一律用“增大”“减小”“不变”填空
(1)在其他条件不变的情况下,25C° 时,在蒸馏水中加入A物质后,与加入前比较,
①由水电离出的C(OH-)
(2)25C° 时,向A的稀溶液中加入少量的烧碱固体.则水的电离度
Ⅱ、.室温下,甲、乙两瓶氨水的浓度分别为1mol/L和0.1mol/L,则甲、乙两瓶氨水中C(OH-)之比为
2K2Cr2O7(橙色)+3C2H5OH+H2SO4→Cr2(SO4)3(绿色)+K2SO4+CH3COOH+H2O
①配平化学方程式后,H2O前面的系数为
②怎样判断司机是酒后开车:
③写出用粮食酿酒的化学方程式:
| ||
| ||
| 酵母菌 |
| ||
| ||
| 酵母菌 |
Ⅱ、下列框图中,A由两种黑色金属氧化物等物质的量混合而成,B中含有四种阳离子.据此回答下列问题:

(1)A的组成是
(2)相同条件下,溶液B中所有阳离子的氧化性由强到弱的顺序依次是
(3)A中某组分可由单质与水反应制得,化学方程式为:
| ||
| ||
(4)电解所用装置如图所示.
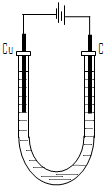
①电解开始阶段,阳极上的电极反应是
阴极上的电极反应是
②电解至阴极刚开始有固体R析出时,该溶液中金属离子浓度由大到小
的顺序是
(1)pH<
(2)对汽车加装尾气催化净化装置,可以使其中的NO、CO相互反应转化成无毒的气体,其原理可以用化学方程式表示为
| ||
| ||
(3)获得洁净安全的饮用水是每个人的正常需要.某农村地区为获得饮用水,在将地表水取回家后,常使用漂白粉或漂白精片进行杀菌消毒,其原理可用化学方程式表示为
Ⅱ、(1)下列常用物质:A.碳酸镁 B.阿斯匹林 C.葡萄糖 D.苯甲酸钠 E.柠檬黄(请用字母填空)
具有解热镇痛疗效的是
(2)①氢氧化铝,小苏打均可防治胃酸分泌过多,其发挥功效时的化学方程式
②淀粉在抗酸药中作填充剂、粘合剂,淀粉在人体内酶的催化作用下发生水解反应,最终转化为(写分子式)
③发育出现障碍,患营养缺乏症,这主要是由于摄入蛋白质不足引起的.蛋白质在人体内水解的最终产物是
 Ⅰ、写出甲烷燃料电池在酸性溶液中的电极反应和总电池反应:
Ⅰ、写出甲烷燃料电池在酸性溶液中的电极反应和总电池反应:正极:
负极:
总反应:
Ⅱ、如图所示,A、F为石墨电极,B、E为铁片电极.
按要求回答下列问题.
(1)打开K2,合并K1.
①B为
②最终可观察到的现象是:
③涉及的两个主要的化学反应的化学方程式为:
(2)打开K1,合并K2.
①E为
②检验F极产生气体的方法是:
(3)若往U型管中滴加酚酞,进行(1)(2)操作时,A、B、E、F电极周围能变红的是
| 周围变红的电极代号(填字母) | 原因 |
A A |
O2+2H2O+4e-=4OH-,产生OH- O2+2H2O+4e-=4OH-,产生OH- |
E E |
2H++2e-=H2↑ H+反应,促进了水的电离,溶液中c(OH-)>c(H+) 2H++2e-=H2↑ H+反应,促进了水的电离,溶液中c(OH-)>c(H+) |
无 无 |
无 无 |
无 无 |
无 无 |