网址:http://m.1010jiajiao.com/timu_id_480422[举报]
选择题:共21小题.每小题6分。共126分。
一、选择题:选对的给6分.选错或未选的给0分。
1.A 2.D 3.B 4.C 5.D 6.C 7.B 8.A 9.D 10.A
11.B 12.C 13.B
二、选择题(本题包括8小题、共48分。每小题给出的四个选项中,有的只有一个选项正
确.有的有多个选项正确.全部选对的得6分.选对但不全的得3分.有选错的得0分)
14.A 15.D 16.B 17.A 18.BC 19.D 20.BC 21.C
非选择题(共174分)
22.实验题(本题共2小题,共18分.把答案填在题中的横线上或按要求作图)
I.①游标卡尺的读数为
 解:如图所示,
解:如图所示, =R/d=tan63°26′06″=2.000,
=R/d=tan63°26′06″=2.000,
∴R=2d=AB,20分度游标卡尺的读数等于AB间距离为
∴被测圆形工件的直径为
②4.600(3分)
Ⅱ.①(4分)
 ②
② (4分)
(4分)
③“等于”(3分)
设电压表内阻为 ,先闭合S1,断开S2,
,先闭合S1,断开S2,
 ;再保持
;再保持 不变,闭合S2,
不变,闭合S2,

计算题(共54分)解答时应写出必要的文宇说明、方程式和重要的演算步骤.只写出最后答案的不能得分。有数值计算的题。答案中必须明确写出数值和单位。
23.(16分)解:设两球碰撞后,球的速度分别为 、
、
由动量守恒定律得: ①(4分)
①(4分)
设B球在最高点的速度为 ,由牛顿第二定律得:
,由牛顿第二定律得: ②(4分)
②(4分)
碰后B球运动到F点的过程中,由动能定理得: ③(4分)
③(4分)
②代人③得:
代入①可得: 一
一
方向水平向左 (1分)
24.(18分)解:(1)设水平拉力为F,对框架、cd棒受力分析,
 当框架匀速运动时,对框架有:F=
当框架匀速运动时,对框架有:F= +F安(2分)
+F安(2分)
对棒有2 mg=
mg= + F安(3分)
+ F安(3分)
当框架刚开始运动时,对框架由牛顿第二定律得:
F一 mg=Ma(3分)
mg=Ma(3分)
解出a= (2分)
(2分)
(2)设框架做匀速运动的速度大小为 ,则感应电动势E=BL
,则感应电动势E=BL (2分)
(2分)
回路中的电流:I= (2分)
(2分)
对框架由力的平衡得:F=BIL+ mg (2分)
mg (2分)
联立以上各式解出: (2分)
(2分)
25.(20分)解:(1)粒子经过电场加速后,设进入磁场的速度为

 (3分)
(3分)
得: (1分)
(1分)
粒子在磁场中做圆周运动,设半径为r, (3分)
(3分)
得:r=2R (1分)
设粒子运动的圆心为点E,圆心角为2 ;
; (2分);
(2分);
∠CGF=2 ,FC=(4R一R)tan2
,FC=(4R一R)tan2 一3R×
一3R× (3 分);
(3 分);
 故F点坐标为(4R;4R)
故F点坐标为(4R;4R)
(2)当圆形磁场整体转动时,粒子做圆周运动的圆心和轨迹都不变。
当磁场区将粒子的轨迹覆盖最长时,即粒子在磁场中的圆弧轨迹
对应的弦长等于磁场的直径2R,此时粒子的出射速度与z轴的偏
角最大,粒子打在光屏上的点距C点最远。(3分)(若论证不充分,
只要图中画出圆形磁场的直径是粒子轨迹的弦,同样得分。)
△OBE为等边三角形,有:
得: (2分)
(2分)
故得最大距离: (2分)
(2分)
说明:计算题其它解法正确的均给分。

26.(14分) (1) (2分)
(2)C(2分) 原子晶体(2分)
(3)Cl2+2OH一=Cl一十ClO一+H2O (4分)
(4)阴(2分) 0.1(2分)
27.(14分)(1)过滤(2分),漏斗,玻璃棒(各1分,共2分)
(2)Cu(2分)
(3)因为Hg有挥发性,且有毒。(2分)
(4)Cu+H2O2+H2SO4=CuSO4+2H2O(4分)
(5)冷却结晶(或结晶)(2分)
28.(14分)(1)0.16(2分)
(2)>(3分),<(3分)
(3)b=
(4)B、C(2分)
29.(18分)(1)C7H6O4(2分) 羟基、羧基(每空1分,共2分) 
②保护酚羟基,防止其被氧化 (2分)
③a、b (2分)

30.(每空2分,共18分)
(3)实验步骤
I.②实验组 对照组
Ⅱ.②大小一致和饱满程度相同的黄豆种子 ③相同的环境下
(4)结果预测与分析
①A组的种子萌发数量和长度与B组相比都有所减少
②A组的种子萌发数量和长度与B组相比都有所增加
洗发水对种子萌发和生长都有一定的促进作用
③A组的种子萌发数量和长度与B组基本相同
洗发水对种子萌发和生长基本没有影响
31.(每空2分,共24分)
I.(1)黄毛、尾弯曲 黄毛、灰毛
(2)BB
(3)BbXTXt
(4) ①显性 ②体
(5)乙 乙突变体的蛋白质中氨基酸的改变比甲突变体可能更多(或:甲突变体的蛋
白质可能只有一个氨基酸发生改变,乙突变体的蛋白氨基酸序列可能从第一个氨
基酸后都改变)。
II.(1)O2释放 CO2吸收速率
(2)光照强度降低,光反应速率降低
“光斑”照耀期间积累的ATP和NADPH还可以使暗反应持续一段时间
(一)新制氢氧化铜悬浊液的配制与应用:
(1)实验室制取新制氢氧化铜悬浊液的操作方法:在试管里加入10%的________溶液2mL,滴入2%的
_________溶液4~6滴(以上选填“硫酸铜”或“氢氧化钠”),振荡即成。这样操作的目的_______________________________________________。
(2)下列各组物质的溶液仅用新制的氢氧化铜悬浊液(必要时可以加热)不能检验出来的是______。 A.HCOOCH3,C6H5COOH,C6H5CH2OH
B.NaHSO4,BaCl2,Na2CO3,酚酞
C.HCOOH,HCOONa,HCOOCH2CH3
D.葡萄糖,CH2OHCHOHCH2OH
(二)下列是四个研究性学习小组分别从不同层面开展研究性学习活动:
(3)研究性学习小组甲为了探究新制氢氧化铜与久置氢氧化铜氧化性的差异性,利用乙醛作还原剂,他们设计的方案是:取编号为X、Y的两支试管,分别装入一定量的新制氢氧化铜悬浊液和氢氧化铜沉淀,再分别加入3mL乙醛溶液,同时用水浴加热几分钟,结果X试管里出现砖红色沉淀,而Y试管出现黑色。你认为可能的原因是_____________________________________________________________。
(4)研究性学习小组乙对教材实验结论“乙醛与新制氢氧化铜反应生成的红色沉淀是Cu2O”提出质疑,他们认为红色沉淀不一定是Cu2O。为了确定红色沉淀的成分,开展了如下研究:
提出猜想:__________________________________________。
查阅资料:①Cu2O属于碱性氧化物;
②+1价的铜离子在酸性条件下易发生自身氧化还原反应;
③在空气中灼烧Cu2O会生成CuO。
设计方案:
方案1:取该红色沉淀溶于足量的稀硝酸中,观察溶液颜色变化。
方案2:取该红色沉淀溶于足量的稀硫酸中,观察是否有残渣。
方案3:称取红色沉淀a g,在空气中充分灼烧至完全变黑,并在干燥器里冷却,再称重,反复多次至到固体恒重,称得质量为b g,比较a,b关系。
方案4:取红色固体沉淀装入试管里,加入酸化的硝酸银溶液,观察是否有银白色银析出。
你认为合理的方案是_____________。
(5)研究性学习小组丙,设计新方案,装置如图所示。你认为要测定红色沉淀成分必须测定下列哪些物理量:____________________________。

(6)研究性学习小组丁上网查阅新闻得知,“2005年诺贝尔化学奖授予了三位研究绿色化学的科学家”。“变废为宝”符合绿色化学要求,因此他们想收集上述红色沉淀以制备化学试剂--蓝矾。
请你帮助他们设计一个实验方案:_________________________________________________________
B.氢气分子断键过程
C.氟化氢分子形成共H-F键的过程
D.氟和氢的原子核中质子运动
《新浪财经网》报道,“天然气能量的测定”国家标准已于
2008年12月31日发布,将于2009年8月1日起实施.它标志着在我国开展天然气能量计量将有标准可依,对我国天然气计量方式与国际惯例接轨提供了技术支持,在规范天然气能量的测定方法等方面具有积极的意义.天然气贸易交接计量的方式有按能量计量和按体积
(质量)计量两种.作为能源的天然气,人们关注的是它的热值.天然气是一种混合物气体,除烷烃以外还含有部分二氧化碳和氮气等不可燃物质,这些不可燃物质并不产生热值.所以,在贸易结算中,按体积计量的方式不符合按质论价、优质优价的商品交易原则,只有按能量计量才能科学合理地利用有限天然气资源,对供需双方都具有合理性.附:管道煤气中含有的烃类除甲烷外,还有少量乙烷、丙烷、丁烷等,它们的某些性质见下表.

根据以上阅读材料,用化学视角回答下列问题:
(1)天然气计量的方式有按能量计量和按体积(质量)计量两种,用能量计量方式更好的理由是________.
(2)管道煤气的主要成分是CO、H2和少量烃类,天然气的主要成分是CH4.试根据以上某个关键数据解释冬天严寒的季节有时管道煤气的火焰很小,并且呈断续状态的原因是________.
(3)若某管道煤气中CO和H2的体积比为1∶1,则同质量的管道煤气和纯天然气分别燃烧时放出热量较多的是________,完全燃烧时同体积的纯天然气放出的热量是管道煤气放出热量的________倍.
(4)现有10 L(在标准状况下)某种天然气,假设仅含甲烷和乙烷两种气体,燃烧时共放出热量546.9 kJ.则该天然气的化学式用CHx表示时,其x=________(保留一位小数),用CHx表示该气体燃烧的热化学方程式为________
________,该天然气中甲烷的体积分数为________.
CoCl2·6H2O是一种饲料营养强化剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种新工艺流程如下图:
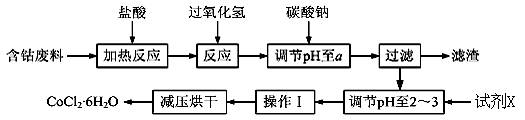
已知:
①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑[来源:学。科。网]
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
|
沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Co(OH)2 |
Al(OH)3 |
|
开始沉淀 |
2.3 |
7.5 |
7.6 |
3.4 |
|
完全沉淀 |
4.1 |
9.7 |
9.2 |
5.2 |
请回答下列问题:
(1)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为 。
(2)加入碳酸钠调节pH至a,a的范围是 ;pH调至a后过滤,再用试剂X将滤液的pH调节至2-3,则所用的试剂X为___________。
(3)操作Ⅰ包含3个基本实验操作,它们是 、 和过滤。
(4)制得的CoCl2·6H2O需减压烘干的原因是 。
(5)为测定产品中CoCl2·6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量。通过计算发现产品中CoCl2·6H2O的质量分数大于100%,其原因可能是 (写出两个原因)。
(6)在实验室中,为了从上述产品中获得纯净的CoCl2·6H2O,采用的方法是 。
查看习题详情和答案>>
 。[来源:学|科|网]
。[来源:学|科|网]
 。
。