摘要:例如:
网址:http://m.1010jiajiao.com/timu_id_471577[举报]
如图所示是电子工业中某原料的生产流程,其中反应②③是你在课本习题中见过,其目的是为了提纯B;物质A-H均为短周期元素组成;G为五原子非极性分子;A-D均是单质且元素原子的最外层电子数目的关系为C>A=B>D;H极易溶于水,且其水溶液为-种强酸.

请回答下列问题:
(1)B的电子排布式:
(2)反应①的化学方程式:
(3)与反应①类型相同,且两种单质分属同一主族和不同主族的反应,用化学方程式各写-例:
①单质属同-主族:
(4)F在工业上有多种用途,写出其中一种用途的化学方程式:
查看习题详情和答案>>

请回答下列问题:
(1)B的电子排布式:
1s22s22p63s23p2
1s22s22p63s23p2
;固体E的晶体类型原子晶体
原子晶体
;H中的键型为δ
δ
(填“π”或“δ”);(2)反应①的化学方程式:
SiO2+2C
Si+2CO↑
| ||
SiO2+2C
Si+2CO↑
.
| ||
(3)与反应①类型相同,且两种单质分属同一主族和不同主族的反应,用化学方程式各写-例:
①单质属同-主族:
2H2S+O2=2S↓+2H2O
2H2S+O2=2S↓+2H2O
;②单质属不同主族:2Mg+CO2
2MgO+C
| ||
2Mg+CO2
2MgO+C
.
| ||
(4)F在工业上有多种用途,写出其中一种用途的化学方程式:
3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
.
| ||
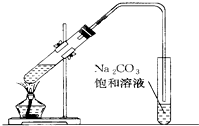 如图是实验室制取乙酸乙酯的装置.
如图是实验室制取乙酸乙酯的装置.(1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合溶液的方法是:
向试管倒入一定量的乙醇,然后边摇动试管边慢慢加入一定量的浓硫酸和一定量的醋酸
向试管倒入一定量的乙醇,然后边摇动试管边慢慢加入一定量的浓硫酸和一定量的醋酸
,并轻轻地振荡试管,使之混合均匀.反应方程式:CH3COOH+CH3CH2OH
CH3COOC2H5+H2O
| 浓硫酸 |
| 加热 |
CH3COOH+CH3CH2OH
CH3COOC2H5+H2O
.| 浓硫酸 |
| 加热 |
(2)装置中通蒸气的导管位置位于饱和Na2CO3溶液的液面上,不能插入溶液中,目的是
防止倒吸
防止倒吸
.(3)浓硫酸的作用是:
催化作用
催化作用
;吸水作用
吸水作用
.(4)饱和Na2CO3溶液的作用是
除去乙醇和乙酸、
除去乙醇和乙酸、
;降低乙酸乙酯的溶解度,便于分层
降低乙酸乙酯的溶解度,便于分层
.(5)实验中生成的乙酸乙酯,其密度比水
小
小
(填“大”或“小”),分离乙酸乙酯用到的主要玻璃仪器是分液漏斗
分液漏斗
.如图是某有色金属冶炼厂以某铜矿石(主要成分为Cu2S,且含有Fe、Zn硫化物)为原料冶炼铜的工艺流程,其冶炼过程中铜、硫回收率达到97%、87%.

(1)冶炼精铜矿制粗铜的主要反应方程式为 ,从提高资源利用率和减排考虑,烟气中的主要废气可综合利用其制备 .
(2)以硫酸铜溶液为介质电解精炼铜时,阴极上的电极反应式为 ;电解过程中,硫酸铜溶液的浓度会 (填“变大”“不变”或“变小”).
(3)在精炼铜的过程中,电解质溶液中c(Fe2+)、c(Zn2+) 会逐渐增大而影响进一步电解.几种物质的溶度积常数(Ksp)如下:
①调节电解液的pH是除去杂质离子的常用方法.根据上表中溶度积数据判断,含等物质的量浓度 Fe2+、Zn2+、Fe3+、Cu2+的溶液,随pH升高最先沉淀下来的离子是 .
②一种方案是先加入过量的H2O2,再调节pH到4左右,加入H2O2后发生反应的离子方程式为 .
(4)为测定某铁铜合金组成比例,某同学将一定量该合金样品与某浓度的稀硝酸反应,当加入硝酸10mL,剩余金属1.8g,生成NO(标况)0.224L;再加入硝酸10mL,剩余金属0.96g,又生成NO(标况)0.224L;此时溶液中的金属离子是 ,继续加入硝酸10mL,金属恰好全部溶解,又生成NO(标况)0.224L;则该合金中铁铜的物质的量之比为 .
查看习题详情和答案>>

(1)冶炼精铜矿制粗铜的主要反应方程式为
(2)以硫酸铜溶液为介质电解精炼铜时,阴极上的电极反应式为
(3)在精炼铜的过程中,电解质溶液中c(Fe2+)、c(Zn2+) 会逐渐增大而影响进一步电解.几种物质的溶度积常数(Ksp)如下:
| 物质 | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 |
| Ksp | 8.0×10-16 | 4.0×10-38 | 3.0×10-17 | 2.2×10-20 |
②一种方案是先加入过量的H2O2,再调节pH到4左右,加入H2O2后发生反应的离子方程式为
(4)为测定某铁铜合金组成比例,某同学将一定量该合金样品与某浓度的稀硝酸反应,当加入硝酸10mL,剩余金属1.8g,生成NO(标况)0.224L;再加入硝酸10mL,剩余金属0.96g,又生成NO(标况)0.224L;此时溶液中的金属离子是
如图所示是元素周期表中第一、第二周期10种元素的某些性质的一组数据(所列数据的单位相同),除带“…”的四种元素外,其余元素都给出了该种元素的全部该类数据.
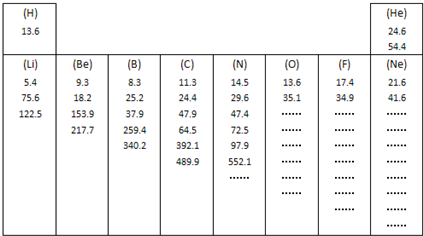
研究这些数据,回答下列问题:
(1)每组数据可能是该元素的 (填序号);
A.原子得到电子所放出的能量 B.原子半径的大小
C.原子逐个失去电子所吸收的能量 D.原子及形成不同分子的半径的大小
(2)分析同周期自左向右各元素的第一个数据:
①总体变化趋势是 (填“增大”或“减小”);
②与前后元素相比,由于该元素的数值增大较多而变得反常的元素位于元素周期表的 族;
③根据你分析所得的变化规律推测,镁和铝的第一个数据的大小关系为Mg(1) Al(1)(填“大于”或“小于”).
(3)分析每个元素的一组数据:
①有些元素的一组数据中个别地方增大的比例(倍数)特别大,形成“突跃”,由此可以证明原子结构中 的结论.
②根据这个规律,你认为氧元素8个数据中出现“突跃”的数据应该是第 个.
查看习题详情和答案>>

研究这些数据,回答下列问题:
(1)每组数据可能是该元素的
A.原子得到电子所放出的能量 B.原子半径的大小
C.原子逐个失去电子所吸收的能量 D.原子及形成不同分子的半径的大小
(2)分析同周期自左向右各元素的第一个数据:
①总体变化趋势是
②与前后元素相比,由于该元素的数值增大较多而变得反常的元素位于元素周期表的
③根据你分析所得的变化规律推测,镁和铝的第一个数据的大小关系为Mg(1)
(3)分析每个元素的一组数据:
①有些元素的一组数据中个别地方增大的比例(倍数)特别大,形成“突跃”,由此可以证明原子结构中
②根据这个规律,你认为氧元素8个数据中出现“突跃”的数据应该是第
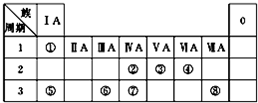 如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:(1)写出由④、⑤、⑧元素中形成的既含离子键又含共价键的一种离子化合物的电子式:
(2)含元素⑧的单质能与自来水中有机物反应生成对人体有危害的物质,现已逐步淘汰.
下列可代替它作自来水消毒剂的是
A.NH4Cl B.AlCl3 C.K2FeO4 D.ClO2
(3)W与④是相邻的同主族元素.在下表中列出H2WO3的各种不同化学性质,举例并写出相应的化学方程式:
| 编号 | 性质 | 化学方程式 |
| 示例 | 氧化性 | H2WO3+3H3PO3═3H3PO4+H2W↑ |
| Ⅰ | 酸性 | |
| Ⅱ | 还原性 |
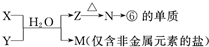
写出X溶液与Y溶液反应的离子方程式