摘要:[考题预测与专题训练] w.w.w.k.s.5.u.c.o.m
网址:http://m.1010jiajiao.com/timu_id_462298[举报]
1D。2D。3B。4BD。5BC。6BD。
13D(从离子的核外电子数之和为20可推出M、R两种原子的核外电子数之和为19,所以符合题示条件的M、R可能有多种答案。但M、R的质子数之差不可能是7)。
ⅠA
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
0
D
C
A
B
进而很容易判断出,原子序数的大小是B>A>C>D)。
16D。 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
17.PCl5、CH4、NaOH;Na2O2、MgF2
18. (1)镁、铝、氯、碳;
(3)Al3++3OH-===Al(OH)3↓;Al(OH)3+OH-==AlO2-+2H2O。
19.(1)C、D
(2)②;①③ (3) ; (4)KO2(其它合理的化学式也同样给分)。
; (4)KO2(其它合理的化学式也同样给分)。
 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
下表为元素周期表的一部分,请参照元素A-H在表中的位置,
族 周期 周期 | IA | | 0 | |||||
| 1 | A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | B | C | D | | |
| 3 | E | | F | G | | | H | |
(1)D、E、F的原子半径由大到小的顺序为_________________________。
(2)B、C、D的第一电离能由大到小的顺序为_________________________。
 (3)A、D、E、H中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(3)A、D、E、H中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。 (4) E、F的最高价氧化物的水化物相互反应的离子方程式
(4) E、F的最高价氧化物的水化物相互反应的离子方程式  。
。(5)在B所形成的化合物CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有 ;
与CO分子互为等电子体的分子和离
 子分别为 和 ,根据等电子理
子分别为 和 ,根据等电子理论推测CO分子的结构式可表示成 ,一个CO分子中有 个σ键, 个л键。
(6)根据VSEPR理论预测D和H所形成的HD4— 离子的空间构型为______________型。
(7)由A、B、C、D、E元素组成的10电子粒子中,含配位键的有 、 ; 查看习题详情和答案>>
【化学--选修3物质结构与性质】
W、Y、Z、Q、R是周期表中前四周期的元素,且原子序数依次增大.W原子核外有2个未成对电子,Q是电负性最大的元素,R元素的原子核外的未成对电子数是W原子核外未成对电子数的2倍.请回答下列问题(答题时,W、Y、Z、Q、R用所对应的元素符号表示):
(l)W、Y、Z 三种元素的第一电离能由大到小的顺序为 .在上述三种元素的原子中,写出与WZ2互为等电子体的分子式 .
(2)已知Y2Q2分子存在如下所示的两种结构(球棍模型,短线不一定代表单键)
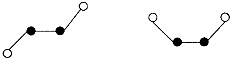
该分子中Y原子的杂化方式是 杂化.
(3)W2-2阴离子的电子式为 ,Z原子最外层电子排布式为 .
(4)YQ3分子的空间构型为 ,Y和Q两元素的氢化物的沸点相比较,高者是 (写分子式).往硫酸铜溶液中通入过量的YH3(Y的氢化物分子式),可生成配离子[Cu(YH3)4]2+,但YQ3不易与Cu2+形成配离子,其原因是 .
(5)科学家通过X射线探明RZ的晶体结构与NaCl晶体结构相似.那么在RZ晶体中距离R2+最近且等距离的R2+有 个.若在RZ晶体中阴阳离子间最近距离为a cm,晶体密度为ρg/cm3,则阿伏伽德罗常数NA的表达式为 mol-1.
(6)已知非整数比化合物R0.95Z,其晶体结构与NaCI相似,但由于R、Z离子个数比小于1:1,故晶体存在缺陷.R0.95Z可表示为
A、R
R
Z B、R
R
Z C、R
R
Z D、Fe2+0.85Fe3+0.1O.
查看习题详情和答案>>
W、Y、Z、Q、R是周期表中前四周期的元素,且原子序数依次增大.W原子核外有2个未成对电子,Q是电负性最大的元素,R元素的原子核外的未成对电子数是W原子核外未成对电子数的2倍.请回答下列问题(答题时,W、Y、Z、Q、R用所对应的元素符号表示):
(l)W、Y、Z 三种元素的第一电离能由大到小的顺序为
(2)已知Y2Q2分子存在如下所示的两种结构(球棍模型,短线不一定代表单键)
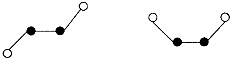
该分子中Y原子的杂化方式是
(3)W2-2阴离子的电子式为
(4)YQ3分子的空间构型为
(5)科学家通过X射线探明RZ的晶体结构与NaCl晶体结构相似.那么在RZ晶体中距离R2+最近且等距离的R2+有
(6)已知非整数比化合物R0.95Z,其晶体结构与NaCI相似,但由于R、Z离子个数比小于1:1,故晶体存在缺陷.R0.95Z可表示为
A、R
2+ 0.45 |
3+ 0.5 |
2+ 0.25 |
3+ 0.70 |
2+ 0.15 |
3+ 0.80 |
某矿石由前20号元素中的4种组成,其化学式为WYZX4.X、Y、Z、W分布在三个周期,原子序数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,W能与冷水剧烈反应,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等,Y、Z位于同周期,Z单质是一种良好的半导体.下列说法正确的是( )
查看习题详情和答案>>

