摘要:离子方程式正误:①看电荷是否守恒 ②看物质拆分中否正确.只有强酸.强碱.可溶性盐可拆.其它一律不拆 ③看产物是否正确.如CO2的反应是生成正盐还是酸式盐.Fe3+与S2-反应是氧化还原反应等 ④看原子是否守恒 ⑤水解与电离方程式要看准.不要被反应物有水所迷惑.
网址:http://m.1010jiajiao.com/timu_id_455666[举报]
(2011?新余二模)下表选项中对规定反应的离子方程式的评价合理的是( )
|
查看习题详情和答案>>
下表选项中对规定反应的离子方程式的评价合理的是( )
查看习题详情和答案>>
| 选项 | 反应 | 离子方程式 | 评价 |
| A | FeI2和Cl2以5:7的物质的量比反应 | 4Fe2++10I一+7Cl2=4Fe3++5I2+14Cl一 | 正确 |
B |
碳酸氢钠溶液与足量 的氢氧化钡溶液反应 |
Ba2++20H一+2HC03=BaC03↓+C032-+2H20 | 正确 |
| C | 金属Na和CuS04溶 液反应 |
Na+Cu2+=Na++Cu | 错误.离子方程式不 符合电荷守恒原则 |
D |
过量二氧化碳通入次 氯酸钙溶液中反应 |
2Cl0一+H20+C02=2HCl0+CO32- | 错误.生成物碳酸钙 不应写成离子形式 |
| A.A | B.B | C.C | D.D |
下列对离子方程式书写评价正确的是( )
查看习题详情和答案>>
| 选项 | 化学反应与离子方程式 | 评价 | |||||||||||||
| A | 将铜屑加入Fe3+溶液中:Fe3++Cu
|
正确 | |||||||||||||
| B | Na2O2与H2O反应Na2O2+H2O
|
错误,氧元素不守恒 | |||||||||||||
| C | NaOH溶液与氧化铝反应:Al2O3+2OH-
|
错误,产物应该是Al(OH
| |||||||||||||
| D | 向Fe(OH
|
正确 |
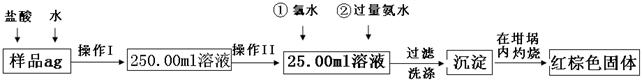
(12分)某氧化铁样品中含有少量的FeCl2杂质。现要测定其中铁元素的质量分数,按以下步骤进行实验:
请根据图的流程,回答下列问题:
⑴操作I的目的为配制250.00ml样品溶液,则所用到玻璃仪器除烧杯、玻璃棒、胶头滴管以外,还必须有 (填仪器名称);操作II必须用到的仪器是 。(填字母)
| A.50ml烧杯 | B.50ml量筒 | C.100ml量筒 | D.25ml滴定管 |
⑵再加入氨水的离子方程式为 。
⑶检验沉淀是否洗涤干净的操作是
。
⑷将沉淀物加热,冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1—b2=0.3,则接下来还应进行的操作是 。
⑸若坩埚的质量为W1g,坩埚与加热后固体的总质量为W2g,则样品中铁元素的质量分数是 。
⑹有学生认为上述实验步骤太繁琐,他认为,将样品溶于水后充分搅拌,在空气中加热蒸干燃烧称量即可,请你评价是否可行? 。(填“可行”或“不可行”) 查看习题详情和答案>>