摘要: "m%K;~:V"[-I-n5N#^记忆法,记忆方法,英语单词记忆,如何提高记忆力,记忆培训,速读,思维导图,脑潜能$F$K%Z#L#E+w.T)H)U"o记忆法|记忆方法|图像记忆|海马记忆|英语单词记忆|记忆培训|速读|思维导图|右脑开发过量的铜投入盛有浓硫酸的试管.并加热.反应毕.待容易冷却后加水.有刺激性气味的气体生成.加水后溶液成天蓝色
网址:http://m.1010jiajiao.com/timu_id_455589[举报]
 已知A、B、C、D、E五种元素的核电荷数依次增大,除E为第四周期元素外,其余都是短周期元素.其中A、B、C是同一周期的非金属元素,A元素最外层电子数是内层电子数的2倍,B元素基态原子的最外层有3个未成对电子,化合物DC的晶体中,D的二价阳离子与C的阴离子具有相同的电子层结构,E元素的正三价离子的3d能级为半充满状态.请根据上述情况,回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
已知A、B、C、D、E五种元素的核电荷数依次增大,除E为第四周期元素外,其余都是短周期元素.其中A、B、C是同一周期的非金属元素,A元素最外层电子数是内层电子数的2倍,B元素基态原子的最外层有3个未成对电子,化合物DC的晶体中,D的二价阳离子与C的阴离子具有相同的电子层结构,E元素的正三价离子的3d能级为半充满状态.请根据上述情况,回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):(1)元素B、C的第一电离能的大小关系是
N>O
N>O
.(2)A的氢化物:A2H4分子中,A原子采取的杂化形式为
sp2杂化
sp2杂化
,分子中含有5
5
个σ键和1
1
个π键,键角是1200
1200
.(3)单质D和铝的混合粉末mg,与足量氢氧化钠浓溶液充分反应,生成标准状况下气体的体积为VL,则混合粉末中单质D的质量百分数是
m-
| ||
| m |
m-
| ||
| m |
(4)由E元素形成的金属的晶胞结构如图,则该晶胞中含有金属原子的数目为
2
2
,已知该晶胞中E元素的相对原子质量为Mg/mol,任意两个相邻距离最近E的核间距为acm,这种金属的密度是| 2M |
| (a)3NA |
| 2M |
| (a)3NA |
碱式碳酸铜[Cu2(OH)2CO3]是孔雀石的主要成分,加热时可分解为氧化铜、二氧化碳和水三种氧化物.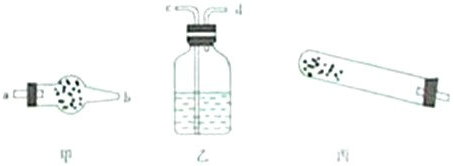
(1)若用如图所示仪器对分解产物中的非固体氧化物进行验证.则碱式碳酸铜应该放在
(2)将碱式碳酸铜与过量的木炭混合加热,可能得到铜、一氧化碳和水三种物质,该反应的化学方程式是
(3)铜及其合金用途广泛,常见的铜的合金有黄铜(铜锌合金)、青铜(铜锡合金).现有w g黄铜样品,放入足量的橘盐酸中,产生V mL气体(标准状况下),则样品中铜和锌的物质的量之比是
(用含m、V的代数式表示).
查看习题详情和答案>>

(1)若用如图所示仪器对分解产物中的非固体氧化物进行验证.则碱式碳酸铜应该放在
丙
丙
中(填甲、乙、丙),且还需使用的玻璃仪器是酒精灯
酒精灯
.(2)将碱式碳酸铜与过量的木炭混合加热,可能得到铜、一氧化碳和水三种物质,该反应的化学方程式是
4C+Cu2(OH)2CO3
2Cu+4CO↑+H20↑
| ||
4C+Cu2(OH)2CO3
2Cu+4CO↑+H20↑
.
| ||
(3)铜及其合金用途广泛,常见的铜的合金有黄铜(铜锌合金)、青铜(铜锡合金).现有w g黄铜样品,放入足量的橘盐酸中,产生V mL气体(标准状况下),则样品中铜和锌的物质的量之比是
| 22400w-65V |
| 64V |
| 22400w-65V |
| 64V |
聚合硫酸铁(PFS)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理.现用一定质量的铁的氧化物(如下图)为原料来制取聚合硫酸铁,为控制水解时Fe3+的浓度,防止生成氢氧化铁沉淀,原料中的Fe3+必须先还原为Fe2+.实验步骤如下:
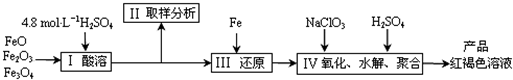
(1)实验室用18.4mol?L-1的浓硫酸配制250mL4.8mol?L-1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种带有刻度的移液管)外,还需
(2)步骤Ⅱ取样分析溶液中的Fe2+、Fe3+的含量,目的是
A.控制溶液中Fe2+与Fe3+含量比 B.确定下一步还原所需铁的量
C.确定氧化Fe2+所需NaClO3的量 D.确保铁的氧化物酸溶完全
(3)写出步骤Ⅳ中用NaClO3氧化时的离子方程式
已知1mol HNO3的价格为0.16元,1mol NaClO3的价格为0.45元,评价用HNO3代替NaClO3作为氧化剂的利弊,利是
(4)为了分析产品聚合硫酸铁溶液中SO42-与Fe3+物质的量之比,有人设计了以下操作:
(a)取25mL聚合硫酸铁溶液,加入足量的BaCl2溶液,产生白色沉淀,白色沉淀经过过滤、洗涤、干燥后,称重,其质量为m g.
(b)另取25mL聚合硫酸铁溶液,加足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并配成250mL溶液,取该溶液25.00mL,用KMnO4酸性溶液滴定,到达终点时用去0.1000mol/L KMnO4标准溶液VmL.反应的离子方程式为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
回答下列问题:
①判断(a)步骤溶液中SO42-离子已沉淀完全的方法是
②在(b)步骤中判断达到终点的现象是
③聚合硫酸铁中SO42-与Fe3+的物质的量之比为
=
=
(用含m、V的代数式表示).
查看习题详情和答案>>

(1)实验室用18.4mol?L-1的浓硫酸配制250mL4.8mol?L-1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种带有刻度的移液管)外,还需
250mL容量瓶、胶头滴管
250mL容量瓶、胶头滴管
.(2)步骤Ⅱ取样分析溶液中的Fe2+、Fe3+的含量,目的是
BC
BC
.A.控制溶液中Fe2+与Fe3+含量比 B.确定下一步还原所需铁的量
C.确定氧化Fe2+所需NaClO3的量 D.确保铁的氧化物酸溶完全
(3)写出步骤Ⅳ中用NaClO3氧化时的离子方程式
6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O
6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O
(提示:ClO3-转化为Cl-);已知1mol HNO3的价格为0.16元,1mol NaClO3的价格为0.45元,评价用HNO3代替NaClO3作为氧化剂的利弊,利是
原料成本较低
原料成本较低
,弊是产生气体对大气有污染
产生气体对大气有污染
.(4)为了分析产品聚合硫酸铁溶液中SO42-与Fe3+物质的量之比,有人设计了以下操作:
(a)取25mL聚合硫酸铁溶液,加入足量的BaCl2溶液,产生白色沉淀,白色沉淀经过过滤、洗涤、干燥后,称重,其质量为m g.
(b)另取25mL聚合硫酸铁溶液,加足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并配成250mL溶液,取该溶液25.00mL,用KMnO4酸性溶液滴定,到达终点时用去0.1000mol/L KMnO4标准溶液VmL.反应的离子方程式为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
回答下列问题:
①判断(a)步骤溶液中SO42-离子已沉淀完全的方法是
取上层清夜,滴加BaCl2溶液,若无沉淀产生,则溶液中SO42-已沉淀完全
取上层清夜,滴加BaCl2溶液,若无沉淀产生,则溶液中SO42-已沉淀完全
;②在(b)步骤中判断达到终点的现象是
溶液由浅蓝色变为浅紫红色,且半分钟内不变色
溶液由浅蓝色变为浅紫红色,且半分钟内不变色
;③聚合硫酸铁中SO42-与Fe3+的物质的量之比为
| m |
| 233 |
| V |
| 200 |
| m |
| 233 |
| V |
| 200 |
 某化学兴趣小组用如图所示装置电解CuSO4溶液,测定铜的相对分子质量.
某化学兴趣小组用如图所示装置电解CuSO4溶液,测定铜的相对分子质量.(1)若实验中测定在标准状况下放出的氧气的体积VL,A连接直流电源的
负极
负极
(填“正极”或“负极”).(2)电解开始一段时间后,在U形管中可观察到的现象有
铜电极上有红色固体析出,石墨电极上有无色气体产生,溶液蓝色变浅
铜电极上有红色固体析出,石墨电极上有无色气体产生,溶液蓝色变浅
.电解的离子方程式为2Cu2++2H2O
2Cu+O2↑+4H+
| ||
2Cu2++2H2O
2Cu+O2↑+4H+
.
| ||
(3)实验中还需测定的数据是
①
①
(填写序号).①A极的质量增重m g ②B极的质量增重m g
(4)下列实验操作中必要的是
ABDE
ABDE
(填字母).A.称量电解前电极的质量
B.电解后,电极在烘干称重前,必须用蒸馏水冲洗
C.刮下电解过程中电极上析出的铜,并清洗、称重
D.电极在烘干称重的操作中必须按“烘干-称重一再烘干一再称重”进行
E.在有空气存在的情况下,烘干电极必须采用低温烘干的方法
(5)铜的相对原子质量为:
| 11.2m |
| M |
| 11.2m |
| M |
(6)如果用碱性(KOH为电解质)甲醇燃料电池作为电源进行实验,放电时负极的电极反应式为
CH3OH-6e-+8OH-=CO32-+6H2O
CH3OH-6e-+8OH-=CO32-+6H2O
.