网址:http://m.1010jiajiao.com/timu_id_455534[举报]
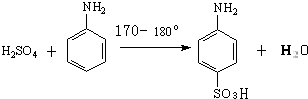
主要试剂及产品的物理常数:
| 名称 | 性状 | 熔点/°C | 沸点/°C | 在水中的溶解度(g/100mL) |
| 苯胺 | 无色油状液体 | -6.1 | 184.4 | 3.6/18℃ |
| 对氨基苯磺酸 | 无色结晶 | 熔点365°C;内盐280~290°C | 0.8/10℃;1.08/20℃;6.67/100℃ | |

①在一个250mL三颈烧瓶中加入10mL苯胺及几粒沸石,将三颈 烧瓶放入冷水中冷却,小心地加入18mL浓硫酸.如图所示,在三颈烧瓶的两个瓶口上分别装冷凝管、温度计(水银球浸入反应液中),另一个没有使用的瓶口用塞子塞紧.
②将三颈烧瓶置于
③将反应产物冷却至约50℃后,倒入盛有100mL冷水的烧杯中,用玻璃棒不断搅拌,促使对氨基苯磺酸晶体析出.用该烧杯中的少量冷水将烧瓶内残留的产物冲洗到烧杯中,抽滤,用少量冷水洗涤,得到的晶体是对氨基苯磺酸粗产品.
④为提高产品的纯度,将粗产品先
请回答下列问题:
(1)装置中冷凝管的作用是
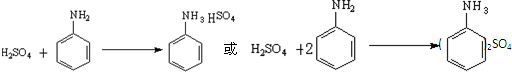

(2)步骤②中采用
(3)步骤③用少量冷水洗涤晶体的好处是
(4)步骤③和④均进行抽滤操作,在抽滤完毕停止抽滤时,应注意先
(5)步骤④中将粗产品先

主要试剂及产品的物理常数:
| 名称 | 性状 | 熔点/°C | 沸点/°C | 在水中的溶解度(g/100mL) |
| 苯胺 | 无色油状液体 | -6.1 | 184.4 | 3.6/18℃ |
| 对氨基苯磺酸 | 无色结晶 | 熔点365°C;内盐280~290°C | 0.8/10℃;1.08/20℃;6.67/100℃ | |

①在一个250mL三颈烧瓶中加入10mL苯胺及几粒沸石,将三颈 烧瓶放入冷水中冷却,小心地加入18mL浓硫酸.如图所示,在三颈烧瓶的两个瓶口上分别装冷凝管、温度计(水银球浸入反应液中),另一个没有使用的瓶口用塞子塞紧.
②将三颈烧瓶置于______中加热至170~180℃,维持此温度2~2.5h.
③将反应产物冷却至约50℃后,倒入盛有100mL冷水的烧杯中,用玻璃棒不断搅拌,促使对氨基苯磺酸晶体析出.用该烧杯中的少量冷水将烧瓶内残留的产物冲洗到烧杯中,抽滤,用少量冷水洗涤,得到的晶体是对氨基苯磺酸粗产品.
④为提高产品的纯度,将粗产品先______,再______,抽滤,收集产品,晾干.
请回答下列问题:
(1)装置中冷凝管的作用是______,冷却水应从______口(填“a”或“b”)处通入,加入浓硫酸时烧瓶中出现白烟,杯壁上出现白色块状物,写出其反应方程式:______.
(2)步骤②中采用______加热,这种加热方法的优点是______.
(3)步骤③用少量冷水洗涤晶体的好处是______.
(4)步骤③和④均进行抽滤操作,在抽滤完毕停止抽滤时,应注意先______,然后______,以防倒吸.
(5)步骤④中将粗产品先______,再______,抽滤,收集产品,晾干,以提高对氨基苯磺酸的纯度.每次抽滤后均应将母液收集起来,再进行适当处理,其目的是______.

主要试剂及产品的物理常数:
| 名称 | 性状 | 熔点/°C | 沸点/°C | 在水中的溶解度(g/100mL) |
| 苯胺 | 无色油状液体 | -6.1 | 184.4 | 3.6/18℃ |
| 对氨基苯磺酸 | 无色结晶 | 熔点365°C;内盐280~290°C | 0.8/10℃;1.08/20℃;6.67/100℃ | |

①在一个250mL三颈烧瓶中加入10mL苯胺及几粒沸石,将三颈 烧瓶放入冷水中冷却,小心地加入18mL浓硫酸.如图所示,在三颈烧瓶的两个瓶口上分别装冷凝管、温度计(水银球浸入反应液中),另一个没有使用的瓶口用塞子塞紧.
②将三颈烧瓶置于______中加热至170~180℃,维持此温度2~2.5h.
③将反应产物冷却至约50℃后,倒入盛有100mL冷水的烧杯中,用玻璃棒不断搅拌,促使对氨基苯磺酸晶体析出.用该烧杯中的少量冷水将烧瓶内残留的产物冲洗到烧杯中,抽滤,用少量冷水洗涤,得到的晶体是对氨基苯磺酸粗产品.
④为提高产品的纯度,将粗产品先______,再______,抽滤,收集产品,晾干.
请回答下列问题:
(1)装置中冷凝管的作用是______,冷却水应从______口(填“a”或“b”)处通入,加入浓硫酸时烧瓶中出现白烟,杯壁上出现白色块状物,写出其反应方程式:______.
(2)步骤②中采用______加热,这种加热方法的优点是______.
(3)步骤③用少量冷水洗涤晶体的好处是______.
(4)步骤③和④均进行抽滤操作,在抽滤完毕停止抽滤时,应注意先______,然后______,以防倒吸.
(5)步骤④中将粗产品先______,再______,抽滤,收集产品,晾干,以提高对氨基苯磺酸的纯度.每次抽滤后均应将母液收集起来,再进行适当处理,其目的是______.
查看习题详情和答案>>
某实验小组对FeCl3的性质和用途展开了实验。
实验一:
实验步骤
①往锥形瓶中加入50 mL、3.0%的双氧水。
②分别往锥形瓶中加0.5 g不同的催化剂粉末,立即塞上橡皮塞。
③采集和记录数据。
④整理数据得出下表。
表:不同催化剂催化双氧水分解产生O2的压强对反应时间的斜率
| 催化剂 | 氯化铁 | 二氧化锰 | 猪肝 | 马铃薯 |
| 压强对时间的斜率 | 0.0605 | 3.8214 | 0.3981 | 0.0049 |
(1)该“实验一”的实验名称是 ;
(2)催化效果最好的催化剂是 ;
实验二:氯化铁催化分解双氧水的最佳条件
该实验小组的同学在进行实验二时,得到了如下的数据。
表:不同浓度的双氧水在不同用量的FeCl3?6H2O作用下完全反应所需时间
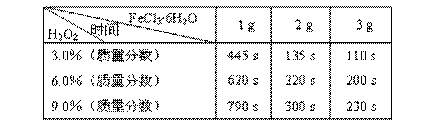
分析表中数据我们可以得出:
(3)如果从实验结果和节省药品的角度综合分析,当选用6.0%的双氧水时,加入______g FeCl3?6H2O能使实验效果最佳;
(4)进行该实验时,控制不变的因素有反应温度、 等;
(5)如图是2 gFeCl3?6H2O催化分解50 ml3.0%的双氧水时收集到的O2体积对反应时间示意图,请分别画出相同条件下1 g、3 g FeCl3?6H2O催化分解50 ml3.0%的双氧水时收集到的同温同压下O2体积对反应时间示意图,并作必要的标注;

讨论:有关FeCl3参加的可逆反应的两个问题:
(6)分别取若干毫升稀FeCl3溶液与稀KSCN
溶液混合,溶液呈血红色。限用FeCl3、KSCN、
KCl三种试剂,仪器不限,为证明FeCl3溶液与
KSCN溶液的反应是一个可逆反应,至少还要进行
次实验;
(7)一定浓度的FeCl3与KSCN两溶液反应达到平衡,在t1时刻加入一些FeCl3固体,反应重新达到平衡。若其反应过程可用如下的速率v―时间t图像表示。

请根据此图像和平衡移动规律求证新平衡下FeCl3的浓度比原平衡大
。
查看习题详情和答案>>A:
合成氨是人类科学技术上的一项重大突破,是化学和技术对社会发展与进步的巨大贡献之一.在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒.除去CO的化学反应方程式(HAc表示醋酸):Cu(NH3)2Ac+CO+NH3=Cu(NH3)3(CO)Ac
请回答下列问题:
(1)C、N、O的第一电离能由大到小的顺序为
(2)写出基态Cu+的核外电子排布式
(3)配合物Cu(NH3)3(CO)Ac中心原子的配位数为
(4)写出与CO互为等电子体的离子
(5)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],尿素中 C原子轨道的杂化类型分别为
(6)铜金合金形成的晶胞如图1所示,其中Cu、Au原子个数比为
B:
对氨基苯磺酸是制取染料和一些药物的重要中间体,可由苯胺磺化得到.
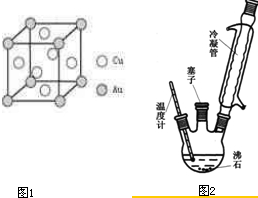
实验室可利用如图2实验装置合成对氨基苯磺酸.实验步骤如下:
1在一个250mL三颈烧瓶中加入10mL苯胺及几粒沸石,将三颈烧瓶放入冷水中冷却,小心地加入18mL浓硫酸.
2将三颈烧瓶置于油浴中缓慢加热至170~180℃,维持此温度2~2.5h.
③将反应液冷却至约50℃后,倒入盛有100mL冷水的烧杯中,用玻璃棒不断搅拌,促使晶体析出,抽滤,用少量冷水洗涤,得到的晶体是对氨基苯磺酸粗产品.
④将粗产品用沸水溶解,冷却结晶(若溶液颜色过深,可用活性炭脱色),抽滤,收集产品,晾干.(说明:100mL水在20℃时可溶解对氨基苯磺酸1.08g,在100℃时可溶解6.67g.)
试回答填空.
(1)装置中冷凝管的作用是
(2)步骤②中采用油浴加热,下列说法正确的是
A.用油浴加热的好处是反应物受热均匀,便于控制温度
B.此处也可以改用水浴加热
C.实验装置中的温度计可以改变位置,也可使其水银球浸入在油中
(3)步骤③用少量冷水洗涤晶体的好处是
(4)步骤③和④均进行抽滤操作,在抽滤完毕停止抽滤时,应注意先
(5)步骤④中有时需要将“粗产品用沸水溶解,冷却结晶,抽滤”的操作进行多次,其目的是