摘要: 配制FeCl3.SnCl2等易水解的盐溶液时.先溶于少量浓盐酸中.再稀释.
网址:http://m.1010jiajiao.com/timu_id_455518[举报]
(2012?深圳二模)钛(Ti)具有高强度和耐酸腐蚀性,是重要的工业原料.以金红石(主要成分为TiO2,含少量Fe2O3、SiO2)为原料可制取Ti.工业流程如下:

(1)粗TiCl4中含有少量FeCl3、SiCl4等,它们的部分性质如下:
从粗TiCl4中精制TiCl4的方法是
(2)写出金红石高温反应制取TiCl4的化学方程式
(3)写出电解熔融NaCl的化学方程式
(4)粗钛产品粉碎后要用盐酸浸洗.其主要目的是
(5)Ti可溶解在浓HF溶液中,请完成下列离子方程式.
查看习题详情和答案>>

(1)粗TiCl4中含有少量FeCl3、SiCl4等,它们的部分性质如下:
| 物质 | 沸点/°C | 在水中 | 在乙醚中 |
| TiCl4 | 136 | 强烈水解 | 易溶 |
| SiCl4 | 58 | 强烈水解 | 易溶 |
| FeCl3 | 303(升华) | 水解 | 易溶 |
B
B
A.用水溶解后,重结晶 B.蒸馏 C.用乙醚萃取后,分液(2)写出金红石高温反应制取TiCl4的化学方程式
TiO2+2C+2Cl2
TiCl4+2CO
| ||
TiO2+2C+2Cl2
TiCl4+2CO
.
| ||
(3)写出电解熔融NaCl的化学方程式
2NaCl (熔融)
2Na+Cl2↑
| ||
2NaCl (熔融)
2Na+Cl2↑
;阴极产物是
| ||
钠
钠
.(4)粗钛产品粉碎后要用盐酸浸洗.其主要目的是
除去粗钛产品中剩余的少量钠,促进NaCl晶体析出(Cl-同离子效应)
除去粗钛产品中剩余的少量钠,促进NaCl晶体析出(Cl-同离子效应)
.(5)Ti可溶解在浓HF溶液中,请完成下列离子方程式.
1
1
Ti+6
6
HF-1
1
TiF62-+2(H+)
2(H+)
+2
2
H2↑(2013?泰安三模)钛(Ti)具有高强度和耐酸腐蚀性,是重要的工业原料.以金红石(主要成分为TiO2,含少量Fe2O3、SiO2)为原料可制取Ti.工业流程如图1所示:

(1)粗TiC14中含有少量FeCl3、SiCl4等,它们的部分性质如下:
从粗TiC14中精制TiC14的方法是
(2)写出用惰性电极电解熔融NaCl时阳极的电极反应式:
(3)Ti可溶解在浓HF溶液中,请完成下列离子方程式:
+
(4)如图2所示是一个制取氯气并以氯气为原料进行反应的装置.
①装置A中发生反应的化学方程式为
②在实验室中,某同学欲用如图3所示装置净化氯气,则M、N中应盛放的试剂分别是
③实验开始时,先点燃A处的酒精灯,打开旋塞K,让C12充满整个装置,再点燃C处酒精灯.Cl2通过装置M、N再进入装置C,与装置C中的固体粉末发生氧化还原反应生成CO气体.试写出装置C中发生反应的化学方程式:
查看习题详情和答案>>

(1)粗TiC14中含有少量FeCl3、SiCl4等,它们的部分性质如下:
| 物质 | 沸点/℃ | 在水中 | 在乙醚中 |
| TiC14 | 136 | 强烈水解 | 易溶 |
| SiCl4 | 58 | 强烈水解 | 易溶 |
| FeCl3 | 303(升华) | 水解 | 易溶 |
B
B
(填字母).A.用水溶解后,重结晶 B.蒸馏 C.用乙醚萃取后,分液(2)写出用惰性电极电解熔融NaCl时阳极的电极反应式:
2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
;阴极产物是钠
钠
.(3)Ti可溶解在浓HF溶液中,请完成下列离子方程式:
1
1
Ti+6
6
HF═1
1
Ti| F | 2- 6 |
2
2
H+
H+
+2
2
H2↑(4)如图2所示是一个制取氯气并以氯气为原料进行反应的装置.
①装置A中发生反应的化学方程式为
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
.
| ||
②在实验室中,某同学欲用如图3所示装置净化氯气,则M、N中应盛放的试剂分别是
饱和食盐水
饱和食盐水
、浓硫酸
浓硫酸
.(填试剂名称)③实验开始时,先点燃A处的酒精灯,打开旋塞K,让C12充满整个装置,再点燃C处酒精灯.Cl2通过装置M、N再进入装置C,与装置C中的固体粉末发生氧化还原反应生成CO气体.试写出装置C中发生反应的化学方程式:
TiO2+2Cl2+2C
TiCl4+2CO
| ||
TiO2+2Cl2+2C
TiCl4+2CO
.
| ||
钛(Ti)具有高强度和耐酸腐蚀性,是重要的工业原料,以金红石(主要成份为TiO2,含有少量Fe2O3、SiO2)为原料可制取Ti.工业流程如下:
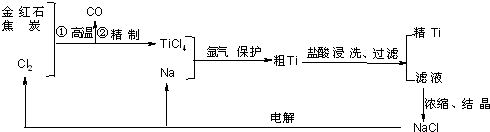
(1)粗TiCl4中含有少量FeCl3、SiCl4等,它们的部分性质如下:
从粗TiCl4 中精制TiCl4 的方法是:
A.用水溶解后,重结晶 B.蒸馏 C.用乙醚萃取后,分液
(2)写出金红石高温反应制取TiCl4 的化学方程式 .
(3)写出电解熔融NaCl的化学方程式 .
(4)粗钛产品粉碎后用盐酸浸洗.其主要目的是 , .
(5)Ti可以溶解在浓HF溶液中,请完成下列离子方程式.
Ti+ HF═ TiF62-+ + H2↑
查看习题详情和答案>>

(1)粗TiCl4中含有少量FeCl3、SiCl4等,它们的部分性质如下:
| 物质 | 沸点/℃ | 在水中 | 在乙醚中 |
| TiCl4 | 136 | 强烈水解 | 易溶 |
| SiCl4 | 58 | 强烈水解 | 易溶 |
| FeCl3 | 303(升华) | 水解 | 易溶 |
A.用水溶解后,重结晶 B.蒸馏 C.用乙醚萃取后,分液
(2)写出金红石高温反应制取TiCl4 的化学方程式
(3)写出电解熔融NaCl的化学方程式
(4)粗钛产品粉碎后用盐酸浸洗.其主要目的是
(5)Ti可以溶解在浓HF溶液中,请完成下列离子方程式.