网址:http://m.1010jiajiao.com/timu_id_455426[举报]
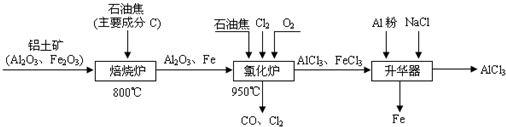
 A、B、C、D都是中学化学中的常见物质,具有如图所示的转化关系(反应条件,其他反应物及多余产物均已略去):
A、B、C、D都是中学化学中的常见物质,具有如图所示的转化关系(反应条件,其他反应物及多余产物均已略去):(1)若A是一种白色难溶于水的钙盐,由三种元素组成,C是一种参与植物光合作用的气体.按要求写出下列物质化学式或反应式:
B
(2)若A是一种无色液体,D是一种金属氧化物,其相对分子质量为232,其中金属元素和氧元素的质量比为21:8.按要求写出下列物质化学式或反应式:B
| ||
| ||

(1)已知:C(s)+
| 1 |
| 2 |
| 3 |
| 2 |
请写出C还原Fe2O3生成CO的热化学方程式
(2)反应2CO+O2
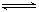 2CO2的平衡常数为K1;反应4Fe+3O2
2CO2的平衡常数为K1;反应4Fe+3O2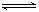 2Fe2O3的平衡常数K2,则反应3CO+Fe2O3
2Fe2O3的平衡常数K2,则反应3CO+Fe2O3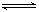 2Fe+3CO2的平衡常数K与K1、K2的关系式
2Fe+3CO2的平衡常数K与K1、K2的关系式
|
|
(3)高温下,氧化铁能跟碳发生下列反应:
①Fe2O3+3C
| ||
| ||
| n(C) |
| n(Fe2O3) |
| n(C) |
| n(Fe2O3) |
| n(C) |
| n(Fe2O3) |
(4)氯化炉中生成的气体,通常用碱性的亚硫酸钠溶液来吸收,请用离子方程式分析亚硫酸钠溶液呈碱性的原因
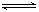 HSO3-+OH-
HSO3-+OH-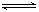 HSO3-+OH-
HSO3-+OH-(5)氯化炉中发生:3Cl2(g)+3C(s)+Al2O3(s)
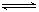 2AlCl3(g)+3CO(g)△H>0,欲提高金属铝的氯化效果,不可采取的措施是
2AlCl3(g)+3CO(g)△H>0,欲提高金属铝的氯化效果,不可采取的措施是①增加C的量 ②多通入Cl2③升高温度 ④移走部分AlCl3(g) ⑤使用合适的催化剂工业上还常采用向氯化炉中通入O2的方法,其目的是
(6)沉淀分析法一般规定:溶液中某离子物质的量浓度低于1.0×10-5mol/L时,可认为已沉淀完全.现向一定浓度的AlCl3和FeCl3的混合溶液中逐滴加入氨水,当Fe3+完全沉淀时,测定c(Al3+)=0.2mol/L.此时所得沉淀中
硫酸亚锡(SnSO4)是一种重要的硫酸盐,主要用于电镀工业的镀锡、铝合金表面的氧化着色、印染工业的媒染剂、双氧水去除剂等。某研究小组设计SnSO4制备路线如下:

查阅资料:
Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成难溶物Sn(OH)Cl(碱式氯化亚锡)。
请回答下列问题:
(1)SnCl2粉末需加浓盐酸进行溶解,请用平衡移动原理解释原因 。
(2)加入Sn粉的作用有两个:①调节溶液pH ② 。
(3)反应Ⅰ生成的气体为CO2,得到的沉淀是SnO。该沉淀经过滤后需漂洗,如何证明沉淀已经洗涤完全? 。
(4)多步操作包含的具体实验步骤的名称可以是: 。
(5)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是 。
(6)该小组通过下列方法测所用锡粉样品的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:Sn + 2HCl→SnCl2 + H2↑;
②加入过量的FeCl3 ;
③用已知浓度的K2Cr2O7滴定生成的Fe2+,发生的反应为:6FeCl2 + K2Cr2O7 + 14HCl →6FeCl3 + 2KCl + 2CrCl3 +7H2O
取1. 226 g 锡粉样品,经上述各步反应后,共用去0.1000 mol/L K2Cr2O7溶液32.00 mL。则该锡粉样品中锡的质量分数是
查看习题详情和答案>>

C(s)+1/2O2(g)==CO(g) △H=-110.5kJ/mol
2Fe(s)+3/2O2(g)===Fe2O3(s) △H=-822.1kJ/mol
请写出C还原Fe2O3生成CO的热化学方程式___________________________。
(2)反应2CO+O2
 2CO2的平衡常数为K1;反应4Fe+3O2
2CO2的平衡常数为K1;反应4Fe+3O2 2Fe2O3的平衡常数K2,则反应
2Fe2O3的平衡常数K2,则反应3CO+Fe2O3
 2Fe+3CO2的平衡常数K与K1、K2的关系式___________。
2Fe+3CO2的平衡常数K与K1、K2的关系式___________。(3)高温下,氧化铁能跟碳发生下列反应:
① Fe2O3+3C
 2Fe+3CO ② Fe2O3+3CO
2Fe+3CO ② Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2 若反应产生的气体是CO2和CO,则
 的取值范围是_________________。
的取值范围是_________________。(4)氯化炉中生成的气体,通常用碱性的亚硫酸钠溶液来吸收,请用离子方程式分析亚硫酸钠溶液呈碱性的原因____________________。
(5)氯化炉中发生:3Cl2(g)+3C(s)+Al2O3(s)
 2AlCl3(g)+3CO(g) △H>0,欲提高金属铝的氯化效果,不可采取的措施是______(填序号):
2AlCl3(g)+3CO(g) △H>0,欲提高金属铝的氯化效果,不可采取的措施是______(填序号): ①增加C的量 ②多通入Cl2 ③升高温度 ④移走部分AlCl3(g)
⑤使用合适的催化剂工业上还常采用向氯化炉中通入O2的方法,其目的是________________。
(6)沉淀分析法一般规定:溶液中某离子物质的量浓度低于1.0×10-5 mol/L时,可认为已沉淀完全。现向一定浓度的AlCl3和FeCl3的混合溶液中逐滴加入氨水,当Fe3+完全沉淀时,测定c(Al3+)=0.2mol/L。此时所得沉淀中_____(填“是”或“否”)含有Al(OH)3。(已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.1×10-33)。
(1)已知:C(s)+
| 1 |
| 2 |
| 3 |
| 2 |
请写出C还原Fe2O3生成CO的热化学方程式______.
(2)反应2CO+O2
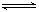
2CO2的平衡常数为K1;反应4Fe+3O2
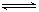
2Fe2O3的平衡常数K2,则反应3CO+Fe2O3
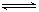
2Fe+3CO2的平衡常数K与K1、K2的关系式______.
(3)高温下,氧化铁能跟碳发生下列反应:
①Fe2O3+3C
| ||
| ||
| n(C) |
| n(Fe2O3) |
(4)氯化炉中生成的气体,通常用碱性的亚硫酸钠溶液来吸收,请用离子方程式分析亚硫酸钠溶液呈碱性的原因______.
(5)氯化炉中发生:3Cl2(g)+3C(s)+Al2O3(s)
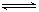
2AlCl3(g)+3CO(g)△H>0,欲提高金属铝的氯化效果,不可采取的措施是______(填序号):
①增加C的量 ②多通入Cl2③升高温度 ④移走部分AlCl3(g) ⑤使用合适的催化剂工业上还常采用向氯化炉中通入O2的方法,其目的是______.
(6)沉淀分析法一般规定:溶液中某离子物质的量浓度低于1.0×10-5mol/L时,可认为已沉淀完全.现向一定浓度的AlCl3和FeCl3的混合溶液中逐滴加入氨水,当Fe3+完全沉淀时,测定c(Al3+)=0.2mol/L.此时所得沉淀中______(填“是”或“否”)含有Al(OH)3.(已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.1×10-33).